Br J Cancer:靶向细胞自噬作用改善乳腺癌治疗中PARP抑制剂耐药性的产生
2021-01-25 xiaozeng MedSci原创
乳腺癌作为全球女性中最常见的癌症之一,也是癌症相关死亡的主要原因。
乳腺癌作为全球女性中最常见的癌症之一,也是癌症相关死亡的主要原因。据国际癌症研究机构的估计,在2018年全球约有200万新病例和60万乳腺癌相关死亡病例,尽管该疾病的检测技术和治疗策略在过去的二十年中已显著改善,但化疗耐药性的产生仍是乳腺癌治疗过程中的一大挑战。
目前的乳腺癌治疗策略中较新的进展之一为靶向PARP的治疗策略。既往研究显示,PARPs在多种细胞过程中具有关键作用,并成为了具有吸引力且可行的药物靶标。在BRCA突变的乳腺癌患者中,PARP抑制剂(PARPi)显示出了潜在的单药抗肿瘤功效。
然而,PARPi治疗成功受限于携带BRCA1/2突变的一小部分乳腺癌患者(<10%)。此外,BRCA突变乳腺癌患者中获得性耐药的产生也会导致PARPi治疗的失败。且大多数BRCA野生型(WT)乳腺癌患者对PARPi具有内在耐药性。因此,目前急需一种可广泛应用于乳腺癌患者和对PARPi具有耐药性的患者的治疗策略。
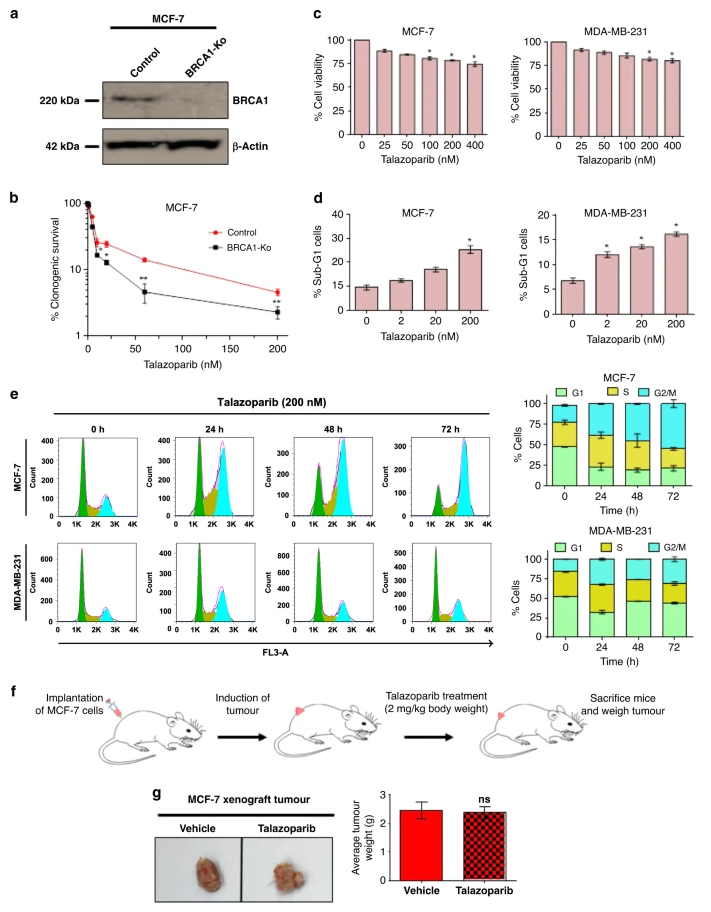
BRCA-WT乳腺癌细胞对他拉唑帕尼单药治疗具有内在耐药性
细胞自噬是一种去除功能异常和多余的生物分子和细胞器的细胞内稳态机制。既往研究显示,抑制细胞自噬作用会导致HR的降低和NHEJ的升高。然而,目前尚不清楚细胞自噬的激活是否与BRCA-WT乳腺癌对PARPi的耐药性相关,且靶向细胞自噬是否有益于PARPi的治疗效果。
该研究旨在评估细胞自噬在疾病耐药性中的作用,并探究潜在的分子机制。研究人员通过检测乳腺癌细胞中内源性LC3-II的表达水平,以及异位表达EGFP-LC3和mRFP-EGFP-LC3来评估自噬体的形成和自噬通量。采用CRISPR-Cas9系统敲除BECN1、ATG5、p62/SQSTM1和LAMP1来构建自噬缺陷型细胞。在自噬能力强和有缺陷的乳腺癌细胞以及移植瘤小鼠模型中评估对PARPi的反应。
细胞自噬的药理抑制使BRCA1-WT移植瘤对PARPi治疗致敏
研究人员发现,他拉唑帕尼(talazoparib)治疗的BRCA-WT乳腺癌细胞系的细胞自噬水平显著增强。自噬缺陷型细胞致敏于他拉唑帕尼。移植瘤小鼠模型显示,靶向自噬能够协同增强他拉唑帕尼在BRCA1-WT乳腺癌细胞中的治疗效果。
机制研究显示,氯喹(chloroquine)的自噬抑制作用能够促进有害的NHEJ介导的DSB修复过程,并最终导致广泛的基因组不稳定和细胞有丝分裂障碍。
综上,该研究结果显示,细胞自噬作用能够引起PARP抑制剂他拉唑帕尼耐药性的产生。而抑制细胞自噬作用则能够改善PARPi的治疗效果,该发现也为之后临床上的应用提供了一定的理论依据。
原始出处:
Pai Bellare, G., Saha, B. & Patro, B.S. Targeting autophagy reverses de novo resistance in homologous recombination repair proficient breast cancers to PARP inhibition. Br J Cancer (21 January 2021).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#靶向细胞#
81
#抑制剂#
78
#细胞自噬#
0
#PARP#
94