Gastroenterology:兰州大学焦作义团队发现胰腺癌吉西他滨耐药的潜在机理
2023-03-15 iNature iNature 发表于上海
尽管小部分患者亚群受益于当前的靶向策略或免疫治疗,但吉西他滨仍然是胰腺癌(PC)治疗的一线药物。
尽管小部分患者亚群受益于当前的靶向策略或免疫治疗,但吉西他滨仍然是胰腺癌(PC)治疗的一线药物。然而,吉西他滨耐药普遍存在,危及长期生存。
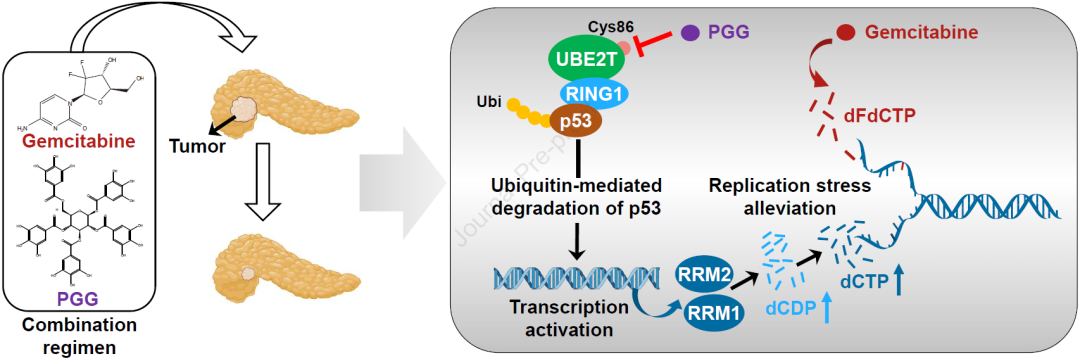
2023年2月24日,兰州大学焦作义团队在Gastroenterology在线发表题为“Targeting UBE2T potentiates gemcitabine efficacy in pancreatic cancer by regulating pyrimidine metabolism and replication stress”的研究论文,该研究结合蛋白质组学和代谢组学研究UBE2T对嘧啶代谢重塑的影响。该研究发现Ube2t 缺失的自发性PC小鼠在吉西他滨治疗后具有明显的生存优势,临床患者中Ube2t 水平与吉西他滨耐药呈正相关。在机制上,UBE2T催化RING1介导的p53泛素化,缓解RRM1和RRM2的转录抑制,导致不受约束的嘧啶生物合成和缓解复制应激。此外,利用类器官进行高通量化合物文库筛选,发现五烯丙基葡萄糖(PGG)是一种有效的UBE2T抑制剂和吉西他滨增敏剂。吉西他滨和PGG联合使用可降低PDX模型中的肿瘤生长,并延长自发性PC小鼠的长期生存期。
总之,该研究发现UBE2T介导的p53降解通过促进嘧啶生物合成和缓解复制应激赋予PC吉西他滨耐药性。这项研究提供了通过靶向UBE2T来提高PC生存率的机会,并开发了一种有前途的吉西他滨敏化剂。
另外,2022年5月25日,兰州大学焦作义、杨靖及兰州华帜天成生物科技王琦共同通讯(兰州大学第二医院秦龙、王龙、张俊昶、周辉年博士研究生为该文共同第一作者)在Science Advances 在线发表题为“Therapeutic strategies targeting uPAR potentiate anti–PD-1 efficacy in diffuse-type gastric cancer”的研究论文,该研究将尿激酶型纤溶酶原激活物受体 (uPAR) 确定为 DGC 的潜在治疗靶点。该研究开发了一种新型抗 uPAR 单克隆抗体,该抗体靶向 uPAR 的结构域 II 和 III,并阻断尿激酶型纤溶酶原激活剂与 uPAR 的结合。该研究使用细胞系来源的异种移植物和患者来源的异种移植物小鼠模型表明,抗 uPAR 和抗程序性细胞死亡蛋白 1 (PD-1) 的组合通过多种机制显著抑制肿瘤生长并延长生存期。此外,基于新型抗 uPAR 的 uPAR 嵌合抗原受体表达 T 细胞可有效杀死 DGC 患者来源的类器官,并在已建立的小鼠模型中表现出生存益处,尤其是与 PD-1 阻断疗法联合使用时。总之,该研究通过以独特的方式靶向 uPAR,为 DGC 治疗提供了一种新的可能性(点击阅读)。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











坚持打卡
106