J Hepatol:南京大学孙倍成/姜润秋/王频发现肝细胞癌中巨噬细胞极化的调控新机制
2023-07-20 iNature iNature 发表于上海
该研究发现XOR-IDH3α轴控制肝细胞癌中的巨噬细胞极化。该研究发现在HCC TAMs中,XOR表达下调,并与患者生存呈正相关,这与肿瘤微环境(TME)的特征,特别是缺氧密切相关。
肿瘤相关巨噬细胞(TAMs)在肝细胞癌(HCC)肿瘤微环境中是不可或缺的。黄嘌呤氧化还原酶 (XOR),也称为黄嘌呤脱氢酶(XDH),参与嘌呤代谢、尿酸生成和巨噬细胞极化至促炎表型。然而,XOR在HCC相关TAMs中的作用尚不清楚。
2023年7月17日,南京大学孙倍成、姜润秋及王频共同通讯在Journal of Hepatology在线发表题为“The XOR-IDH3α axis controls macrophage polarization in hepatocellular carcinoma”的研究论文,该研究发现XOR-IDH3α轴控制肝细胞癌中的巨噬细胞极化。该研究发现在HCC TAMs中,XOR表达下调,并与患者生存呈正相关,这与肿瘤微环境(TME)的特征,特别是缺氧密切相关。
在肝癌小鼠 (Xdhf/fLyz2cre和Xdhf/fClec4fcre)中,该研究者发现单核细胞来源的TAMs 而不是Kupffer细胞中的XOR缺失促进了它们的M2极化和CD8+ T细胞衰竭,从而加剧了HCC的进展。此外,三羧酸循环受到干扰,α-酮戊二酸(α-KG)的生成在XOR缺失的巨噬细胞中增强。XOR通过与IDH3α催化位点 (K142和Q139)相互作用抑制α-KG的产生。IDH3α活性的增加导致TAM中腺苷和犬尿酸的产生增加,从而增强了TAM和CD8+ T细胞的免疫抑制作用。

肝细胞癌(HCC)是世界上最常见的癌症之一。据估计,到2025年,每年将诊断出超过100万例HCC。HCC的高发病率与多种危险因素有关,包括乙型肝炎病毒感染,过度饮酒,代谢性疾病,以及接触黄曲霉毒素等毒素。然而,由于缺乏早期诊断工具和传统治疗方法疗效不佳,HCC的5年生存率很低。
肿瘤相关巨噬细胞(TAMs)是TME的重要组成部分,可分为M1样(促炎)和M2样(抗炎)表型。M2样TAMs是TAMs的主要亚群,促进血管生成、肿瘤生长、免疫逃逸和治疗耐受。鉴于TAMs的促肿瘤作用,已有许多研究对TAMs的功能进行了调节。TAMs在乳腺癌、胰腺癌和肝癌中的研究使用了Lyz2cre小鼠肿瘤模型(骨髓细胞谱系中靶向基因特异性缺失)。然而,在HCC的背景下,由于其高丰度,应考虑Kupffer细胞。它们在生理和病理条件下都起着关键作用。但是,大多数关于肝TAMs的研究并没有区分Kupffer细胞和单核细胞来源的巨噬细胞的作用,因为它们只评估了Lyz2cre小鼠模型的HCC。
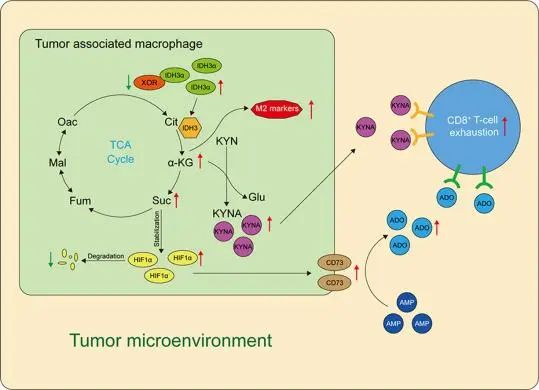
机理模式图(图源自Journal of Hepatology )
黄嘌呤氧化还原酶(XOR)是嘌呤和尿酸代谢以及活性氧和活性氮生成过程中不可缺少的酶。它在痛风、肿瘤发生和器官缺血再灌注损伤等多种疾病中起主要作用。此外,异或是先天免疫系统功能的核心,并将其与适应性免疫系统联系起来。XOR通常被认为是M1巨噬细胞激活的启动子。它可以通过激活NLR家族pyrin domain containing 3 (NLRP3)上调巨噬细胞产生的IL -1β的产生。然而,XOR在HCC相关TAMs中的功能尚未阐明。
总之,该研究揭示了XOR-IDH3α轴在控制 TAM极化和HCC进展中的重要作用。肿瘤微环境的缺氧加重了TAMs的XOR损失。单核细胞来源的TAMs中XOR的缺失促进了HCC的进展,而常驻Kupffer细胞中则没有。这进一步导致单核细胞来源的TAMs通过增加α-KG的产生而增加M2-极化,这依赖于IDH3活性的增强。XOR无效的单核细胞衍生的TAMs 通过免疫抑制代谢物(包括腺苷和KYNA)促进CD8+ T细胞衰竭。考虑到过继转移模型的有效性,XOR- IDH3α轴可能是HCC免疫治疗的潜在靶点。
原文链接:
https://doi.org/10.1016/j.jhep.2023.06.022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言