纳米类似药何去何从——再议原研药与仿制药的差异
全国合理用药监测办公室的孙忠实教授应邀分享了“再议原研药与仿制药的差异”主题演讲,从纳米药物的视角剖析了纳米类似药物研发面临的机遇与挑战。
肿瘤资讯 - 纳米类似药,原研药,仿制药 - 2018-05-31
生物类似药领域的里程碑:罗氏赫赛汀安维汀生物类似药获批
肿瘤药咨询委员会一致赞成,批准贝伐单抗和曲妥单抗的生物类似药。 这个专家评审结果,将是生物类似药领域的里程碑。
健点子ihealth - 罗氏,生物类似药,FDA - 2017-07-14
中欧美生物类似药可及性对比
中欧美等国家地区看,欧盟是生物类似药时代的先行者!2006年04月11日,EMA便批准首款生物类似药,即生长激素Omnitrope (somatropin),截止目前,EMA已批准53款生物类似药获批,2款生物类似药上市申请被驳回,其中包括19款单抗,
CPhI制药在线 - 生物类似药 - 2020-01-10
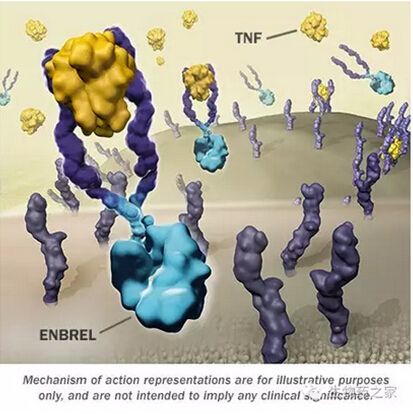
Enbrel生物类似药Erelzi获FDA批准上市
8月30日,FDA宣布批准诺华旗下Sandoz开发的Enbrel(etanercept)生物类似药上市,商品名Erelzi(etanercept-szzs),用于治疗多种炎症疾病,成为FDA批准的第三个生物类似药Enbrel(恩利,通用名:Etanercept,依那西普)是Amgen的一款超级重磅产品,该药是全球最畅销的抗炎药,2014年全球销售额高达90亿美元。 目前,Enbrel在美国已
生物药之家 - Enbrel,生物类似药,FDA - 2016-08-31
中国生物类似药临床应用循证管理指南(2024)
10条推荐意见涵盖了未获批适应证的外推应用、用药前评估、患者教育、用药前预处理、用药方案调整以及临床用药管理等方面,旨在为生物类似药临床应用与管理提供规范化指导,促进其广泛、合理地用于临床治疗。
中国药房 - 生物类似药 - 2024-07-15
Lancet Oncol:生物类似药的曲折前行—LILAC研究
生物类似药的研发和上市也存在严格的标准,需要证明类似药与参照药的疗效是等效的。在乳腺癌的治疗中,已有多项3期研究证实了几种生物类似药与曲妥珠单抗参照药的临床相似性,但尚未有研究评估从曲妥珠单抗转换到生物类似药后的疗效如何。
肿瘤资讯 - 生物类似药,LILAC,乳腺癌,曲妥珠单抗 - 2018-06-15
共话生物类似药的复杂性及监管策略
近年来,生物药快速发展并在治疗肿瘤等疾病方面显示出明显的临床优势。随着原研生物药专利到期、生物药需求增加及生物技术的不断发展,以原研生物药质量、安全性和有效性为基础的生物类似药的研发,有助于提高生物药的可及性和降低价格,满足患者用药需求。为了确保向患者处方最安全、最有效的治疗药物,包括医生和患者在内的所有主要参与者均需了解生物类似药的复杂性,并做出符合患者最大利益的决策。就生物类似药的复杂性及监管
肿瘤资讯 - 生物类似药,监管策略,治疗 - 2019-11-05
FDA 2019:批准45款新药,9款生物类似药
美国FDA的药物评估与研究中心(CDER)已经批准42款新药,9款生物类似药,3款在路上,而生物制品评估与研究中心(CBER)也批准了诺华公司的基因疗法Zolgensma和首款登革热疫苗。
MedSci - FDA,新药 - 2019-12-24
野百合也有春 56个生物类似药绽放
随着美国FDA在生物类似药方面的一系列法规出台,美国乃至全球的生物仿制药市场进入了迅速发展的时期。在3月伦敦举行的欧洲生物类似药物会议上,昆泰艾美仕战略伙伴部门副总裁Per Troein博士展示了研发和市场的最新数据。
健点子ihealth - 生物类似药,FDA,EMA,研发管线 - 2017-04-19
抗肿瘤生物类似药临床转换应用及管理的专家共识
抗肿瘤生物类似药临床转换应用及管理专家共识的制定旨在为抗肿瘤生物类似药转换规则体系的建立及科学监管提供参考。
中国临床药学杂志 - 抗肿瘤生物类似药 - 2024-04-18
抗肿瘤生物类似药治疗药物监测药学专家共识(2020版)
该共识涵盖了临床治疗中进行抗肿瘤生物类似药治疗药物监测的必要性、个体化监测方案要点、临床药师对结果的解读及参与治疗等。
中日友好医院 - 药物监测,抗肿瘤生物类似药 - 2022-12-17
全球生物制剂拐点:重磅生物药如何应对生物类似药的竞争
摘要:面对生物类似药的激烈竞争,如何成为生物制剂市场的胜者?这两款药皆为强生的重磅炸弹药Remica
生物谷 - 生物药 - 2014-10-08
生物类似药临床药理学研究技术指导原则
近年来,生物类似药的研发和申报日益增多。为规范生物类似药的研发和评价,进一步指导生物类似药临床药理学研究,药审中心组织制定了《生物类似药临床药理学研究技术指导原则》(见附件)。
CDE - 生物类似药 - 2022-04-12
为您找到相关结果约500个