Blood:新诊断FLT3-ITD AML索拉非尼联合强化疗的2期研究失败
2023-09-22 聊聊血液 聊聊血液 发表于上海
一项2期、多中心、随机、安慰剂对照、双盲研究,纳入FLT3-ITD AML 患者以评估索拉非尼联合强化诱导和巩固化疗,随后进行 HCT 或索拉非尼维持治疗的安全性和疗效。
索拉非尼联合强化疗
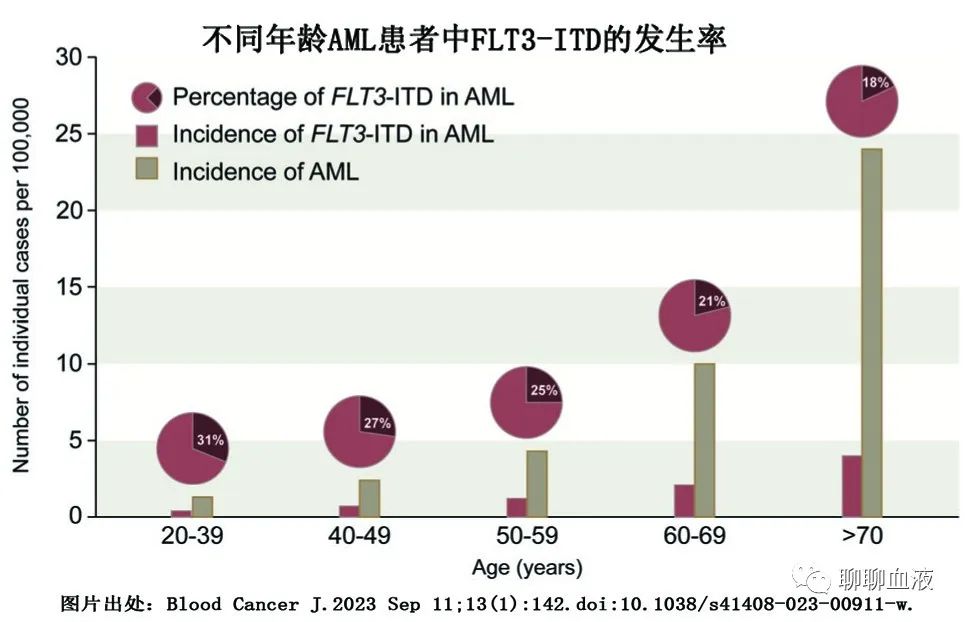
高达30%的新诊断成人急性髓系白血病 (AML) 患者存在FLT3-ITD突变,其与复发风险增加和总生存期 (OS) 缩短相关。已证明 FLT3 激酶活性的小分子靶向治疗是成功的,索拉非尼维持治疗可改善 FLT3-ITD AML患者造血细胞移植 (HCT) 后的结局,尽管索拉非尼强化疗前景良好,但随机数据有限,索拉非尼在 HCT 前 FLT3-ITD AML 患者一线联合强化疗中的作用仍存在争议。
因此澳大利亚Andrew H. Wei教授牵头开展了一项2期、多中心、随机、安慰剂对照、双盲研究,纳入FLT3-ITD AML 患者以评估索拉非尼联合强化诱导和巩固化疗,随后进行 HCT 或索拉非尼维持治疗的安全性和疗效。研究结果近日发表于《Blood》。

研究方法
该研究纳入新诊断的18-65岁FLT3-ITD 突变 AML 患者(FLT3-ITD 等位基因比率≥0.05),研究示意图见图1。
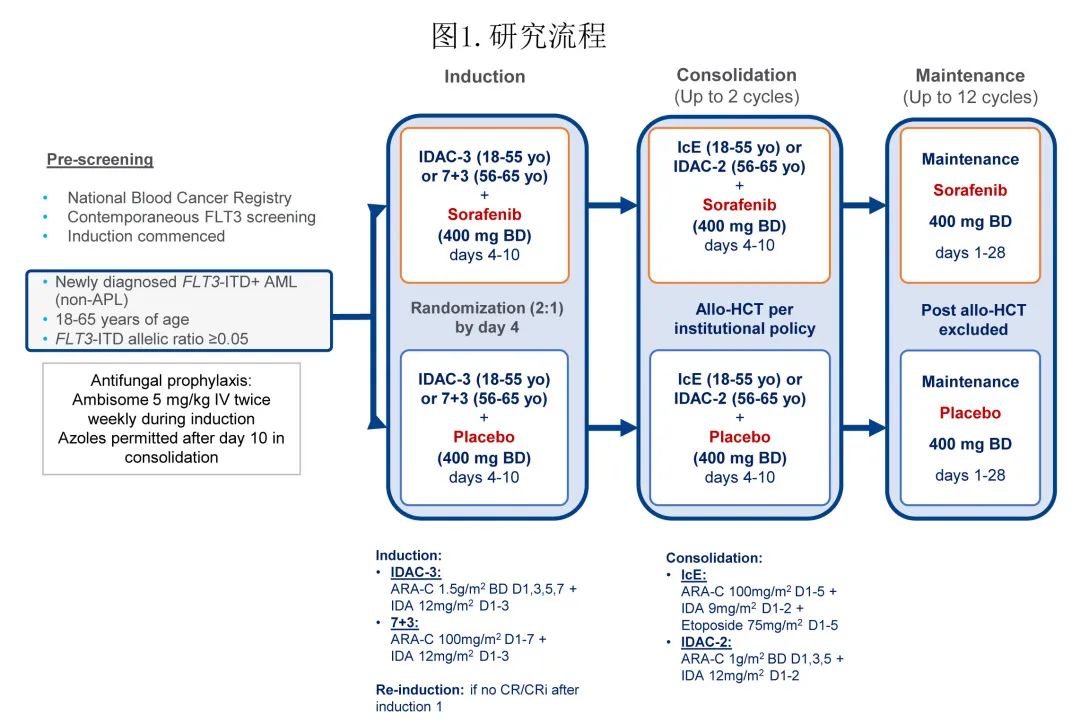
诱导化疗第4天,入组患者以2:1的比例随机接受诱导化疗联合索拉非尼或安慰剂治疗。18-55岁患者接受IDAC-3(阿糖胞苷1.5 g/m2静脉 [IV] 给药2-4小时,每日两次 [BD],第1、3、5和7天;伊达比星12 mg/m2 IV,第1-3天);56-65岁或 FLT3-ITD 阳性CBF AML 患者接受7+3治疗(第1-7天给予阿糖胞苷100 mg/m2,第1-3天给予伊达比星12 mg/m2 IV)。在第4-10天口服索拉非尼或安慰剂400mg BD,共给药14次。为减轻毒性,在伊达比星给药后给予7天疗程的索拉非尼/安慰剂;化疗诱导的血细胞减少症引起的高水平循环 FLT3 配体 (FLT3L) 可抑制 FLT3 抑制剂活性,将索拉非尼暴露限制在诱导的第4-10天可尽量减少索拉非尼对高水平 FLT3L 的暴露。
诱导治疗后未达到完全缓解 (CR) 或 CR 伴不完全血液学恢复 (CRi) 的患者允许接受与第一个周期相同的第二个诱导周期。如果再诱导治疗后未达到CR/CRi,则中止方案治疗。达到 CR/CRi 的患者接受巩固化疗:18-55岁患者接受了2个周期的IcE(第1-2天伊达比星9 mg/m2 IV,第1-5天阿糖胞苷 100 mg/m2连续 IV 输注,第1-5天依托泊苷75 mg/m2 IV);56-65岁患者接受2个周期的IDAC-2(第1、3和5天 BD 2-4 小时内阿糖胞苷1 g/m2 IV,第1-2天伊达比星12 mg/m2 IV);CBF AML 患者在第1、3和5天接受3个周期的阿糖胞苷1.5 g/m2 IV 2-4小时BD。在所有巩固周期中,从第4-10天口服索拉非尼或安慰剂400 mg BD,共给药14次。维持治疗期间,在开始末次巩固治疗周期后不早于第42天给予索拉非尼或安慰剂400 mg BD,但如果等待中性粒细胞恢复至1.0 x 109/L和血小板恢复至75 x 109/L,则不晚于第90天。维持治疗最多持续 12 x 28 天周期。患者可随时停止治疗并进行allo-HCT,但不允许移植后使用索拉非尼或安慰剂(招募时索拉非尼维持治疗尚不是标准治疗)。
主要终点为无事件生存期(EFS),次要终点包括安全性、缓解率、无复发生存期(RFS:存活患者从 CR/CRi 日期至复发、死亡或末次随访日期)和OS。
研究结果
患者特征
共102例患者符合入组条件并随机,其中3例未接收治疗(索拉非尼组2例,安慰剂组1例),1例复核为FLT3-ITD阴性而排除,98例患者形成最终分析集。
两组之间的基线特征平衡(表1)。中位年龄为49岁。研究入组时的中位 WCC 为35.7 × 109/L,FLT3-ITD等位基因比率≥0.7的患者比例为29%。两组的 FLT3-ITD 长度和插入部位特征相似。安慰剂组并发 NPM1 突变为81%,索拉非尼组为60%(p=0.07)。在索拉非尼组和安慰剂组中,分别有78%和79%的患者开始巩固治疗,32%和27%的患者开始维持治疗。

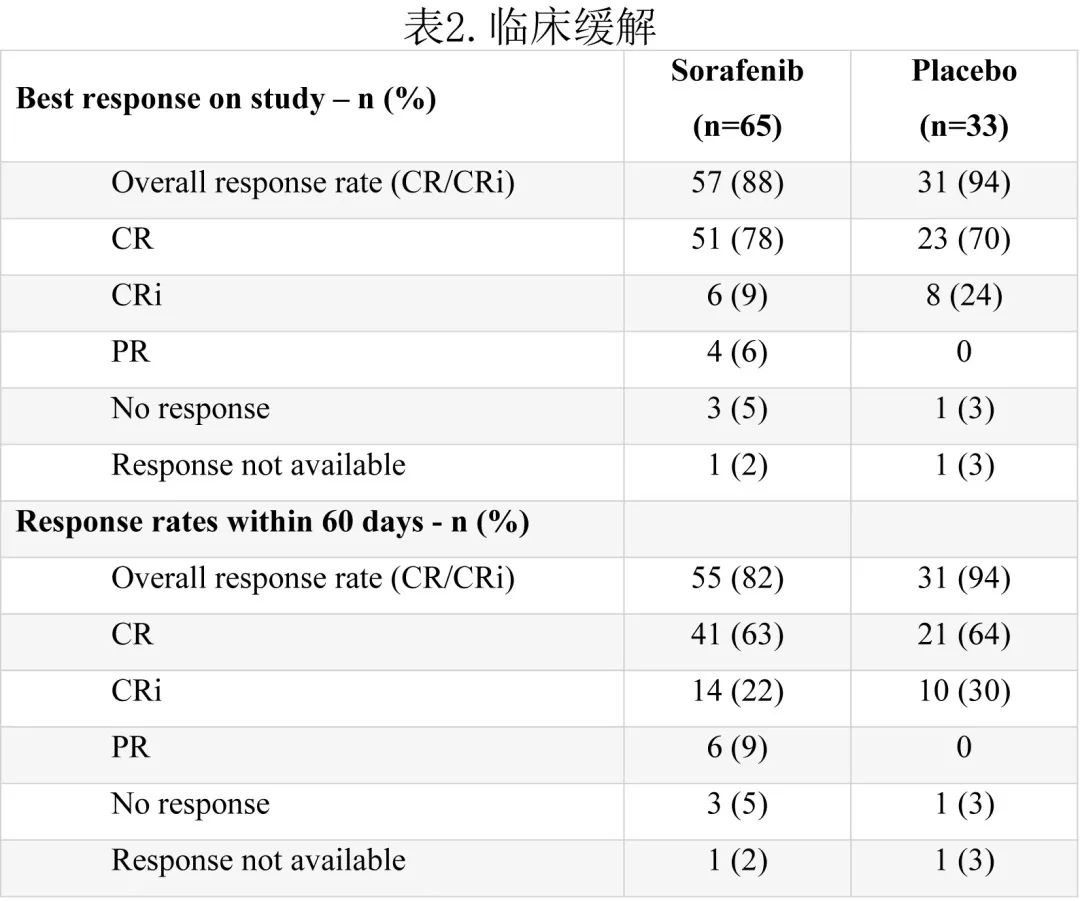
临床缓解
索拉非尼组的客观缓解率 (ORR;CR/CRi) 为88%(57/65),安慰剂组为94%(31/33)(p=0.49),分别有78%和70%达到CR(p=0.46)(表2)。首次诱导后,索拉非尼组7例患者 (11%) 出现部分缓解,其中3例患者在第2个化疗周期后达到CR/CRi,其余4例患者退出研究接受治疗,因此被指定为治疗失败。在接受更强化 IDAC-3 诱导的年轻患者中,索拉非尼组的 CR 率为82%,而安慰剂组为65%(p=0.14)。总体而言,索拉非尼组48例 (74%) 患者和安慰剂组21例 (64%) 患者继续接受HCT;分别有40例 (62%) 和安慰剂组19例 (58%) 患者是在首次缓解时接受移植。从研究随机化至移植的中位时间为4.2个月。
EFS、RFS和OS
中位随访时间为49.1个月,两组的EFS无差异 (HR=0.87)(图2A),索拉非尼组的2年 EFS 为47.9%,安慰剂组为45.4% (p=0.61)(图2A)。对于RFS,索拉非尼组的2年估计值为54%,而安慰剂组为40% (HR=0.76)(图2B)。还评估了仅限于 CR 缓解者并在60天时标记的EFS (EFSCR60),索拉非尼组的2年EFSCR60为38%,安慰剂组为30%(HR=0.81)。索拉非尼组的2年 RFS CR60为61%,安慰剂组为36%(HR=0.64)。
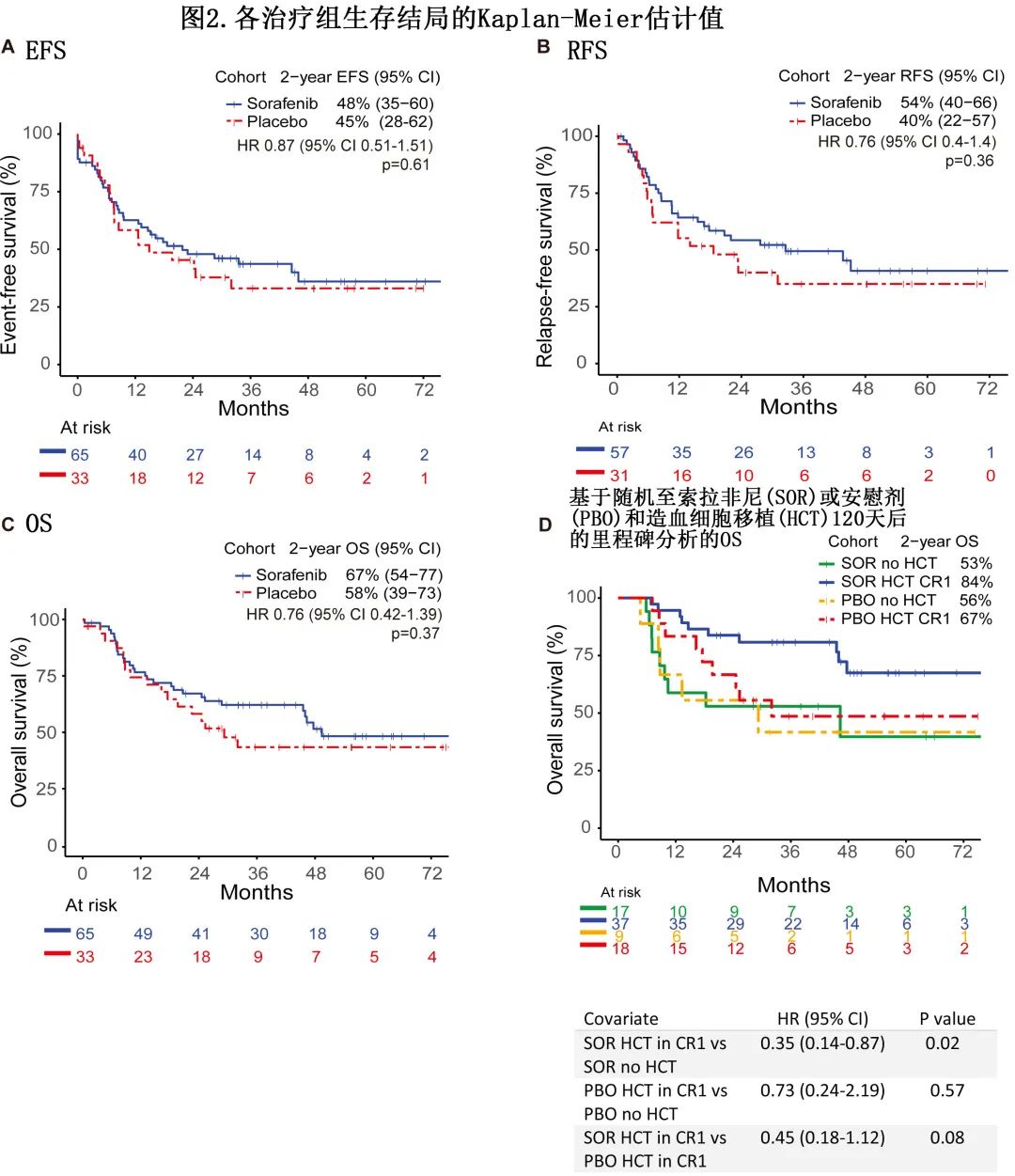
两组的 OS 无差异,索拉非尼组的2年 OS 为67%,安慰剂组为58%(HR=0.76)(图2C)。为了评估 allo-HCT 对结局的影响,在第60、90和120天进行了里程碑分析,以解释与 HCT 相关的时间依赖性偏倚。使用120天标志性时间点作为代表性示例,与未移植患者相比,首次缓解时移植的索拉非尼组患者的2年 OS 显著延长 (84% vs 53%,HR=0.35;p=0.02),表明 allo-HCT 作为缓解后治疗具有获益(图2D);而安慰剂组的 HCT 似乎没有获益。接下来确定了索拉非尼与安慰剂对首次缓解并进行 allo-HCT 的患者的影响:索拉非尼组的2年 OS 为84%,安慰剂组为67%(HR=0.45;p=0.08);如果在第60天或第90天以随机化后的生存期为标志,则观察到相似的结局。
安全性
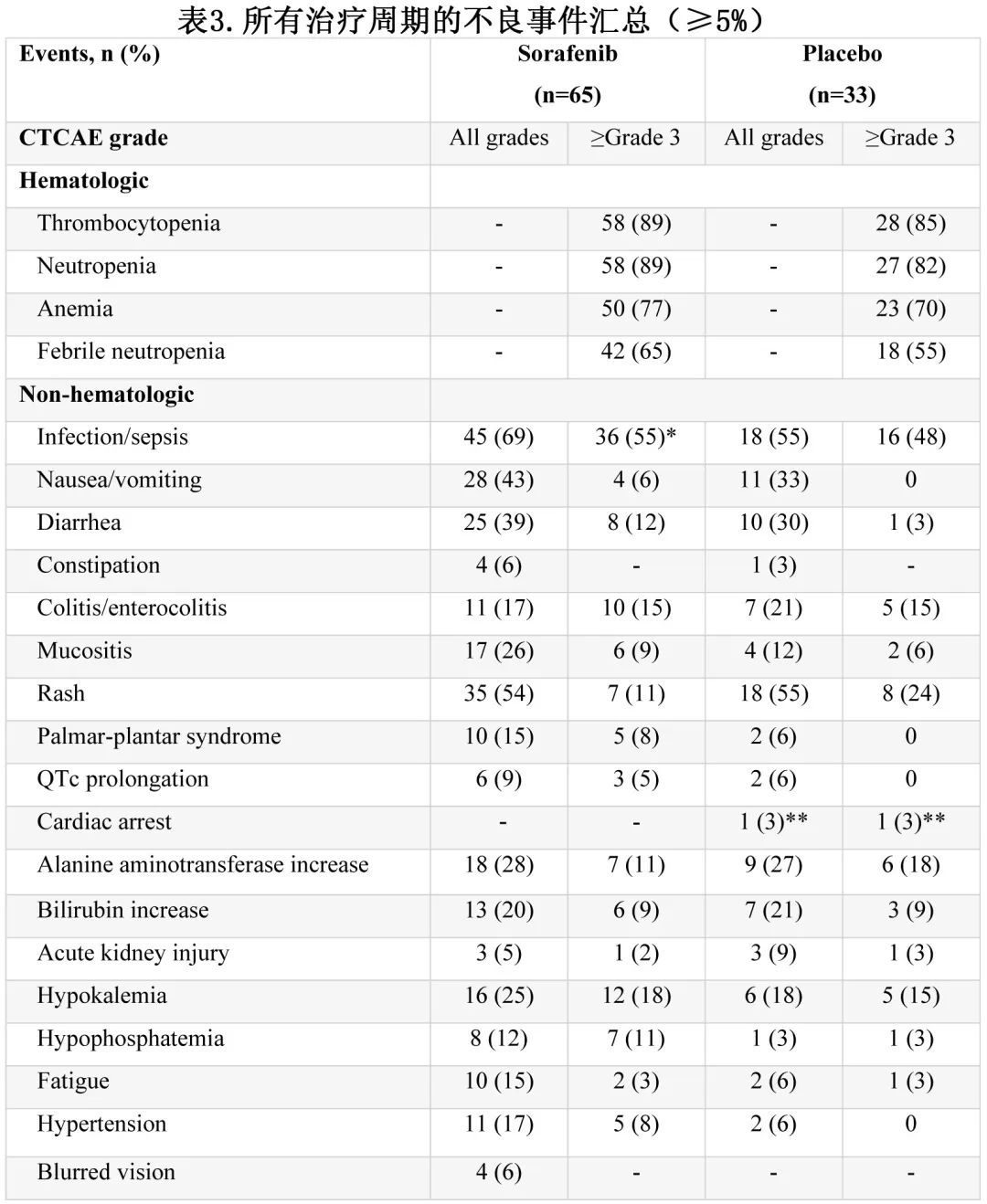
考虑到所有治疗周期中至少5%的患者发生的不良事件,两个治疗组≥3级血液学毒性的发生率相似,索拉非尼组和安慰剂组分别有65%和55%的患者报告发热性中性粒细胞减少(表3)。索拉非尼组和安慰剂组最常见的≥3级非血液学毒性分别为感染/脓毒症 (55% vs 48%)、皮疹 (11% vs 24%)、丙氨酸氨基转移酶升高 (11% vs 18%) 或小肠结肠炎 (15% vs 15%)。索拉非尼组掌跖综合征(任何等级)的发生率更高(15% vs 6%;≥3级:8% vs 0%),QTc间期延长也是如此(≥3级:5% vs 0%)。索拉非尼组的30天死亡率为2%(1例脓毒症/多器官衰竭患者),安慰剂组为3%(1例心脏骤停患者)。
还进行了探索性分析,显示诱导治疗后 FLT3-ITD MRD阴性状态 (<0.001%) 与2年 OS 改善相关 (83% vs 60%;HR=0.4,p=0.028)。
总结
该安慰剂对照、II期研究将102例18-65岁的新诊断的 FLT3-ITD AML 患者2:1随机分配至索拉非尼组或安慰剂(第4-10天)联合强化诱导治疗组;强化疗包括:伊达比星12 mg/m2第1-3天联合阿糖胞苷第1、3、5、7天1.5 g/m2每日两次(18-55岁)或第1-7天100mg/m2(56-65岁),巩固治疗,随后维持治疗12个月(HCT后不进行维持治疗)。排除4例患者后评估了98例。
两组的CR/CRi率均较高(索拉非尼组78%/9%,安慰剂组70%/24%)。中位随访49.1个月,索拉非尼未改善主要终点EFS(2年EFS 47.9% vs 45.4%;HR=0.87;p=0.61)。索拉非尼组的2年总生存率 (OS) 为67%,安慰剂组为58%(HR=0.76)。对于首次缓解时接受移植的患者,索拉非尼组和安慰剂组的2年 OS 分别为84%和67%(HR=0.45;p=0.08)。
总之,本研究不支持在未经选择的 FLT3-ITD AML 患者中常规使用移植前索拉非尼+化疗。
参考文献
Loo S,et al. Sorafenib plus intensive chemotherapy in newly diagnosed FLT3-ITD AML:a randomized, placebo-controlled study by the ALLG.Blood . 2023 Aug 30;blood.2023020301. doi: 10.1182/blood.2023020301.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












竟然没有改善结果
0