Hypertension 程俊/徐清波课题组揭示高血压增加血管新生内膜形成新机制
2024-01-23 论道心血管 论道心血管 发表于陕西省
研究提出高血压状态下能量代谢驱动损伤血管细胞表型转化的新概念,为高血压状态下血管损伤重构提供新的机理,也从机制角度为临床上预防高血压患者介入术后再狭窄提供新的代谢分子靶点。
血管介入手术是治疗各种缺血性疾病如冠心病和外周动脉疾病的有效方式,然而术后血管再狭窄一直是限制患者晚期预后的核心问题。近年来研究报道高血压是介入术后再狭窄的核心危险因素之一,然而有关其机理及潜在治疗靶点证据严重缺乏。
2024年1月19日,西南医科大学和浙江大学徐清波课题组在心血管领域TOP期刊Hypertension上在线发表题为 “Atlas of Cell Repertoire Within Neointimal Lesions Is Metabolically Altered in Hypertensive Rats” 的研究论文,揭示了高血压状态下损伤血管的动态细胞图谱。免疫细胞、内皮细胞和平滑肌细胞在血管损伤和高血压诱导的动脉重塑过程中均发生代谢重编程,抑制线粒体复合物 III 活性可显著改善高血压状态下血管损伤后重构。研究提出高血压状态下能量代谢驱动损伤血管细胞表型转化的新概念,为高血压状态下血管损伤重构提供新的机理,也从机制角度为临床上预防高血压患者介入术后再狭窄提供新的代谢分子靶点。

首先,作者构建了自发性高血压大鼠(SHR)及对照大鼠(WKY)颈动脉球囊拉伤模型,发现SHR大鼠在血管损伤后重构程度显著高于WKY大鼠。为进一步阐明高血压状态下血管损伤重构加剧的机理,作者进一步利用单细胞测序技术,对稳态血管及损伤后2周及4周血管细胞进行细胞图谱鉴定,通过降维聚类分析得到了主要血管细胞类型如免疫细胞、平滑肌细胞及内皮细胞的表型。发现高血压状态下,血管损伤后各主要血管细胞类型的表型变化轨迹均受到影响,其中改变最为显著的为代谢相关分子通路。
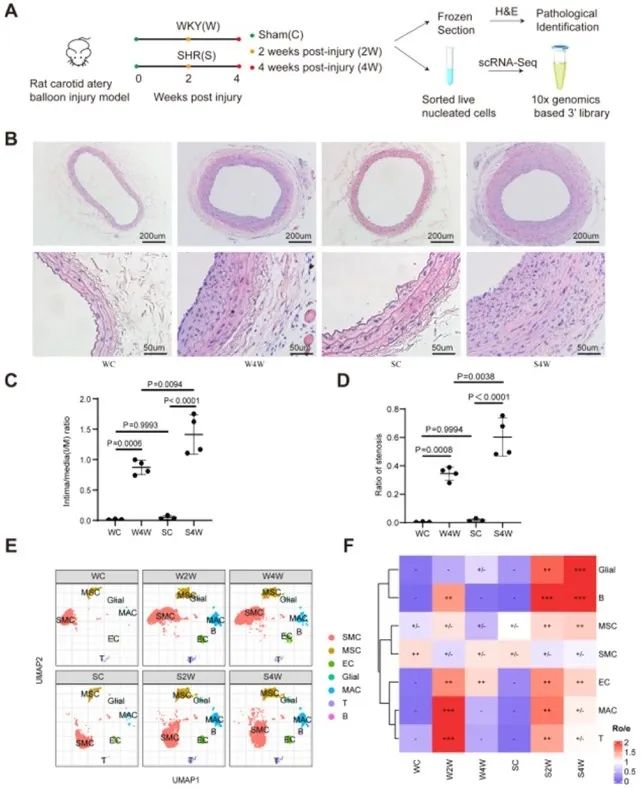
为进一步验证代谢改变是驱动高血压状态下血管损伤后重构的核心机制,作者进一步通过靶向代谢组学探索了损伤后主要代谢物水平改变,其中能量代谢分子及线粒体呼吸链中相关分子包括三磷酸腺苷(ATP)等在高血压状态下的损伤血管中显著上调,这一发现提示线粒体氧化呼吸链可能是介导高血压状态下血管损伤后重构的关键环节。作者最后发现,线粒体复合物III抑制剂(Antimycin A)可以显著改善高血压状态下血管损伤后重构,且其作用独立于血压改变。
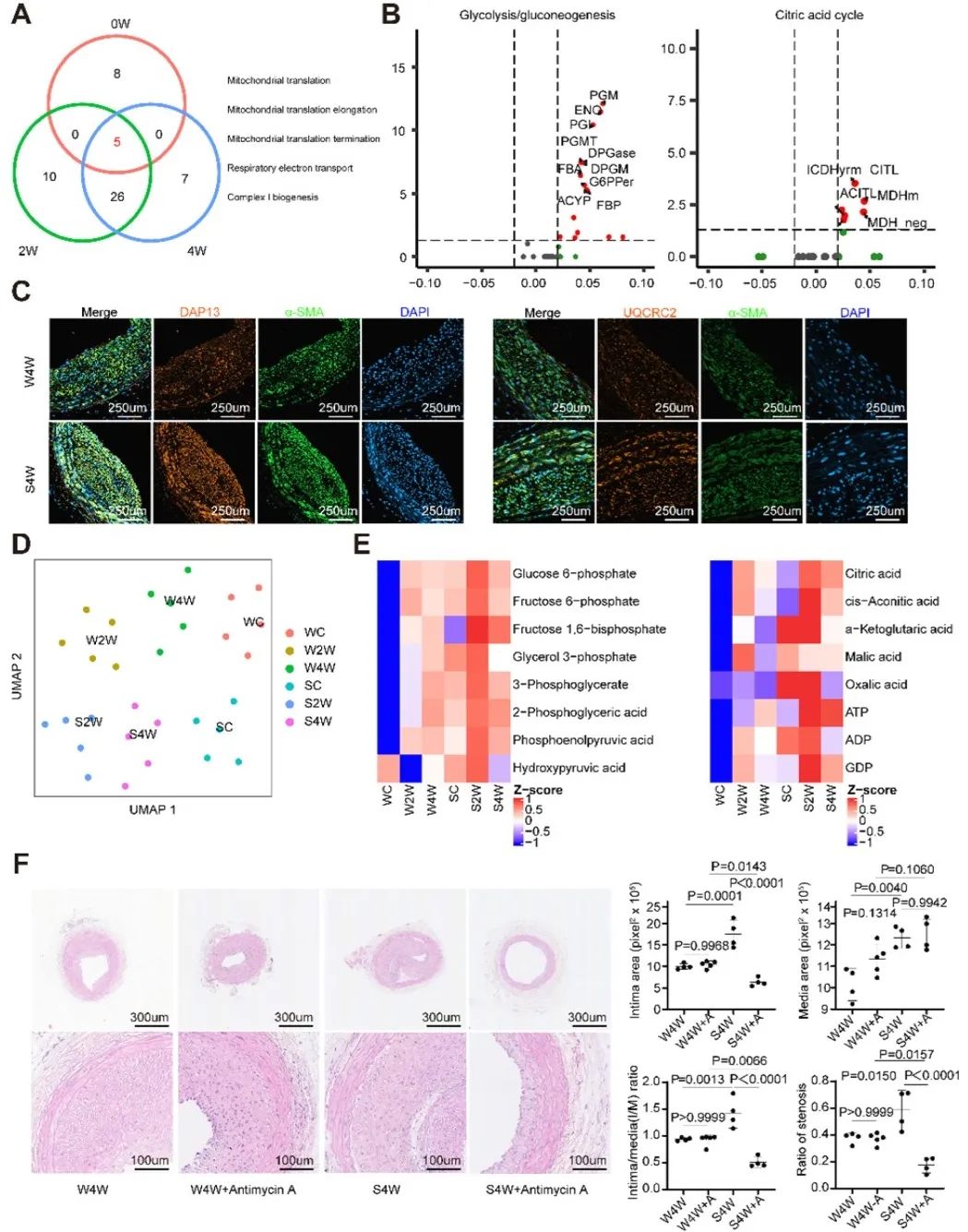
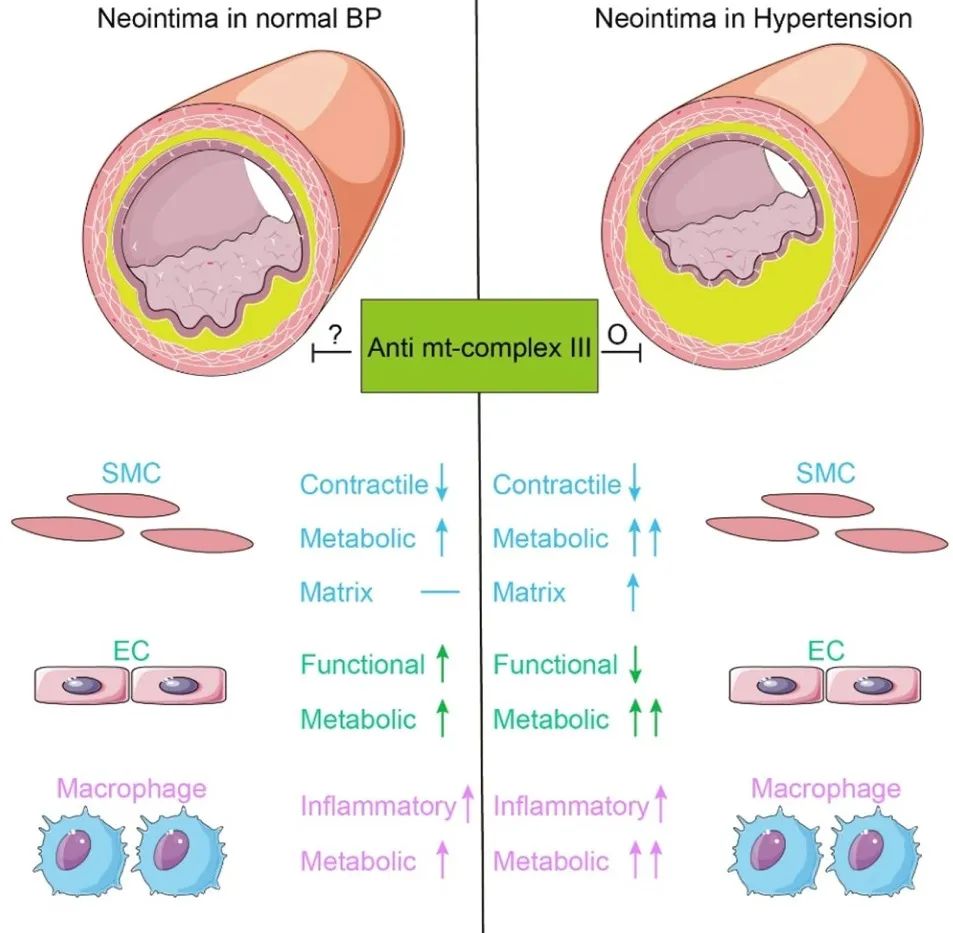
综上所述,本研究利用球囊拉伤血管损伤大鼠模型及单细胞测序技术,揭示了高血压状态下血管损伤重构过程中细胞图谱,证实了能量代谢是免疫细胞、内皮细胞和平滑肌细胞在表型改变过程中核心因素,抑制线粒体复合物 III 活性可显著改善高血压状态下血管损伤后重构。研究提出高血压状态下能量代谢驱动损伤血管细胞表型转化的新概念,为高血压状态下血管损伤重构提供新的机理,也从为临床上预防高血压患者介入术后再狭窄提供新的代谢分子靶点。
浙江大学附属第一医院徐清波教授、西南医科大学程俊教授和伦敦玛丽女王大学Qingzhong Xiao教授为本文的共同通讯作者,西南医科大学附属医院血管外科孙晓磊副主任医师和中南大学湘雅三医院心内科伍俊儒医师为本文共同第一作者,该研究受到浙江大学附属第一医院心内科蒋鎏骏医师、中南大学湘雅三医院蔡菁菁教授、袁洪教授和西南医科大学杨艳教授的指导,并受到国家自然科学基金重点项目、面上项目、博士后面上基金、国家资助博士后人员计划、湖南省荷尖人才项目等课题资助。
原文链接:
https://doi.org/10.1161/HYPERTENSIONAHA.123.22057
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#高血压# #术后再狭窄# #血管新生内膜#
70