Cell Res:贺福初团队发现乳腺癌细胞干性促进机制,开启肿瘤治疗新篇章!
2019-03-25 Ruthy 转化医学网
2018年全球癌症统计报告显示,乳腺癌是女性癌症发病和死亡的最大元凶,发病人数占癌症近1/4,死亡占比也达到了15.0%。随着对乳腺癌发生、发展机制的不断深入研究,乳腺癌干细胞(BCSC)日益受到重视。
导 读
2018年全球癌症统计报告显示,乳腺癌是女性癌症发病和死亡的最大元凶,发病人数占癌症近1/4,死亡占比也达到了15.0%。随着对乳腺癌发生、发展机制的不断深入研究,乳腺癌干细胞(BCSC)日益受到重视。有研究指出,巨噬细胞是构建BCSC生态位的重要助力,然而具体机制却始终扑朔迷离。近日,北京蛋白质组研究中心的研究人员发现,从肿瘤相关巨噬细胞(TAM)旁分泌的跨膜蛋白LSECtin能增强乳腺癌细胞的干性,有望为乳腺癌提供新型治疗方案,开启乳腺癌治疗新篇章!
BCSC:乳腺癌转移复发的罪魁祸首
BCSC是一群未分化、具有自我更新、一定多系分化潜能的细胞,是第一个在实体瘤中被鉴定的肿瘤干细胞。BCSC具有化疗抵抗性、放疗抵抗性、缺氧抵抗性、高致瘤性、高侵袭转移性等特征(即BCSC干性),在乳腺癌的发生发展以及复发转移中发挥重要作用,成为乳腺癌复发的重要原因,并且与乳腺癌预后相关。
BCSC具有无限自我更新能力,可以产生异质性肿瘤细胞,同时具有很强的迁移和侵袭能力,相比实体肿瘤细胞,BCSC更易从原发部位脱离,迁移并侵袭进入淋巴管或血管,随循环到达远处器官,其自我更新能力使肿瘤干细胞大量增殖并分化,最后造成乳腺癌的转移。所以,BCSC就是乳腺癌“无药可治”的真正罪魁祸首。这是否意味着我们真的对BCSC干性无能为力?不是的,有症必有相克之法,要对症下药,最重要的就是要知道“症”从何来。
LSECtin:BCSC形成的推手,乳腺癌转移所对之“症”
恶性乳腺癌“除之不尽,复发难免”,BCSC自然难辞其咎,但是有个问题不能忽略——为什么BCSC总能在多种治疗手段下安然幸存?我们的免疫系统干什么去了?曾有研究指出,TAM旁分泌所形成的特殊免疫微环境对胶质瘤癌症干细胞(CSC)的恶性行为具有显着促进作用,在黑色素瘤中,TAM表达的跨膜蛋白LSECtin还可有效抑制抗肿瘤T细胞免疫反应。那么,对乳腺癌来说,TAM是否也“叛变”了,助了BCSC一臂之力?
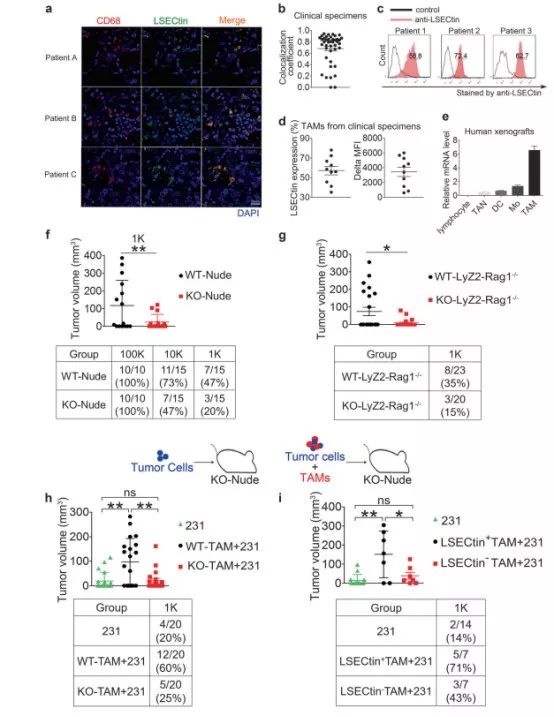
LSECtin存在的 TAM可促使乳腺癌细胞生长
为了究其根由,研究人员收集了42个表达糖蛋白CD68的乳腺癌TAM样本,发现超过70%的样本表达了LSECtin。而后的小鼠模型实验中,研究人员利用乳腺癌的异种移植肿瘤对TAM样本的LSECtin进行观测,发现LSECtin存在的TAM可促使乳腺癌细胞生长。
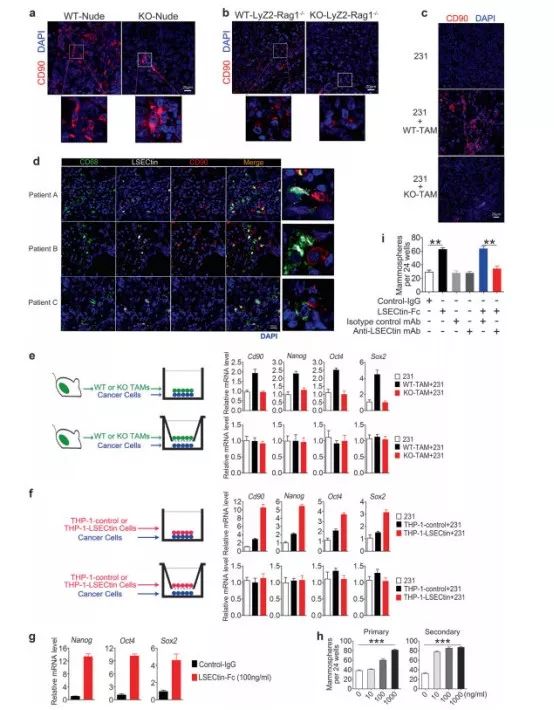
LSECtin可通过接触依赖性方式形成TAM—BCSC交互,促进乳腺癌干性
进一步研究发现,LSECtin可通过接触依赖性方式形成TAM—BCSC交互,促进乳腺癌干性。他们对含有LSECtin的阴性外源基因细胞株(HEK293)进行五轮分选,发现B7家族成员之一BTN3A3对LSECtin有着高度的亲和性,可作为乳腺癌细胞上LSECtin的受体,与LSECtin结合可促进肿瘤细胞干性。也就是说,LSECtin正是BCSC形成的推手,乳腺癌转移复发所对之“症”。

LSECtin与BTN3A3结合可促进乳腺癌干性
既然LSECtin-BTN3A3可促进乳腺癌细胞干性,那么LSECtin-BTN3A3应该有希望成为乳腺癌治疗的靶点。小鼠接种实验的结果表明,注射LSECtin-BTN3A3抗体的小鼠体内乳腺癌细胞数量明显少于对照组,这就说明了LSECtin-BTN3A3作为乳腺癌治疗靶标的可行性。

靶向LSECtin-BTN3A3可降低乳腺癌干性,抑制肿瘤生长
这项研究为乳腺癌治疗提供了一个新的研究思路,明确了BCSC的促进机制,对靶向BCSC的治疗方法的研究具有重要指导意义,为乳腺癌转移和复发的解决拓宽了前进之路。未来,相信减少乳腺癌的不良预后,降低死亡率将逐步实现。
原始出处:Liu D, Lu Q, Wang X, et al. LSECtin on tumor-associated macrophages enhances breast cancer stemness via interaction with its receptor BTN3A3. Cell Res. 2019 Mar 11.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#贺福初#
95
#新篇章#
109
#Cell#
63
#CEL#
96
#癌细胞#
85
#肿瘤治疗#
76