指南推荐|2023年美国肝病学会实践指导:肝细胞癌的预防、诊断和治疗
2023-10-08 临床肝胆病杂志 临床肝胆病杂志 发表于上海
笔者团队摘译专家小组提出的相关指导意见以及图表,供读者参考学习。1HCC的流行病学与预防
2018年,美国肝病学会(AASLD)采用GRADE分级系统评估循证医学证据和建议推荐强度,并制定了肝细胞癌(HCC)治疗指南。该指南主要关注临床实践,回答了医务工作者在评估和管理HCC患者中关心的10个关键问题,具有重要的指导价值。近年来,在临床和基础科研方面,HCC的治疗取得了一些新进展,个性化治疗和前沿技术治疗也逐渐引起了人们的关注。因此,进一步完善和更新HCC的诊断及治疗规范流程并提供全面的临床指导显得尤为必要。为了更好地指导临床实践,AASLD于2023年5月在Hepatology在线发表了《2023年美国肝病学会实践指导:肝细胞癌的预防、诊断和治疗》[1](以下简称“指导意见”),以期为医务工作者对HCC的预防、诊断及治疗提供重要参考和更为准确的建议。笔者团队摘译专家小组提出的相关指导意见以及图表,供读者参考学习。
1HCC的流行病学与预防
指导意见:
(1)应通过制定公共卫生政策和实施干预措施以降低美国HCC显著升高的死亡率(LoE 5,强烈推荐)。
(2)所有新生儿以及出生时未接种HBV疫苗的高风险成年人均应接种疫苗,以降低罹患HCC的风险(LoE 2,强烈推荐)。
(3)所有符合AASLD发布的HBV和HCV感染实践指导中治疗标准的患者均应给予抗病毒药物治疗。在慢性病毒性肝炎患者中,抑制HBV和根除HCV感染可降低HCC的发生风险(LoE 2,强烈推荐)。
(4)应建议慢性肝病患者保持健康的体质量、均衡的饮食并避免烟酒等不良嗜好。与此同时应充分控制包括代谢综合征在内的合并病情。健康的生活方式有多种益处,可以降低罹患HCC的风险(LoE 3,强烈推荐)。
(5)慢性肝病患者建议饮用咖啡,与HCC发生风险降低相关(LoE 5,弱推荐,80%共识)。有研究表明饮用咖啡与降低HCC发生风险之间存在剂量-反应曲线,但尚未有足够数据确定具体的咖啡摄入量。
(6)尽管有证据表明使用化学预防疗法可降低HCC罹患风险,但AASLD不建议使用他汀类药物、阿司匹林、二甲双胍等化学类药物预防HCC的发生(LoE 5,弱推荐)。当患者具有其他适应证的情况下,这些药物可用于治疗慢性肝病(LoE 3,弱推荐)。
2HCC的监测
指导意见:
(7)具有HCC高危因素的患者人群(表1),只要符合HCC治疗条件就应该纳入到HCC监测项目中(LoE 2,强烈推荐)。
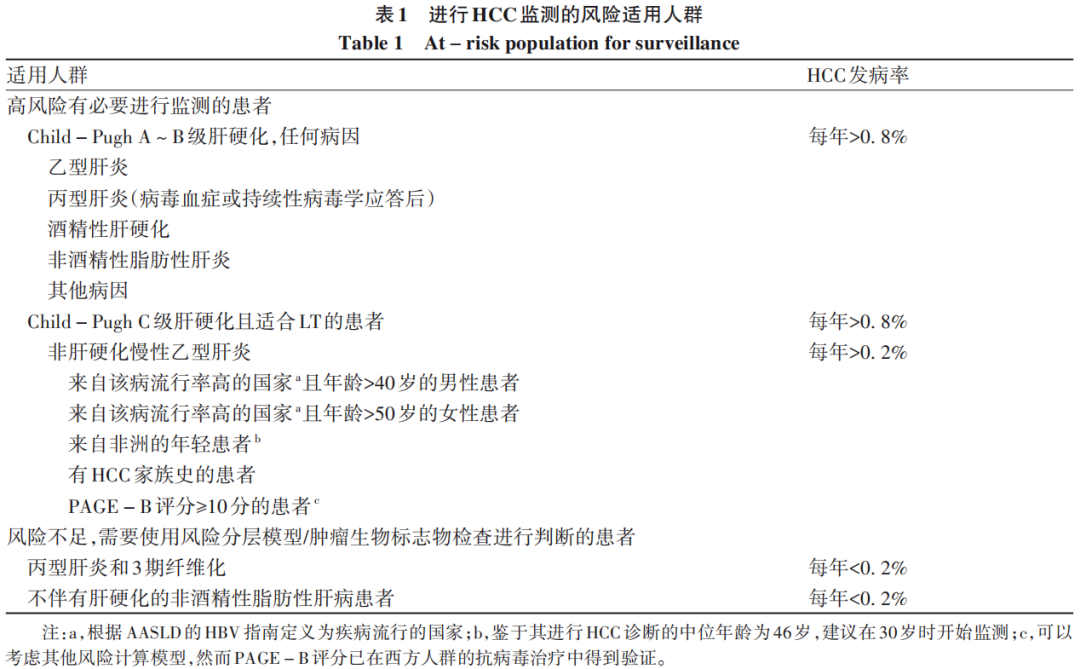
a. Child-Pugh C级的肝硬化患者除非满足行肝移植(LT)的条件,否则不应纳入到监测项目(LoE 3,强烈推荐)。
b. 鉴于早期HCC的发现可能会导致等待LT优先顺序的改变,所有拟行LT的患者应每半年进行一次HCC监测(LoE 3,强烈推荐)。
c. 针对不能行LT或其他定向治疗手段进行补救,同时合并其他疾病且处于善终阶段的患者(寿命预期不足1~2年),AASLD不建议对其进行HCC监测(LoE 5,强烈推荐)。
(8)针对HCV感染获得持续性病毒学应答后伴有晚期纤维化但无肝硬化的患者,AASLD不建议常规进行HCC监测(LoE 3,弱推荐)。
(9)针对患有晚期纤维化但无肝硬化的非酒精性脂肪性肝病患者,AASLD不建议对其常规进行HCC监测(LoE 3,弱推荐)。
(10)建议每半年(6个月)通过联合腹部超声检测和测量甲胎蛋白(AFP)水平进行一次HCC监测(LoE 2,强烈推荐)。鉴于临床实践中HCC监测尚未充分开展,AASLD建议实施最佳监测提醒或类似邮寄监测邀请的监测外展计划等干预措施,以期提高患者HCC监测的依从性(LoE 2,强烈推荐)。
(11)针对存在肝硬化或慢性HBV的HCC高危患者,AASLD不建议对其常规使用 CT或MRI检测以及AFP以外的肿瘤生物标志物检查(LoE 5,弱推荐)。针对腹部超声检测效果不理想的患者,建议考虑增强MRI等其他成像方式进行HCC监测(LoE 3,弱推荐)。
3监测结果的回访与管理
指导意见:
(12)鉴于超声显像对推荐回访程序的影响,应对显像结果进行评估并拟定报告以完成监测检查(LoE 5,强烈推荐)。超声显像结果受限的患者可以接受增强MRI或多相CT进行监测(LoE 5,弱推荐)。
(13)针对腹部超声结果显示病灶直径<1 cm的患者,AASLD建议在3~6个月的时间间隔内重复进行超声和AFP检查(LoE 3,强烈推荐)。针对上述患者,若两次或两次以上随访的超声检查结果保持稳定,则重新回归每半年一次超声和AFP联合检查的监测频率(LoE 5,弱推荐)。
(14)针对超声检查结果中出现任何病灶直径≥1 cm可疑病变的患者应接受多相对比增强CT或MRI进行诊断评估(LoE 1,强烈推荐)。
(15)针对AFP≥20 ng/mL或AFP升高的患者,AASLD建议进行多相对比增强CT或MRI进行诊断评估(LoE 3,强烈推荐)。
4HCC的诊断
指导意见:
(16)针对肝硬化或慢性HBV感染的高危患者,HCC的诊断应基于无创成像标准和/或病理学检查(LoE 1,强烈推荐)。
a. 肝脏成像报告与数据系统(LI-RADS)定义的无创成像标准(图1)应适用于肝硬化或慢性HBV感染的高危患者进行HCC的诊断(LoE 5,弱推荐)。
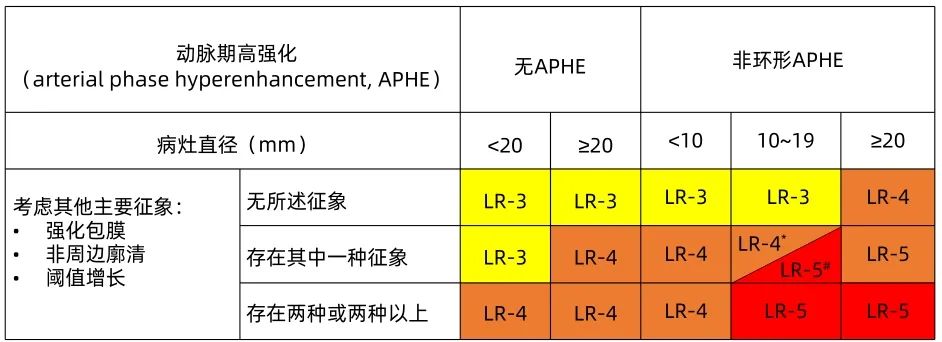
图1 LI-RADS分类
注:*若存在强化包膜;#若存在非周边廓清或阈值增长征象。
b. 针对HCC的病理学诊断应基于国际共识建议并基于标本切片的组织学染色和免疫组化分析(LoE 5,强烈推荐)。
c. 鉴于包括AFP以及液体活检相关的肿瘤生物标志物诊断HCC的准确性不佳,AASLD不建议将其单独用于HCC的诊断(LoE 3,弱推荐)。
(17)鉴于无创成像标准在尚无肝硬化或慢性HBV感染的患者中检测准确性不足,对于此类患者HCC的诊断应通过病理学结果进行证实(LoE 1,强烈推荐)。
(18)HCC的无创性诊断应基于动态增强MRI或多相CT(LoE 1,强烈推荐)。
(19)针对LR-3观察结果的患者,AASLD建议在3~6个月内密切随访,在此期间多次进行横断面成像检查(LoE 2,弱推荐)。
(20)针对LR-4观察结果的患者,AASLD建议进行多学科讨论以确定最佳随访方案,包括在3个月内密切随访以及重复使用对比增强MRI或多相CT成像进行检查或立即进行病理学活检(LoE 2,强烈推荐)。针对即刻诊断HCC后会对管理决策产生影响的患者,AASLD建议进行活检而非重复进行影像学检查(LoE 5,强烈推荐)。
(21)AASLD建议对LR-4和LR-5观察结果患者的活检进行多学科分析以确定HCC诊断或进行分子分型分析(LoE 3,弱推荐)。
(22)考虑到混合性肿瘤和非HCC恶性肿瘤的风险,AASLD建议应对LR-M观察结果的患者进行活检(LoE 1,强烈推荐)。
5HCC的分期
指导意见:
(23)所有HCC患者均应通过腹部多相CT或增强MRI确定分期(LoE 2,强烈推荐)。
a. 针对超过BCLC 0期的HCC患者,AASLD建议应接受胸部平扫CT检查以评估是否存在转移性病灶(LoE 5,强烈推荐)。
b. 鉴于正电子发射计算机断层显像和骨扫描对HCC敏感性较低,AASLD不建议常规使用以确定肿瘤分期(LoE 3,弱推荐)。
(24)在所有HCC患者进行初始治疗评价阶段,均应确定由肿瘤负荷、肝功能障碍程度和美国东部肿瘤协作组体力状况(ECOG PS)评分组成的肿瘤分期并留存证明材料进行记录(LoE 5,强烈推荐)。
(25)尽管目前存在多种分期系统,但AASLD建议使用BCLC分期(LoE 5,强烈推荐)。
(26)鉴于多学科肿瘤委员会讨论已被证明可以更改对影像学结果的判读,AASLD建议采用以确定肿瘤分期(LoE 3,强烈推荐)。
6HCC的多学科护理
指导意见:
(27)HCC患者应在多学科护理的环境中进行讨论和管理(LoE 3,强烈推荐)。
7外科手术治疗
指导意见:
(28)针对不伴有肝硬化的局限性HCC患者,手术切除应是其首选的治疗方法(LoE 2,强烈推荐)。
(29)针对肝硬化患者,若其肿瘤负荷较小、肝硬化代偿良好且临床上无显著的门静脉高压,肝脏残余量充分,AASLD建议应考虑将手术切除作为首选的治疗方法(LoE 2,强烈推荐)。
(30)微创肝切除术(腹腔镜肝切除和机器人辅助肝切除)的选择可提高患者术后恢复情况,并降低围手术期的并发症风险(LoE 3,弱推荐)。
(31)针对所有肝切除术后的HCC患者,AASLD建议每3~6个月使用对比增强多相CT或MRI进行一次常规术后监测以检测是否存在肿瘤复发的情况(LoE 3,强烈推荐)。目前有关肝切除术后监测的最佳时机与持续时间尚不明确,AASLD建议无限期监测(LoE 5,弱推荐)。
(32)针对肝切除术或局部消融术后预计复发风险较高的患者,AASLD建议使用基于免疫检查点抑制剂的术后辅助治疗(LoE 2,强烈推荐)。
a. AASLD建议根据术后复发模型选择辅助治疗手段,采取进展后治疗(图2)(LoE 4,弱推荐)。
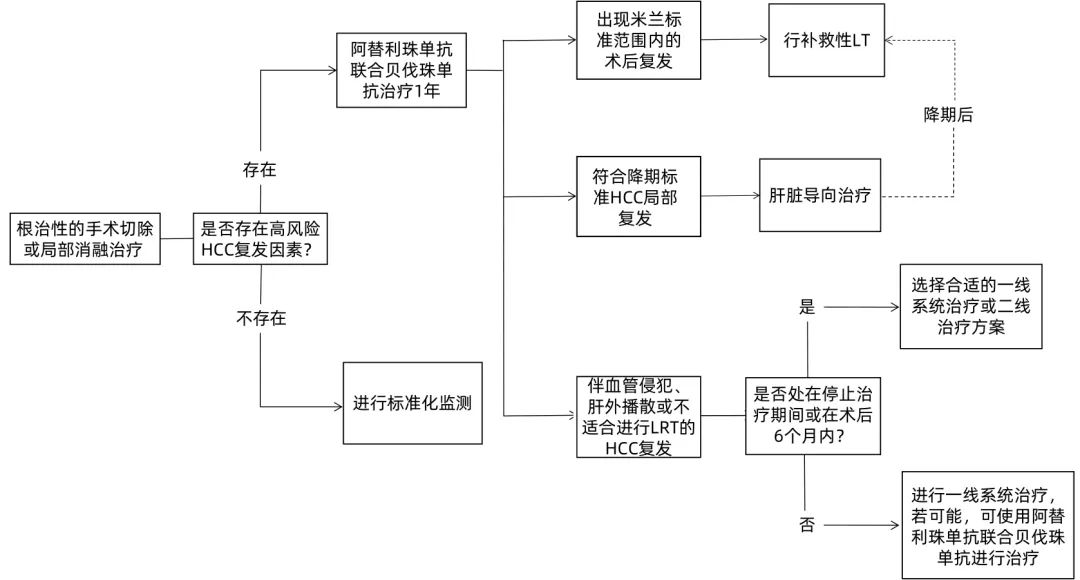
图2 进行辅助治疗期间或之后出现HCC复发的患者管理
注:高风险HCC复发因素包括肿瘤直径5 cm以上;肿瘤个数3个以上;伴有微血管或大血管侵犯;肿瘤分化程度较低。LRT,局部区域治疗。
b. 针对接受肝切除术的患者,AASLD不建议在只根据现有数据而不结合临床试验的情况下对其使用新的辅助治疗方案(LoE 2,弱推荐)。
8LT
指导意见:
(33)针对伴有临床显著门静脉高压和/或处于失代偿期肝硬化的早期HCC患者,若其符合LT条件,则LT应是治疗首选(LoE 2,强烈推荐)。LT应该是肝切除术后米兰标准范围内复发且符合移植标准的HCC患者的治疗选择(LoE 3,强烈推荐)。
(34)针对正在接受评估或列入LT名单中肝脏储备充足的患者,在预期等待时间延长的情况下为降低出现等待过程中途退出的风险,AASLD建议对其采取移植前桥接治疗(LoE 3,强烈推荐)。
a. AASLD并未针对桥接治疗中的LRT提供具体建议。一般而言LRT的选择应基于肿瘤大小、肿瘤位置和中心专家评定(LoE 3,弱推荐)。
b. AASLD不建议常规使用系统治疗作为桥接治疗手段。但系统治疗并不影响患者进行LT的评估(LoE 5,弱推荐)。
(35)针对失代偿期肝硬化发展成T1期HCC且符合LT条件的患者,AASLD建议在进行LRT之前至少每3个月进行一次影像学监测,直到满足终末期肝病模型额外进行加分的标准(LoE 3,弱推荐)。若患者出现AFP显著升高或不再适合进行LT的情况,可考虑立即行LRT(LoE 3,弱推荐)。
(36)针对初始肿瘤负荷满足除米兰标准以外的其他符合移植筛选标准,特别是符合器官共享联合网络(UNOS)降级标准的患者,AASLD建议应在3~6个月的观察期成功降级符合米兰标准后考虑LT(LoE 2,强烈推荐)。AFP>1 000 ng/mL的HCC患者必须降至AFP<500 ng/mL方可视为降期(LoE 2,强烈推荐)。
(37)AASLD建议使用多相对比增强腹部CT或MRI和胸部CT扫描以监测移植后HCC复发(LoE 2,强烈推荐)。移植后监测的最佳时机和持续时间尚不明确,但可以考虑风险分数引导决策。
9局部消融治疗
指导意见:
(38)针对单个肿瘤直径≤5 cm的HCC患者,若其不适合或拒绝进行手术治疗,AASLD建议应采用局部消融治疗进行根治性治疗(LoE 1,强烈推荐)。
(39)针对肿瘤直径≤3 cm早期HCC患者,若其不适合或拒绝进行手术治疗,肝脏热消融术(射频消融术或微波消融术)应被视为首选治疗方法(LoE 1,强烈推荐)。
(40)针对不适合手术切除的包括肿瘤直径>3 cm在内的BCLC A期HCC患者,靶向放射性栓塞(放射节段切除术)或外放射治疗可用于热消融术的替代疗法(LoE 3,强烈推荐)。
10经动脉治疗
指导意见:
(41)BCLC B期HCC患者应接受经动脉化疗栓塞治疗(LoE 1,强烈推荐)。
(42)AASLD建议经动脉放射栓塞作为BCLC B期HCC患者经动脉化疗栓塞的替代疗法(LoE 3,强烈推荐)。
(43)鉴于肝功能障碍的风险较低,AASLD建议应尽可能以选择性或节段性方式(跨肝叶治疗)进行经动脉治疗(LoE 5,强烈推荐)。
(44)针对BCLC B期HCC患者,AASLD不建议采取未经过临床试验的系统治疗和经动脉治疗联合方案进行治疗(LoE 2,强烈推荐)。
(45)针对因禁忌证、肝功能障碍恶化、HCC出现进展或缺乏客观肿瘤反应等原因不适宜进行局部治疗或局部治疗难治的中度HCC患者,AASLD建议进行系统治疗(LoE 3,强烈推荐)。
11系统治疗
指导意见:
(46)针对肝功能正常(Child- Pugh A级或部分B级肝硬化),ECOG PS 0~1分、BCLC C期HCC或BCLC B期HCC不适合局部治疗或局部治疗后出现进展的患者,AASLD建议对其进行系统治疗(LoE 1,强烈推荐)。
a. Child-Pugh A级肝硬化晚期HCC患者应接受阿替利珠单抗+贝伐珠单抗或度伐利尤单抗+曲美木单抗作为首选一线治疗方案(LoE 2,强烈推荐)。
i. 考虑接受阿替利珠单抗联合贝伐珠单抗治疗的患者应进行食管、胃、十二指肠镜检查(EGD)以评估是否存在静脉曲张或其他胃肠道出血等高危体征(LoE 5,强烈推荐)。
ii.尽管AASLD建议在开始阿替利珠单抗联合贝伐珠单抗治疗之前进行至少一次胃肠道曲张血管绑扎治疗,但针对大静脉曲张最佳治疗方法尚不清楚。卡维地洛可作为阿替利珠单抗+贝伐单抗治疗静脉曲张的替代治疗(LoE 5,弱推荐)。
iii.针对近6个月内出现胃肠道出血和EGD中有出血高风险标记的患者,AASLD建议应在开始阿替利珠单抗+贝伐珠单抗治疗前充分治疗静脉曲张,或可考虑接受度伐利尤单抗+曲美木单抗治疗(LoE 5,强烈推荐)。
b.禁忌使用阿替利珠单抗+贝伐珠单抗和度伐利尤单抗+曲美木单抗的Child-Pugh A级肝硬化患者应接受索拉非尼或仑伐替尼一线治疗(LoE 1,强烈推荐)。
(47)部分Child-Pugh B级肝硬化患者可接受索拉非尼、仑伐替尼或PD-1/PD-L1单抗免疫检查点抑制剂治疗(LoE 3,弱推荐)。
(48)针对肝功能正常(Child-Pugh A级或部分Child-Pugh B级肝硬化)、ECOG PS 0~1分、发生HCC进展或对一线系统治疗不耐受的患者,AASLD建议进行二线治疗(LoE 1,强烈推荐)。
a.若上述患者不符合临床试验条件,AASLD建议使用索拉非尼或仑伐替尼作为一线阿替利珠单抗+贝伐珠单抗后的首选药物(LoE 5,弱推荐)。卡博替尼、瑞格非尼或伊匹木单抗加纳武单抗可用于上述患者(LoE 5,弱推荐)。
b.若上述患者不符合临床试验条件,AASLD建议使用索拉非尼或仑伐替尼作为一线度伐利尤单抗+曲美木单抗后的首选药物(LoE 5,弱推荐)。
c.若上述患者不符合临床试验条件,AASLD建议使用卡博替尼或瑞格非尼(AFP≥400 ng/mL患者可使用雷莫芦单抗)作为索拉非尼或仑伐替尼之后的首选药物(LoE 1,强烈推荐)。派姆单抗(既往未进行免疫暴露的患者)或伊匹木单抗加纳武单抗可用于上述患者。
(49)针对LT后HCC复发的患者,AASLD不建议使用免疫检查点抑制剂治疗,可能会增加移植排斥和死亡的风险(LoE 4,强烈推荐)。AASLD建议使用索拉非尼或仑伐替尼作为上述患者的一线治疗手段。
12预立医疗照护计划(ACP)
指导意见:
(50)针对所有接受姑息治疗或最佳支持治疗的HCC患者,无论其是否符合移植资格,AASLD建议均应提供ACP(LoE 5,弱推荐)。
全文下载
http://www.lcgdbzz.org/cn/article/doi/10.3969/j.issn.1001-5256.2023.09.008
引证本文
王科淳, 王明达, 杨田 .《2023 年美国肝病学会实践指导:肝细胞癌的预防、诊断和治疗》意见要点[J]. 临床肝胆病杂志,2023, 39(9): 2081-2086
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言