癌症中的血液学功能障碍
2023-01-10 小药说药 小药说药 发表于上海
大多数免疫细胞都是寿命短暂的,并且持续地从造血干细胞和祖细胞(HSPCs)中补充。血液学功能障碍在癌症患者中普遍存在,中性粒细胞与淋巴细胞比率升高是常见的诊断和预后指标。
前言
近几十年来,我们对促进癌症控制和介导肿瘤进展的免疫机制的理解不断深入,并借此开发了许多新型免疫疗法和临床应用。然而,我们必须认识到大多数免疫细胞都是寿命短暂的,并且持续地从造血干细胞和祖细胞(HSPCs)中补充。血液学功能障碍在癌症患者中普遍存在,中性粒细胞与淋巴细胞比率升高是常见的诊断和预后指标。
重要的是,近年来,造血功能障碍越来越被认为不仅仅是癌症病理学的副作用,而是癌症疾病的重要全身特征。最近的一些研究进展,包括造血干细胞和祖细胞的癌症相关表型、骨髓生成和红细胞生成功能障碍、髓外造血在癌症中的重要性以及肿瘤相关巨噬细胞的发育起源。这些研究为我们描述了造血功能障碍对癌症免疫抑制的重要贡献、治疗干预的可能途径。总体而言,造血功能障碍是癌症疾病机制的一个重要组成部分,也是治疗干预的重要目标。
癌症中的造血干细胞和祖细胞
造血干细胞和祖细胞是所有血液和大多数免疫细胞谱系的前体。HSPC感知并响应各种压力、危险信号和炎性细胞因子,被认为是全身免疫和炎性反应的活性介质。因此,全面了解抗肿瘤免疫需要深入了解肿瘤对免疫细胞产生途径和HSPC的影响。
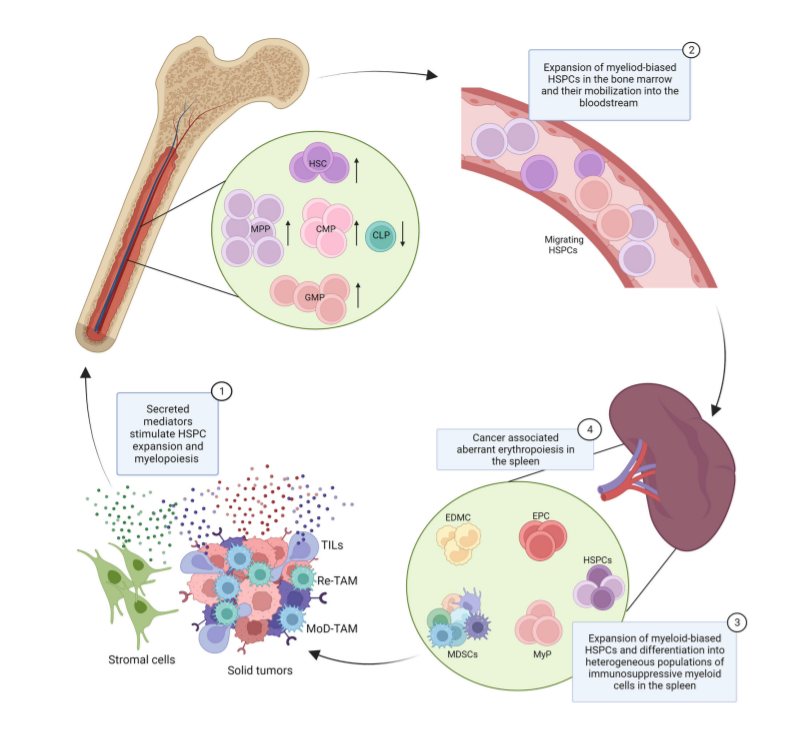
研究表明,在七种不同癌症类型患者的循环中发现HSPCs增加,粒细胞-单核细胞祖细胞(GMPs)显著增加,多能祖细胞(MPPs)和造血干细胞(HSC)显著增加。重要的是,循环GMPs的频率与晚期疾病和预测疾病进展相关。这表明,人类癌症中普遍存在严重的造血失调,并显示其与疾病机制有关。
对小鼠模型的研究为这些结论提供了进一步的支持。在自发乳腺癌的MMTV-PyMT转基因小鼠模型中,免疫抑制髓系细胞在肿瘤内积聚之前,观察到骨髓中HSC、MPPs和GMPs的扩增。在MMTV neu OTI/OTII和其他乳腺肿瘤模型中也观察到了严重的造血功能障碍。这包括骨髓MPP和GMP细胞的扩增、贫血、血小板减少以及小鼠脾脏髓外骨髓生成和红细胞生成的诱导。
此外,在携带B16-F10黑色素瘤的小鼠中,观察到循环淋巴细胞减少,骨髓前B细胞和未成熟B细胞耗竭,表明淋巴细胞生成失调。类似地,在皮下注射同基因EL4胸腺瘤细胞诱导的小鼠癌症模型中,报告了CLPs、NK前体(CD122+NK1.1-CD3-)、NK细胞和B细胞的减少,表明淋巴生成功能紊乱。
癌症中的异常髓系细胞生成
髓系偏向是癌症造血功能障碍的主要特征。它产生具有免疫抑制特性的单核细胞和中性粒细胞的异质群体,这种细胞的丰度是癌症患者预后不良的标志。髓系衍生抑制细胞(MDSCs)广泛概况了此类细胞,它们在表面标记、形态学、基因表达和寿命方面存在显著的异质性。然而,近年来,质谱仪(CyTOF)、scRNA-seq、谱系追踪和其他方法彻底改变了我们对髓系细胞状态异质性的理解,它们具有更广泛的髓系细胞异质性。
癌症中的脾脏髓系细胞生成
脾脏被认为是癌症中免疫抑制性髓系细胞归巢和增殖的重要部位,也是诱导肿瘤抗原耐受的重要场所。最近的研究进一步表明,脾脏也是异常髓系细胞生成的关键部位,这种异常生成会产生促肿瘤性髓系细胞。
有研究表明,在Kras LSL-G12D/+p53 flox/flox(KP)小鼠模型中,癌症进展与小鼠脾脏中GMPs的扩增有关,导致单核细胞和中性粒细胞的局部分化并迁移到肿瘤中。类似地,在肝细胞癌(HCC)的原位小鼠模型中,在肝内注射Hepa1-6细胞后,观察到脾脏HSPCs的显著扩增。此类HSPC保持其长期自我更新的能力,但与骨髓HSPC相反,其骨髓分化潜能受限,并产生具有强大免疫抑制特性的肿瘤相关中性粒细胞。有趣的是,KP肺腺癌小鼠模型中的脾切除术损害了肿瘤内髓系细胞的积聚,并延缓了肿瘤的生长。
此外,在许多疾病中,肝脏也是髓外造血的主要部位。在4T1乳腺癌、B16-F10黑色素瘤或LLC肺腺癌肿瘤的小鼠中,报告了具有免疫抑制特性(CD11b+GR1+)的髓系细胞在肝脏内的积聚。然而,肝脏作为髓系细胞生成部位和免疫抑制性单核细胞和中性粒细胞来源在癌症中的作用仍相对缺乏了解。
促进肿瘤髓系细胞生成的分泌介质
对癌症中驱动脾脏HSPC募集和髓系细胞生成的分子信号的日益理解可能为治疗干预提供了新的策略。GM-CSF是一种重要的炎症介质,其已在多个模型中显示出增强的癌症相关髓系细胞生成。例如,在原位Hepa1-6 HCC小鼠模型中,脾脏HSPCs表达高水平的GM-CSF,抑制其表达会抑制免疫抑制中性粒细胞(CD11b+Ly6G+Ly6Clo)和其他髓系细胞(CD11b+Gr-1+)的产生。然而,GM-CSF同时也具有强大的免疫刺激和辅助特性,此外,GM-CSF也可以对许多癌细胞产生直接影响,促进其增殖和迁移。总之,GM-CSF的多效性使其成为治疗干预的极具挑战性的工具或目标。
M-CSF是单核细胞和组织驻留巨噬细胞发育和维持的重要媒介。其血清水平升高或其受体CSF-1R在肿瘤细胞上的高表达与癌症患者的肿瘤分级和不良预后相关。肿瘤M-CSF的产生也与单核细胞浸润增加相关,可以增强某些癌症模型中单核细胞的免疫抑制特性。CSF-1R的阻断剂或其信号转导的抑制剂在不同的小鼠癌症模型中显示出保护活性,并正在进行临床研究。
其他生长因子和细胞因子也与癌症模型中的造血功能障碍有关。如TNF-α可促进HSPC活化和骨髓生成;G-CSF或IL-1的阻断可使多个组织的免疫细胞数量正常化;原位MMTV-PyMT乳腺肿瘤小鼠中的肿瘤衍生G-CSF也被认为是抑制常规树突状细胞cDC1亚群发育的关键因素。此外,IL-6在胰腺导管腺癌(PDAC)的小鼠模型中参与促进cDC1凋亡和耗竭。
调节肿瘤髓系细胞生成的信号通路
最近的研究证明了未折叠蛋白反应(UPR)及其中介体激酶PERK在肿瘤相关中性粒细胞和单核细胞的产生以及免疫抑制活性中的关键作用。PERK的抑制及其在髓系细胞谱系中的选择性缺失都会增强抗肿瘤免疫活性,减缓多种癌症模型的疾病进展,这种保护活性与髓系细胞中NRF2的抑制和STING信号的上调有关。此外,在肝细胞癌和胃癌患者的脾脏HSPC中观察到PERK激活,并与髓系细胞丰度相关。总体而言,这表明PERK是一种有前途的药物靶点,可以预防癌症免疫逃避。
模式识别受体(PRR)包括多个细胞表面、内吞和细胞内蛋白家族,负责感知微生物化合物和内源性危险信号,从而激活先天免疫和炎症反应。HSPCs表达多种PRR,HSPCs上的细胞固有PRR刺激有助于诱导对感染作出反应的紧急髓系细胞生成。然而,HSPCs上某些PRR的细胞内在刺激是否有助于诱导与癌症相关的紧急髓系细胞生成和免疫抑制仍知之甚少。
最近还发现了其他几种新的途径对癌症相关的髓系细胞生成和免疫抑制很重要。在乳腺癌小鼠模型中,发现视黄酸相关孤儿受体RORC1对肿瘤相关中性粒细胞和单核细胞的分化至关重要,其阻断抑制了肿瘤生长和转移。最近的研究还证明了脂肪酸转运蛋白2(FATP2)在多种小鼠癌症模型中的肿瘤相关中性粒细胞中的重要作用。
肿瘤髓系细胞生成中的表观遗传重编程
在感染性疾病和一些慢性炎症性疾病的背景下诱导紧急髓系细胞生成的特征包括HSPCs的长期表观遗传重编程,这可能导致对后续的免疫反应发生改变。MMTV neu OTI/OTII和其他乳腺肿瘤模型的早期研究表明,HSPC中组蛋白修饰的总体水平发生变化,包括H3K27me3和H3K4me3,并与编码重要表观遗传和转录调节因子的基因表达改变相关,如Ezh2和Hoxa9。总体而言,这支持HSPCs的表观遗传重编程作为癌症造血和免疫功能障碍的可能机制。
红细胞生成功能障碍与癌症免疫机制
几十年来,贫血一直被认为是晚期癌症的共同特征,但最近的研究为癌症中红细胞生成的细胞和分子失调以及其作为癌症进展媒介的意外作用提供了新的机制见解。
研究发现,在皮下接种Lewis肺癌(LLC)或B16-F10黑色素瘤的小鼠模型中,疾病进展与小鼠脾脏中红系祖细胞(EPCs)的积累有关。与在严重贫血中观察到的脾脏内皮祖细胞不同,荷瘤小鼠的脾内皮祖细胞具有强大的免疫抑制特性,在体外抑制CD8+T细胞的增殖和细胞毒性活性,并在体内加速黑色素瘤的进展。重要的是,在癌症患者的血液中也观察到这种能够抑制CD8+T细胞增殖的异常EPCs,其丰度与贫血和免疫抑制相关。
驱动这种癌症相关的红细胞生成功能障碍的分泌介质和信号通路尚不清楚,但血小板衍生生长因子家族成员PDGF-BB在促进髓外红细胞生成中的作用先前已有研究。在这项研究中,T241纤维肉瘤和LLC肺癌小鼠模型中,肿瘤细胞特异性过表达PDGF-BB,并可诱导基质细胞产生红细胞生成素,刺激脾和肝髓外红细胞生成,并促进血管生成和肿瘤生长。
小结
癌症患者的造血功能障碍通常因化疗和放疗方案对造血系统的损害而加剧。这些对抗肿瘤免疫具有复杂的影响,诱导免疫原性癌细胞死亡以引发针对肿瘤抗原的免疫应答,同时也干扰免疫原性和免疫抑制性白细胞亚群的产生。此类方案还增加了癌症患者中克隆性造血的发生率,并易发生与治疗相关的髓系肿瘤。因此,对造血过程生理学、免疫系统和肿瘤之间相互作用的日益了解,有助于开发优化的治疗方案,以最大限度地提高对肿瘤的细胞毒性活性,同时保持造血功能并增强抗肿瘤免疫。
参考文献:
1.Hematologic dysfunction in cancer: Mechanisms, effects on antitumor immunity, and roles in disease progression. Front Immunol.2022; 13: 1041010.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言