罕见病用药再迎曙光!13款新药纳入2024国家医保目录,保障体系持续完善
2024-11-29 梅斯罕见新前沿 MedSci原创
11 月 28 日国家医保局发布 2024 年版药品目录,2025 年 1 月 1 日实施,新增 13 种罕见病药,降低患者负担,标志保障体系完善,展现对民生的关注。
11月28日,国家医疗保障局发布了《国家基本医疗保险、工伤保险和生育保险药品目录(2024年版)》(以下简称《2024年药品目录》),并宣布将于2025年1月1日起正式实施。本次目录调整中,13种罕见病治疗药物成功纳入医保,进一步提升了我国罕见病患者的用药可及性和保障水平。
罕见病长期因患者群体小、研发成本高而面临“药贵”“无药”的困境。国家医保局通过谈判和竞价方式,将13种高临床价值的罕见病治疗药物纳入医保目录,为患者带来了福音。这些药物涵盖了多种严重影响患者生活质量甚至威胁生命的罕见病。据统计,截至2024年,共有90余种罕见病相关治疗药物被纳入国家医保药品目录,覆盖了《第一批罕见病目录》和《第二批罕见病目录》中大部分罕见病种类。
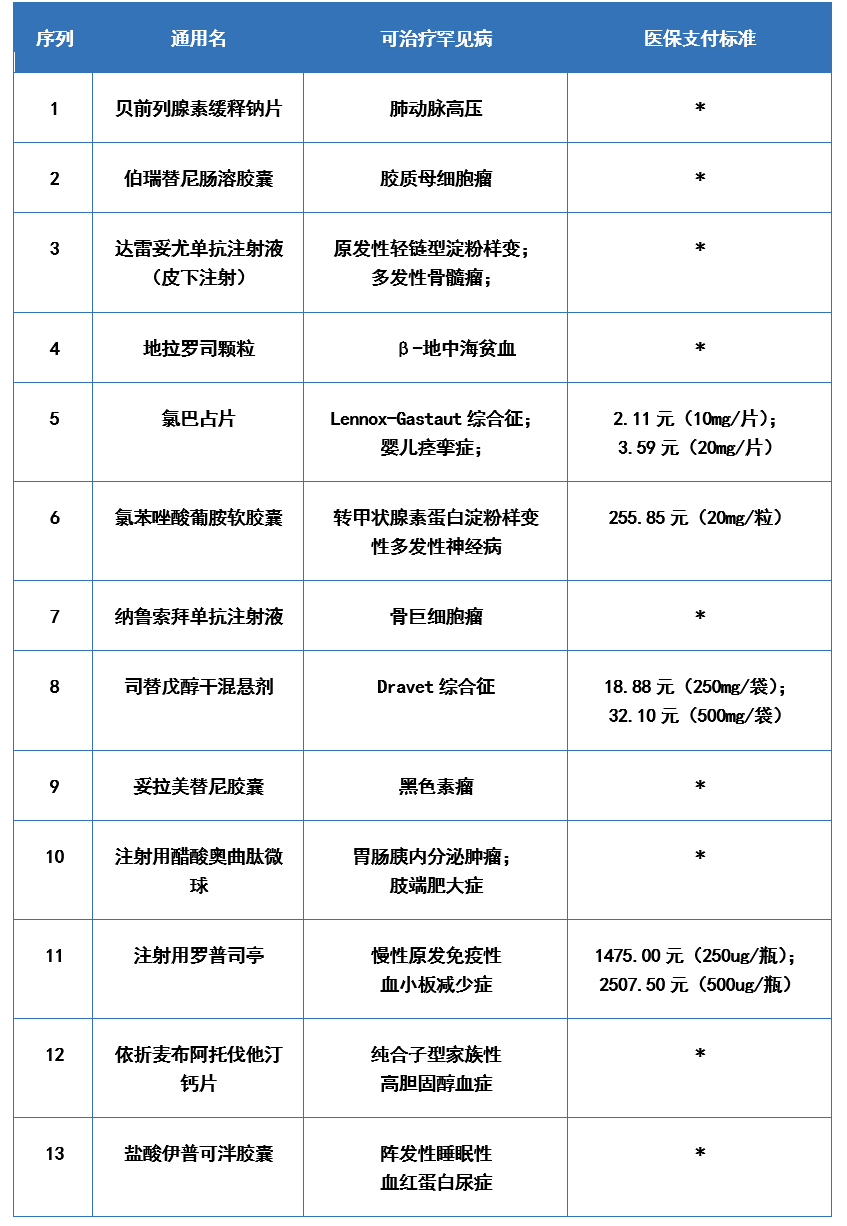
2024版国家医保目录新增罕见病药品部分清单
目录调整后,罕见病患者的用药负担将进一步降低。以往不少罕见病治疗药物动辄每年数十万元甚至上百万元的费用让患者家庭难以承受,而医保的覆盖不仅降低了药物价格,还通过基金支付分担了患者的费用压力,为罕见病患者及其家庭带来实实在在的经济支持。
自2018年起,我国医保药品目录已连续7年动态调整。医保部门秉持“以人民为中心”的理念,通过战略购买、价值评估等方式,累计将多种罕见病治疗药物纳入目录,解决了罕见病患者“有药用、用得起”的迫切需求。
这次调整中的13种罕见病药物的加入,标志着我国罕见病保障体系的进一步完善,也展现了中国式现代化进程中对民生福祉的高度关注。随着《2024年药品目录》的实施,越来越多罕见病患者将看到新的希望,也期待未来有更多创新药物进入医保,让每位患者的生命都能被温柔以待。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#罕见病药物# #国家医保局#
16