Hypertension:靶向内皮 ENO1-PI3K-Akt-mTOR 轴缓解缺氧性肺动脉高压
2023-04-25 刘少飞 MedSci原创 发表于德国
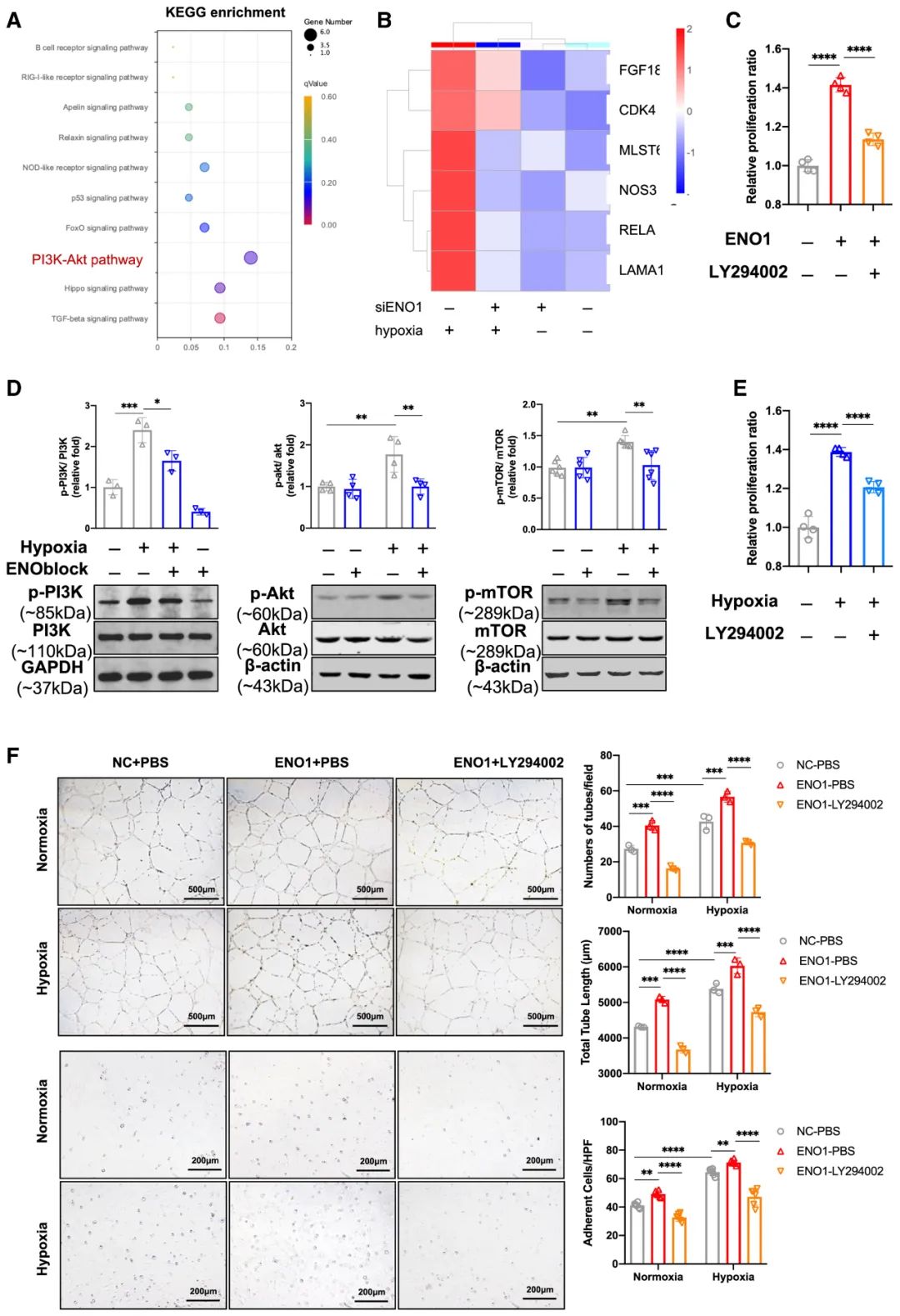
靶向内皮细胞ENO1-PI3K-Akt-mTOR信号通路可能是一种治疗缺氧性肺动脉高压的潜在策略。
肺动脉高压(PAH)是一种罕见但严重的心血管疾病,其发生率为10万分之一到30万分之一。它是一种由于肺动脉高压和肺血管阻力增加导致的肺循环疾病,最终导致右心室衰竭。缺氧性肺动脉高压(HPH)是肺动脉高压的主要类型之一,常见于肺部慢性阻塞性疾病、肺间质纤维化和高山病等缺氧性疾病。目前,缺氧性肺动脉高压的发病机制还不是完全清楚,因此寻找有效的治疗方法非常重要。 研究表明,内皮细胞在缺氧性肺动脉高压的发生和发展中起着关键作用。内皮细胞的生物学功能主要包括促进血管扩张、抗炎、抗凝等方面,而缺氧环境下,内皮细胞可以通过激活一系列的信号通路,如PI3K-Akt-mTOR信号通路,来增强细胞增殖、肺动脉平滑肌收缩等生物学过程,导致肺动脉高压的发生和发展。因此,寻找靶向内皮细胞信号通路的新的治疗方法可能是治疗缺氧性肺动脉高压的有效策略。 ENO1是一种蛋白质,全称为α-烯醇酸(Alpha-Enolase),在糖酵解过程中发挥重要的催化作用,参与糖的代谢,同时也被认为在细胞增殖、转移和凋亡等生物学过程中发挥了重要作用。此外,近年来的研究表明,ENO1在多种肿瘤中的表达也明显上调,并参与了肿瘤细胞的增殖、侵袭和转移等过程。糖酵解蛋白 ENO1(α-烯醇化酶)通过作用于平滑肌细胞参与肺动脉高压的发病机制;然而,ENO1 引起的内皮和线粒体功能障碍在第 3 组肺动脉高压中的作用仍未得到探索。 该研究的目的是研究α-烯醇酸(ENO1)在缺氧性肺动脉高压(HPH)中的作用机制及其治疗作用。该研究采用了原代人肺动脉内皮细胞和小鼠模型,通过蛋白质组学、免疫印迹、转染等方法,对ENO1进行了表达和功能分析,并评估了针对ENO1的特异性抑制剂在缓解HPH中的作用。 研究发现,ENO1在缺氧性肺动脉高压患者的肺组织中高表达,并且能够促进肺内皮细胞增殖和肺动脉的收缩。此外,研究还发现,PI3K-Akt-mTOR信号通路在ENO1调控下参与了缺氧性肺动脉高压的发生和发展。特异性抑制ENO1的药物可以显著降低缺氧性肺动脉高压的肺动脉压力和肺血管重构程度,同时还能减少炎症因子的释放。 研究结论显示,ENO1在缺氧性肺动脉高压的发病机制中起着重要作用,通过调节PI3K-Akt-mTOR信号通路促进内皮细胞增殖和肺动脉收缩。针对ENO1-PI3K-Akt-mTOR信号通路的特异性抑制剂可以减轻HPH的病理表现,包括降低肺动脉压力和肺血管重构程度。 针对内皮细胞中的α-烯醇酸(ENO1)通过PI3K-Akt-mTOR信号通路参与了缺氧性肺动脉高压(HPH)的发生和发展,针对这一信号通路的特异性抑制剂可以减轻HPH的病理表现,包括降低肺动脉压力和肺血管重构程度。因此,靶向内皮细胞ENO1-PI3K-Akt-mTOR信号通路可能是一种治疗缺氧性肺动脉高压的潜在策略。这一发现有望为缺氧性肺动脉高压患者提供更有效的治疗选择。 该研究表明,内皮细胞中的α-烯醇酸(ENO1)参与了缺氧性肺动脉高压(HPH)的发生和发展,并通过调节PI3K-Akt-mTOR信号通路促进内皮细胞增殖和肺动脉收缩。针对ENO1-PI3K-Akt-mTOR信号通路的特异性抑制剂可以减轻HPH的病理表现,包括降低肺动脉压力和肺血管重构程度。 这些发现提示,靶向内皮细胞ENO1-PI3K-Akt-mTOR信号通路可能是一种治疗缺氧性肺动脉高压的潜在策略。这种策略有望在临床上开发成为一种新的治疗方法,为缺氧性肺动脉高压患者提供更有效的治疗选择。但是,需要进一步的研究来验证这些结果,并且需要开发和测试更具选择性和有效性的ENO1抑制剂,以期实现临床应用。 Shi Y, Liu J, Zhang R, Zhang M, Cui H, Wang L, Cui Y, Wang W, Sun Y, Wang C. Targeting Endothelial ENO1 (Alpha-Enolase) -PI3K-Akt-mTOR Axis Alleviates Hypoxic Pulmonary Hypertension. Hypertension. 2023 May;80(5):1035-1047. doi: 10.1161/HYPERTENSIONAHA.122.19857. Epub 2023 Mar 8. PMID: 37075135.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言