Nat Aging:王建伟团队发现DNA损伤促进造血干细胞衰老的潜在新机理
2024-04-21 iNature iNature 发表于陕西省
该研究表明衰老诱导的MCPH1易位激活坏死性凋亡并损害造血干细胞功能。
DNA损伤促进造血干细胞(HSCs)的衰老,但其潜在的分子机制尚不完全清楚。
2024年4月17日,中国医学科学院血液病医院(中国医学科学院血液学研究所)王建伟团队(何汉卿博士为第一作者)在Nature Aging 在线发表题为“Aging-induced MCPH1 translocation activates necroptosis and impairs hematopoietic stem cell function”的研究论文,该研究表明衰老诱导的MCPH1易位激活坏死性凋亡并损害造血干细胞功能。

造血干细胞负责在人的一生中产生所有的造血细胞。随着造血干细胞年龄的增长,它们的功能受到损害,重建能力降低,分化倾向于髓系,这是髓系恶性肿瘤的一个危险因素。虽然DNA损伤积累在驱动HSC衰老中的作用已被广泛承认,但DNA损伤导致HSC退化的完整分子级联仍有待充分阐明。MCPH1,也被称为BRIT1 (BRCT- hTERT表达重复抑制剂),是被确定为原发性常染色体小头症驱动因子的初始基因。它的功能作用包括多种细胞功能,包括参与DNA损伤反应,染色体凝聚调节,细胞周期进程,中心体活性和代谢。
MCPH1在招募DNA损伤传感器和中介蛋白(如CHK1、53BP1、MDC1、NBS1、ATM和RPA)修复DNA双链断裂中起着至关重要的作用。在结构上,MCPH1包含三个BRCT (BRCA C端)结构域,其中N端BRCT决定MCPH1相关表型,C端BRCT调节自寡聚化,在电离辐射诱导的病灶形成中发挥重要作用。此外,MCPH1在DNA损伤时通过与SWI-SNF复合物的相互作用参与染色质重塑,并作为细胞周期检查点的关键调节因子,特别是在S内和G2/M阶段。

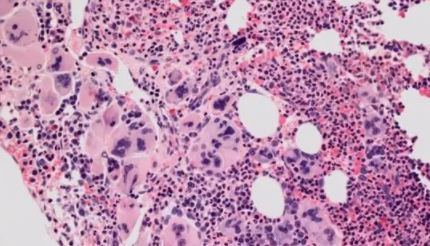
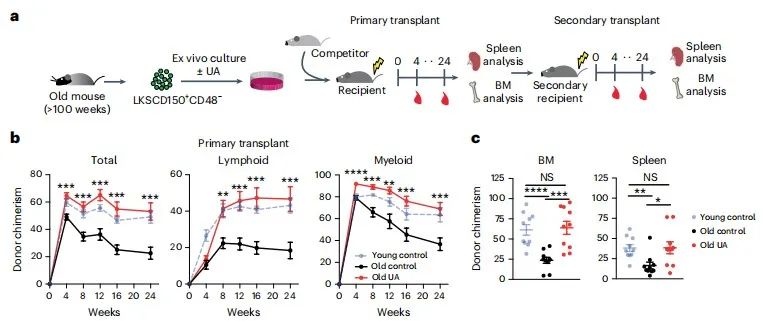
Mcph1功能障碍严重损害造血干细胞的重建能力(图源自Nature Aging )
该研究发现了microcephalin (MCPH1)在小鼠造血干细胞的细胞核和细胞质中的异质功能作用。在细胞核中,MCPH1维持基因组的稳定性,而在细胞质中,它通过与p-RIPK3结合来防止坏死性凋亡。衰老触发MCPH1从细胞质转移到细胞核,减少其细胞质保留,导致坏死性凋亡活化和HSC功能恶化。
在机制上,研究发现在MCPH1的NLS基序中,KAT7介导的赖氨酸乙酰化对DNA损伤的响应促进了其核易位。这些赖氨酸的靶向突变抑制MCPH1易位,从而导致坏死性凋亡。坏死性凋亡信号的功能障碍反过来又改善了衰老HSC的功能。总之,研究结果表明,DNA损伤诱导的MCPH1再分布促进了HSC衰老,并可能对衰老和衰老相关疾病具有更广泛的影响。
原文链接:
https://www.nature.com/articles/s43587-024-00609-z
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#造血干细胞# #DNA损伤#
38