观《黑神话:悟空》,看国产创新药困境
2024-08-21 网络 网络 发表于上海
8月20日上市,国产游戏《黑神话:悟空》正式上线发售,成为全球游戏玩家的焦点,这是中国首个真正意义上的国产3A游戏,许多玩家将其视作具有划时代意义的,开启国产3A游戏元年的一款游戏。
8月20日上市,国产游戏《黑神话:悟空》正式上线发售,成为全球游戏玩家的焦点,这是中国首个真正意义上的国产3A游戏,许多玩家将其视作具有划时代意义的,开启国产3A游戏元年的一款游戏。

自开放预售起,《黑神话:悟空》在游戏平台 Steam 上展现了极强的竞争力,销量突破120万套,预售已破4亿。根据Valve公布的 Steam 平台最新一周销量榜(2024年8月6日至13日),《黑神话:悟空》预购拿下当期全球第一名。
那么,这只风靡全球的猴子究竟是从哪儿蹦出来的呢?
这只“孙悟空”的制作人正是冯骥——游戏科学创始人兼CEO,毕业于华中科技大学生物医学工程专业,一个看似与游戏风马牛不相及的领域。
那么,大家反复提及的“3A游戏”又是什么?
首先,3A游戏并没有一个客观、公正、数据化的评判标准,也没有一个准确的定义,大多数玩家习惯将对电脑配置要求高的游戏统称3A游戏。
3A游戏的说法最早起源于美国,在游戏领域中的“3A”通常是指:大量的金钱(A lot of money),大量的资源(A lot of resources),大量的时间(A lot of time)。也有玩家认为3A游戏代表着高成本、高质量、高体量。
3A游戏与创新药“有趣类比”
这样以高投入、长周期为特点的项目,除了“3A游戏”,还有创新药。近日,有网友将做3A游戏与做创新药进行了对比。

同样的高成本、长周期,却收获截然不同的回报,引起了许多相关领域从业人员的关注,也让我们不禁反思,我们的国产创新药,究竟面临什么样的困境?
2015年是中国创新药元年,先是“7.22核查”,要求企业自查临床数据造假问题,随后,44号文提高审批门槛。中国加入ICH(国际人用药品注册技术协调会),接受境外临床数据,和国际接轨。一项项举措促进了中国创新药的蓬勃发展,八年间繁花似锦,大有追赶美国生物科技之势。
然而刚刚扬帆起航的国产创新药就遭遇了重重困难:
1、带量采购,压低价格。面对医保带量采购,药企要中标,就必然大降价,不中标,则生存都有问题。中国药品90%在医院和诊所销售,据统计2021-2023连续三年谈判成功的新药,平均降价60%以上。
60%的降幅对于一个真正的创新药来说,难以弥补研发端的巨大投入,也无法激励真正的创新。许多国内创新药企业迫于当前的经营水平和财务状况,不得不将公司或管线卖给大型跨国药企。
比如2016年,再鼎医药(09688.HK)拿到了Tesaro公司(后被葛兰素史克收购)抗癌药尼拉帕利(则乐)在中国内地、香港和澳门地区的合作开发与引进协议;2020年,基石药业将舒格利单抗(PD-L1)在中国大陆地区的独家商业化权利卖给了辉瑞;2021年年初,泛生子宣布与正大天晴合作,推广其肝癌早筛产品HCCScreen。
2、缺少源头创新。现阶段的中国创新药产业还摆脱不掉“拿来主义”,倾向于跟进大药企已验证过的成熟靶点,而鲜有人愿意建立一套针对未发现靶点的探索体系,其本质上是一种“急功近利”的表现。创新药,创新才是内核。
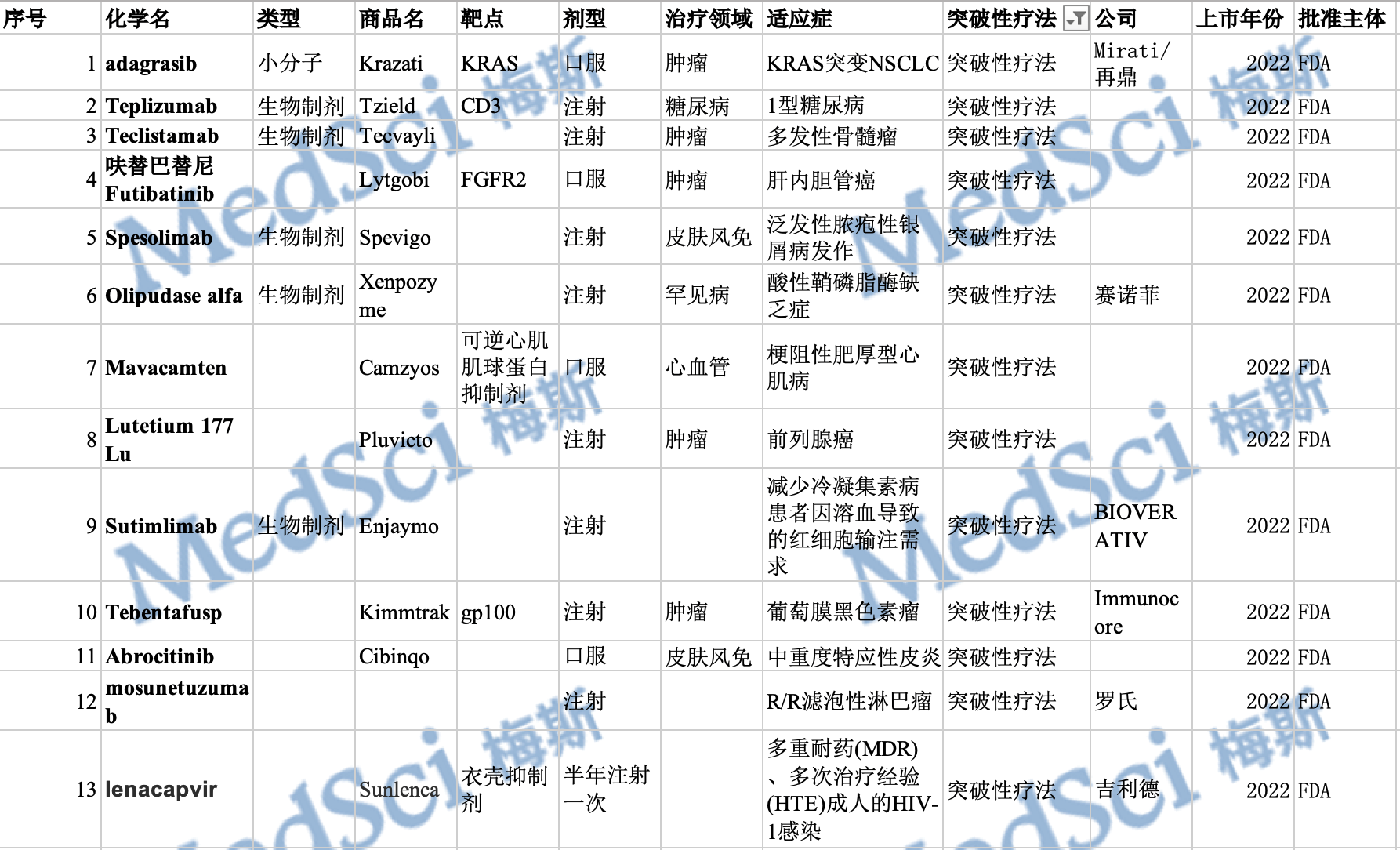
今年初,百济神州自主研发的替雷利珠单抗,继去年在欧盟和英国获批上市之后,又获得FDA批准,用于治疗既往接受化疗后晚期或转移性食管鳞状细胞癌患者。该公司另一创新药物泽布替尼(百悦泽),在2023年跻身“十亿美元分子”行列,其临床疗效在全球70个国家和地区得到认可。
百济神州总裁、首席运营官吴晓滨也曾在采访中表示,相比被“生产”出来的仿制药,创新药前期需要持续投入大量的研发成本,“如果只考虑生产成本,创新将永远得不到成长”。
国家政策向创新药倾斜,鼓励创新药的发展
2023年医保谈判首次提出临床价值评级,设立突破、改进、相当、不及四个档次;简易续约规则优化更新,允许创新药就价格降幅申请重新谈判;按照企业自愿原则对部分药品谈判价格保密,不主动公布药品实际价格。
2024年7月5日,国务院常务会议审议通过《全链条支持创新药发展实施方案》。会议指出,要全链条强化政策保障,统筹用好价格管理、医保支付、商业保险、药品配备使用、投融资等政策,优化审评审批和医疗机构考核机制,合力助推创新药突破发展。
这一系列政策的出台,有望通过合理化政策引导,支持创新药企业获得合理回报,拉动整个创新药行业的研发积极性,开发出真正具有竞争力的产品。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#创新药#
79
不错,学习了。
58