儿童肢体疼痛原因为何?需警惕急性白血病!
2022-10-09 王珏等 江苏省无锡市人民医院等 “检验医学”公众号
儿童急性白血病以急淋多见,临床常表现为血小板减少和/或贫血和/或中性粒细胞减少,白细胞计数不定,肝脾淋巴结肿大常见,骨关节痛可非常突出。
前 言
原始B淋巴细胞白血病/淋巴瘤(B-ALL/LBL)伴重现性遗传学是一组由重现遗传学异常引起的疾病,包括易位和(或)染色体数目的异常。这一组疾病具有不同的临床和表型特征,单独进行分类有着重要的预后意义,但需要通过遗传学及分子生物学的方法才能进行诊断;因为和伴重现性遗传学异常的急性髓系白血病(AML)不同,伴重现性遗传学异常的B-ALL缺乏独特的形态学特征。
今天就给大家介绍一个少见的B-ALL伴重现性遗传学异常病种。
案例经过
简要病史:患儿男,7岁5个月,因间断发热、膝盖疼痛2天,发现血常规三系异常1天入院。患儿2天前开始出现发热、跛行,体温最高38.2℃,给予阿奇霉素及蒲地蓝治疗,症状无明显好转,来到我院就诊。体格检查:体温38℃,脉搏118次/分,贫血貌,神志清,全身浅表淋巴结无肿大,肝脏未触及,脾肋下两指,右侧膝关节疼痛。
实验室检查:
血常规:WBC 18.03×10^9/L,Hb82g/L,PLT50×10^9/L。见图1:
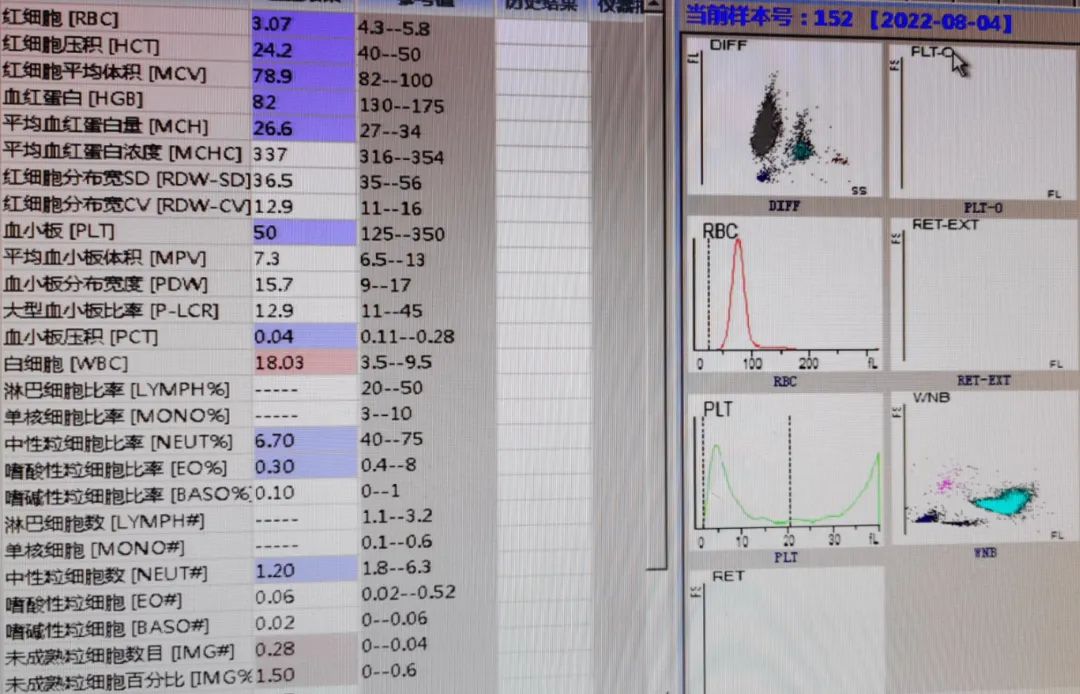
图1血常规报告
凝血:PT13.8s ↑,INR1.27 ↑,APTT34.5s ↑,FIB4.16g/L ↑。
生化免疫:CRP28.11 mg/L ↑,总蛋白62.6g/L ↓,白蛋白36.3g/L ↓, 乳酸脱氢酶2375U/L ↑,α-羟丁酸脱氢酶1471U/L ↑,铁蛋白1036ug/L ↑
查阅国家卫生行业标准WS/T779,7岁儿童的血细胞分析参考区间如下:
WBC (4.3-11.3) × 10^9/L,
Neut (1.6-7.8) × 10^9/L(31-70%),
Lym (1.5-4.6)× 10^9/L(23-59%),
Mon (0.13-0.76) × 10^9/L(2-11%),
Eos (0-0.68)× 10^9/L(0-9%),
Bas (0-0.07)× 10^9/L(0-1%),
RBC (4.2-5.7)× 10^12/L,
Hb 118-156g/L,
HCT 36-46%,
MCV 77-92fl,
MCH 25-34fl,
MCHC 310-355 g/L,
PLT (167-453)× 10^9/L。
该患儿白细胞增高,散点图异常,伴有贫血,血小板减少,临床有跛行表现,笔者心里有了不好的预感。虽然儿童肢体痛也可能是生长痛,外伤或者关节炎等,但患儿的血常规显着异常,会不会是急性淋巴细胞白血病?于是我们推片镜检,外周血片如下,可见原幼细胞,占白细胞的81%(图2-3):
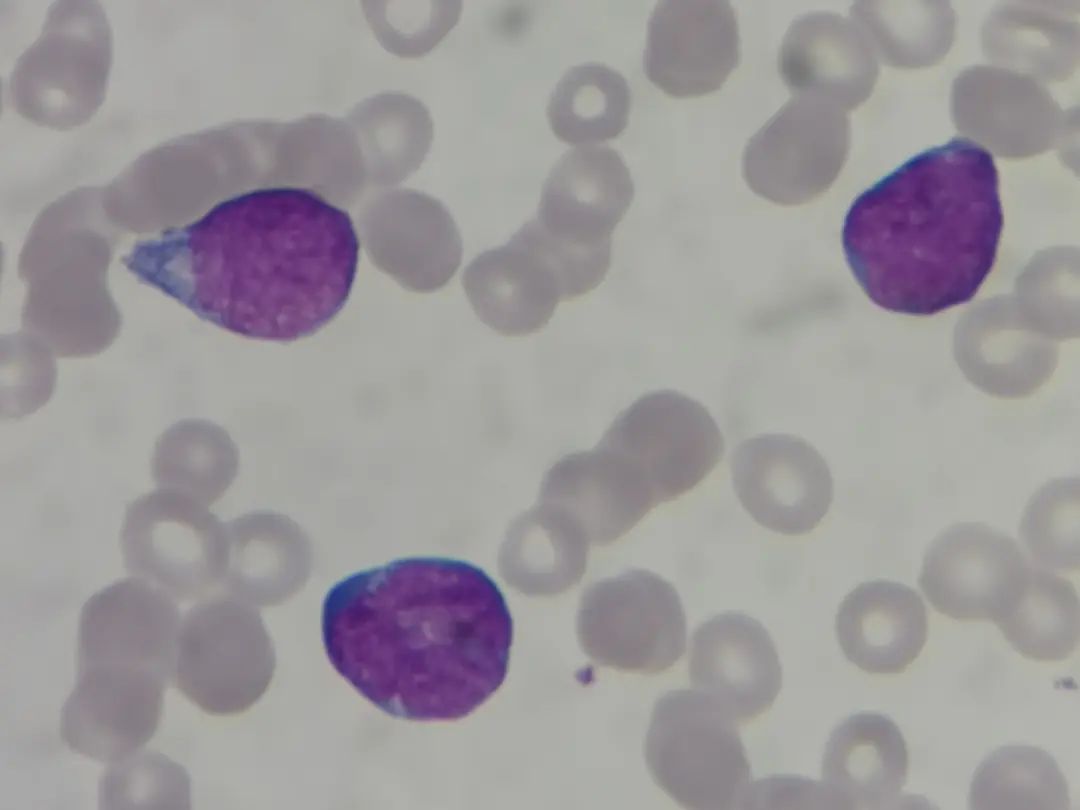
图2外周血片

图3 外周血片
笔者的预感成为了现实,赶紧联系临床说明情况,建议患儿完善骨髓检查。
骨髓细胞学检查:原幼淋巴细胞异常增生,胞体大小不一,胞浆少见,蓝色,核圆形,部分细胞可见切迹,核染色质粗粒状,部分细胞可见核仁,考虑急性淋巴细胞白血病。(图4-8)
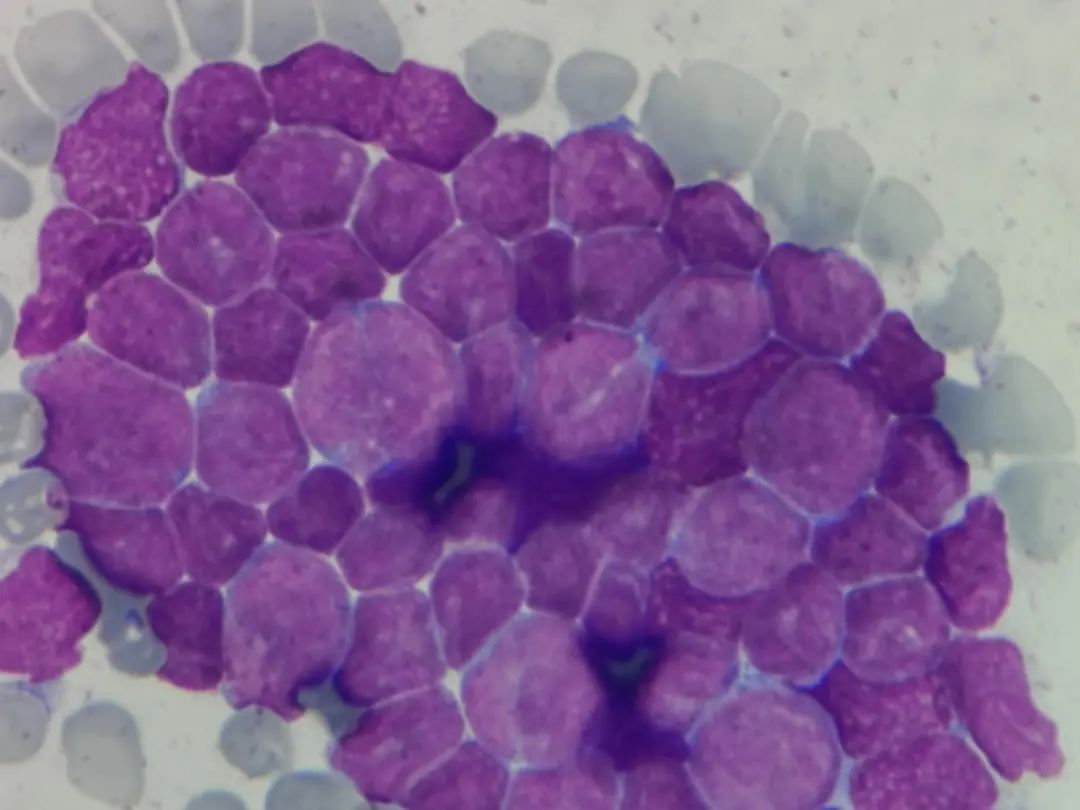
图4 骨髓涂片
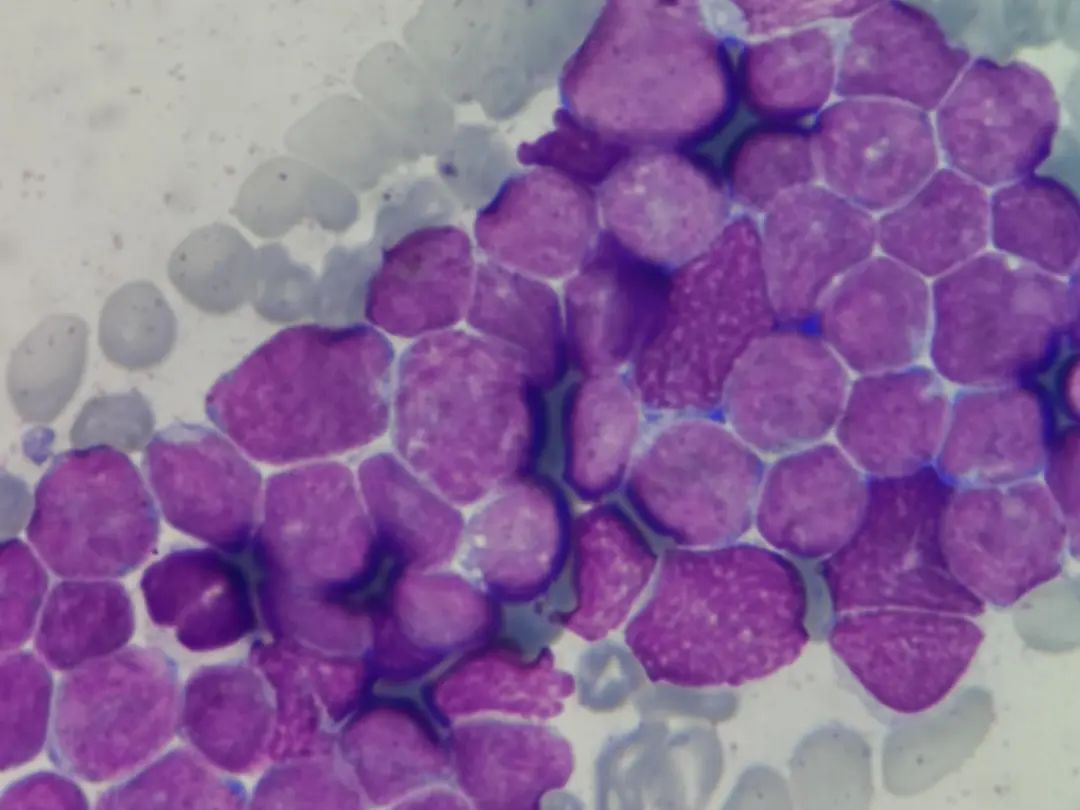
图5 骨髓涂片
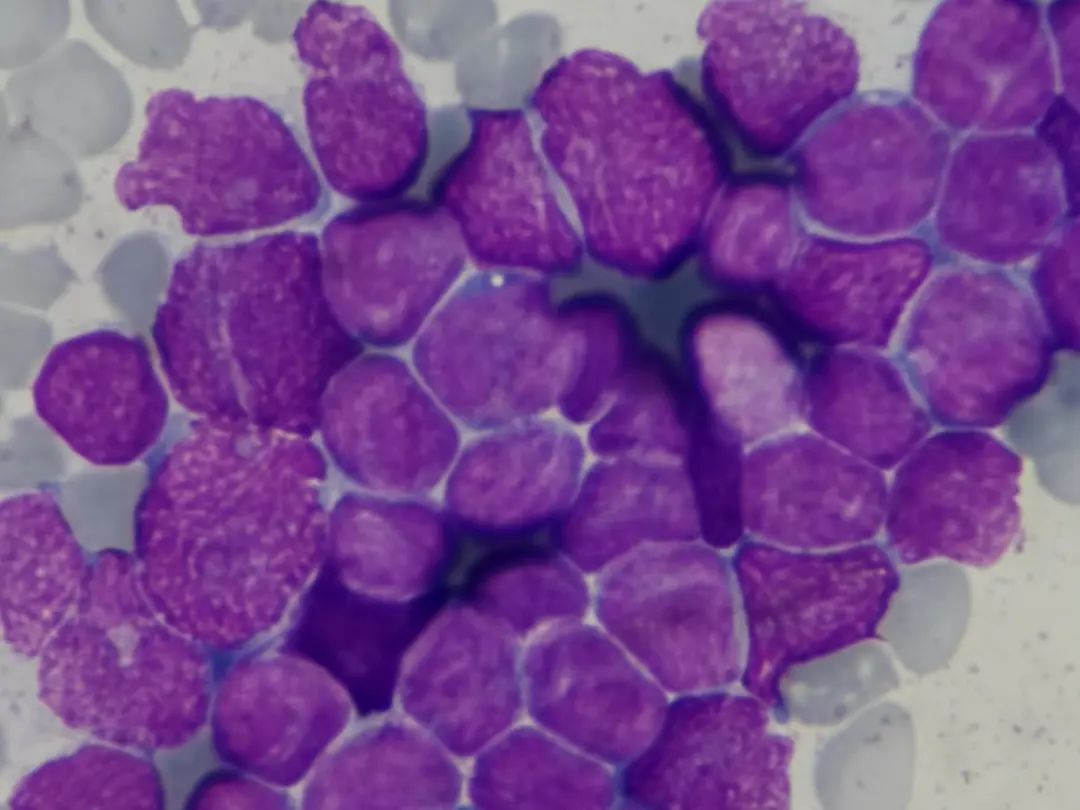
图6 骨髓涂片
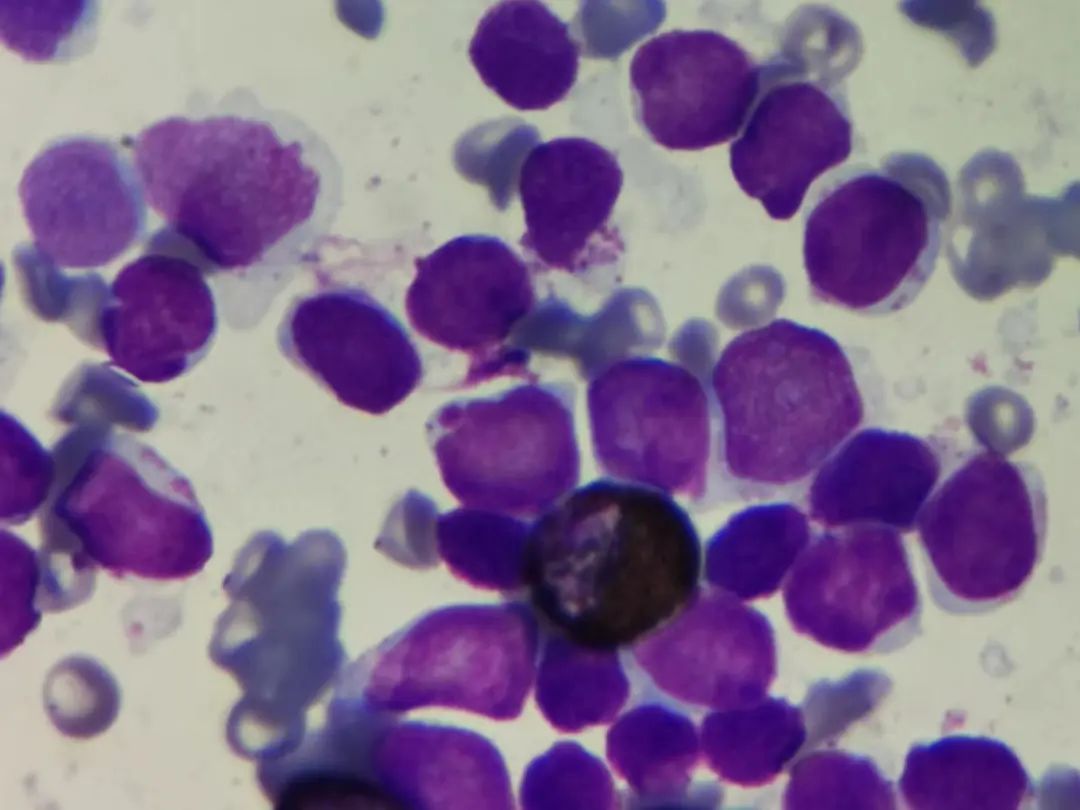
图7 POX染色×1000,原始细胞阴性
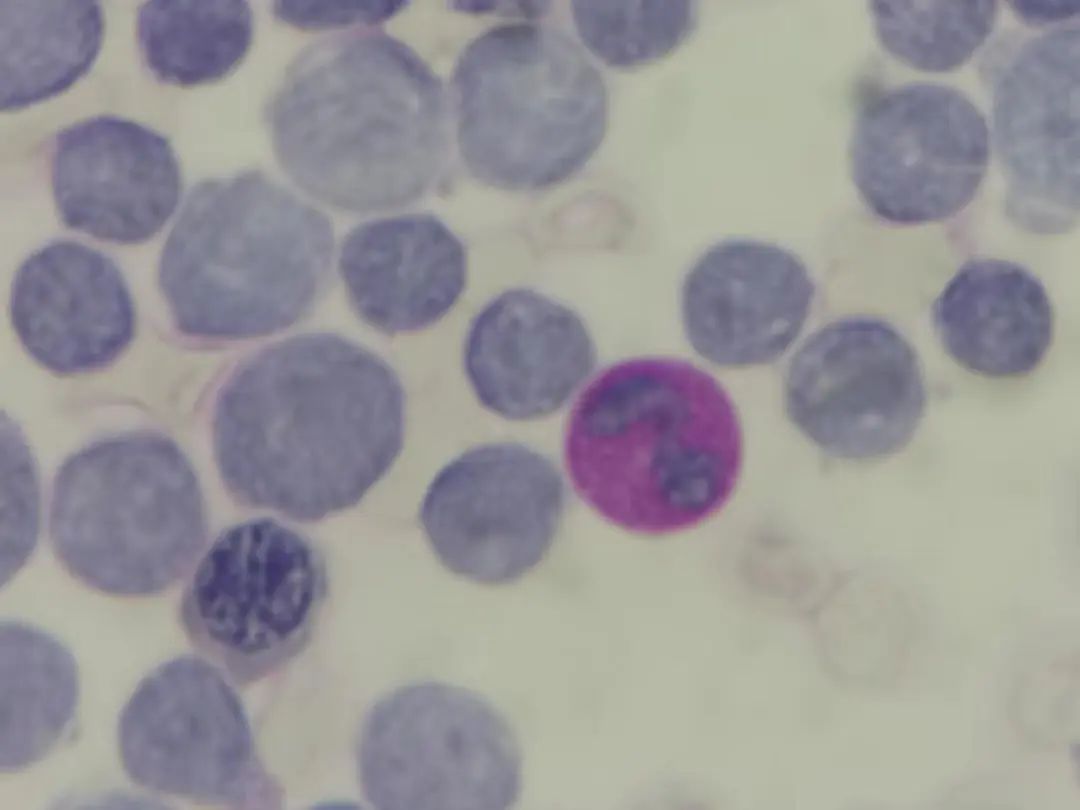
图8 PAS染色×1000,原始细胞阴性
免疫分型:原始细胞占有核细胞的93.40%,表达TdT、CD10和CD19,部分表达HLA-DR,符合急性B淋巴细胞白血病免疫表型
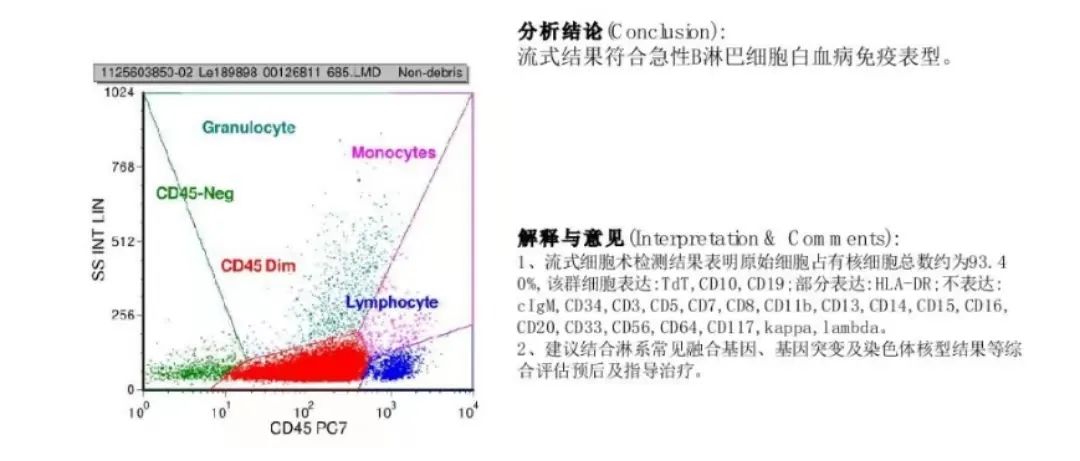
原始细胞是红色的细胞群
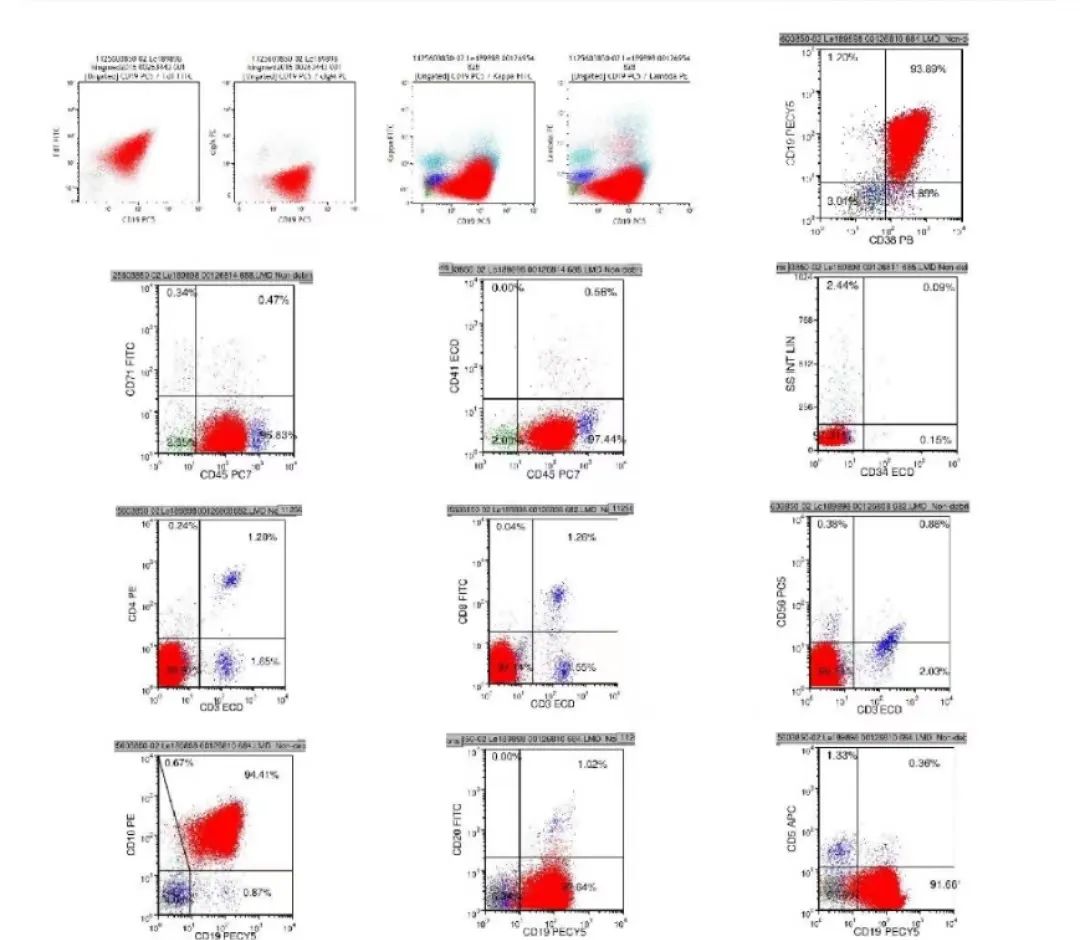
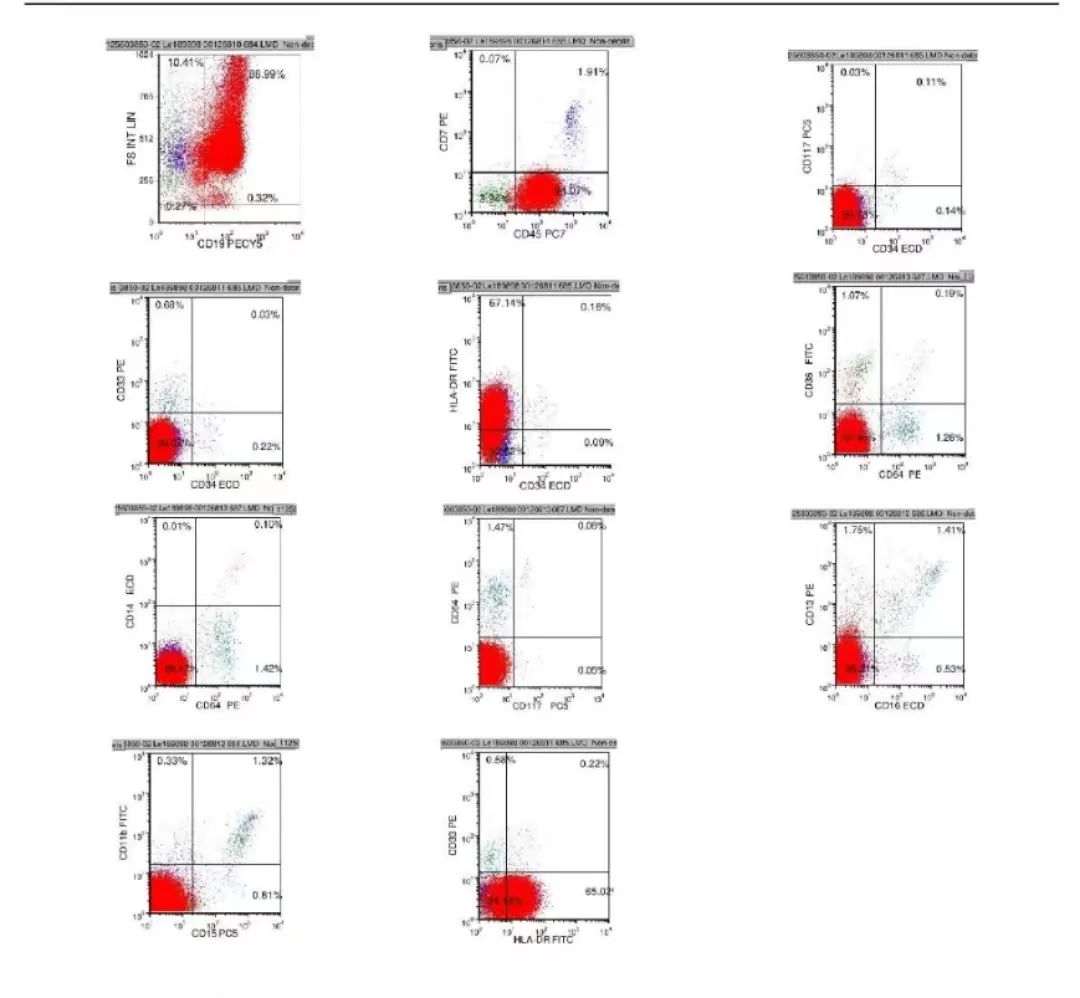
图9 免疫分型报告
染色体核型:分析中期细胞见der(19)t(1;19)(q23;p13)

图10 染色体报告
分子生物学检查:检出E2A::PBX1(TCF3::PBX1)融合基因。
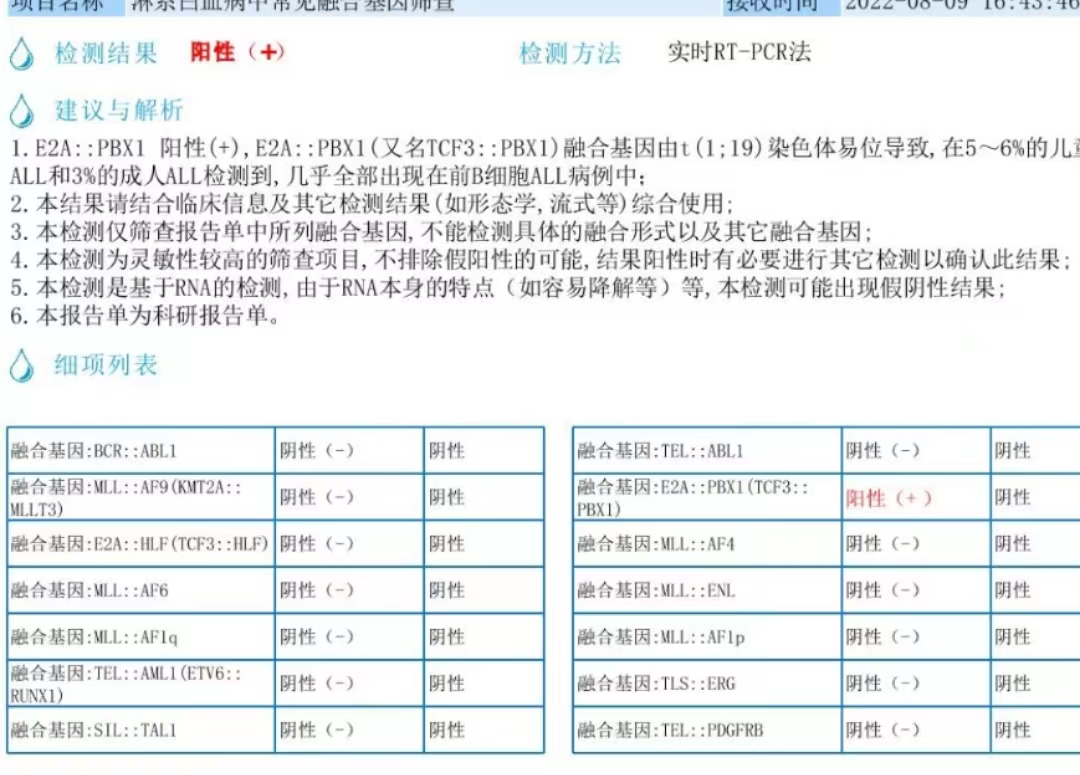
图11 融合基因报告
综合以上MICM检查,该患儿明确诊断为B-ALL伴t(1;19)(q23;p13);TCF3::PBX1,是WHO认定的一种伴重现性遗传学异常的B-ALL。
案例分析
在修订第4版(2017年版)WHO造血与淋巴组织肿瘤分类中,伴重现性遗传学异常的急性B淋巴细胞白血病有以下类型:
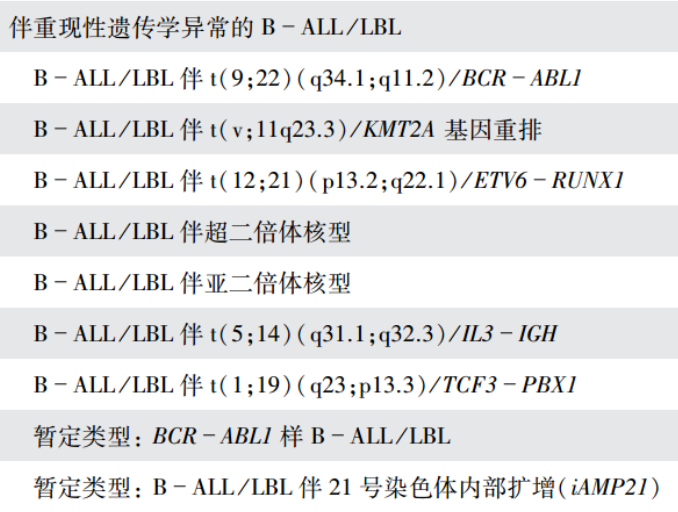
其中倒数第三个就是B-ALL伴t(1;19)(q23;p13.3);E2A-PBX1(TCF3-PBX1)
据说在第5版WHO造血与淋巴组织肿瘤分类中,伴重现性遗传学异常的急性B淋巴细胞白血病有以下类型:

倒数第四个就是B-ALL伴TCF3::PBX1(E2A::PBX1),这一版更强调融合基因的重要性,并且采用双冒号取代横线的写法。
原始B淋巴细胞白血病/淋巴瘤伴t(1;19)(q23;p13.3);E2A-PBX1(TCF3-PBX1)在儿童相对多见,约占儿童急性B淋巴细胞白血病的6%;在成人中相对少见,临床多表现为贫血,肝脾淋巴结肿大,骨关节痛明显,本例为7岁儿童,因发热,脾脏肿大,膝盖疼痛跛行入院。
该病没有特殊的形态学/细胞化学特征可与其他类型急性淋巴细胞白血病相区别。原始细胞有典型的CD19+,CD10+,胞质μ(Cμ)重链阳性的前B细胞表型,此类白血病有典型的CD9强表达和CD34低表达的特征,或者仅有少量的白血病细胞表达有限的CD34。
TCF3-PBX1易位导致一种融合蛋白的产生,这种融合蛋白作为转录激活物,具有致癌作用,且似乎可以干扰由TCF3和PBX1编码的转录因子的正常功能。功能性融合基因存在于19号染色体上,在一些病例中可能有衍生1号染色体的丢失,从而导致不平衡易位。基因表达谱研究显示,该病具有独特的特征。另据报道,甚至有BCR::ABL1与TCF3::PBX1共存的B-ALL病例;一般认为,这些病例的临床特征是由BCR::ABL1决定的。
在早期研究中,TCF3-PBX1与预后不良有关,但目前这一情况已经逐渐被现代的强化治疗克服。然而,这些患者可能有相对较高的中枢神经系统复发风险。笔者去查了NCCN的儿童ALL临床实践指南,TCF3-PBX1确实不在预后不良组中(图14):

favorable是有利的意思,unfavorable是不利的意思
心得体会
有不少儿童检验指标的参考区间与成人不同,而LIS系统往往显示的是成人参考区间,本例就是如此。如今国家卫健委已经出台了部分儿童检验指标的参考区间,我们应当参考之。
儿童急性白血病以急淋多见,临床常表现为血小板减少和/或贫血和/或中性粒细胞减少,白细胞计数不定,肝脾淋巴结肿大常见,骨关节痛可非常突出。对于有发热,治疗无效且跛行的患儿,应警惕有无恶性血液病的可能,若外周血原幼细胞可见,往往提示急性淋巴细胞白血病的可能,因此应注重外周血细胞形态观察。
参考文献
[1]毛飞,许文荣.临床血液检验学[M].北京:科学出版社,2020.2
[2]KennethKaushansky,MarshallA. Lichtman,JosefT. Prchal,etal.Williams Hematology. Ninth Edition. USA:McGraw-HillEducation,2016
[3]SwerdlowSH, Campo E, Harris NL, et al. (Eds) : WHO Classification of TumoursofHaematopoietic and Lymphoid Tissues. Revised 4th edition.Lyon,France: IARC Press, 2017.
[4]卢兴国,叶向军,徐根波.骨髓细胞与组织病理诊断学[M].北京:人民卫生出版社,2020
[5]王建祥,肖志坚,沈志祥等.邓家栋临床血液学[M].第2版.上海:上海科学技术出版社,2020.12
[6]高海燕,刘亚波,吕成芳,陈雪艳.血液病临床检验诊断[M].北京:中国医药科技出版社,2021.3
[7]AlaggioRita,Amador Catalina,Anagnostopoulos Ioannis et al. The 5th editionof the World Health Organization Classification of HaematolymphoidTumours: Lymphoid Neoplasms.[J] .Leukemia, 2022, 36: 1720-1748.
[8]NCCNClinical Practice Guidelines in Oncology (NCCN Guidelines). PediatricAcute Lymphoblastic Leukemia. Version 1. 2022
[9]儿童血细胞分析参考区间(发布稿):WS/T779-2021[S]. 2021.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言