全球获批上市的15款ADC大盘点,中国有6款获批
2023-03-02 找药宝典 找药宝典 发表于上海
抗体偶联药物(ADC),顾名思义是由抗体与细胞毒药物偶联制成的药物。因此ADC包括三个重要组成部分:抗体(Antibody)、连接子(Linker)和毒素(Drug/Toxin/Payload),然后
近些年来,对于肿瘤的治疗手段逐渐由放化疗的“无差别杀伤”扩展成靶向药物、免疫治疗的“精确制导”。而早在上个世纪初由诺贝尔生理学医学奖获得者,化疗之父提出的设想,即通过某种载体将毒素精确射向肿瘤细胞的“魔法子弹”(Magic Bullet),随着抗体技术与化学连接的发展,也在这个世纪以ADC的方式付诸于实现。ADC强大的疗效与截然相反的低毒副作用也成为了这个时代抗癌领域新的研究热点。
什么是ADC
抗体偶联药物(ADC),顾名思义是由抗体与细胞毒药物偶联制成的药物。因此ADC包括三个重要组成部分:抗体(Antibody)、连接子(Linker)和毒素(Drug/Toxin/Payload),然后通过偶联技术将三者进行组合。
►抗体
抗体是子弹的制导系统,抗体的选择是一款ADC设计的起点。肿瘤靶点是ADC识别肿瘤细胞的媒介,目前ADC靶点的选择主要集中在已被验证的肿瘤靶点,包括HER2、EGFR、CD-19等。而ADC的抗体一般需满足以下几个条件:与靶点具有较高亲和力;较长的半衰期;最小化的免疫原性。抗体与肿瘤细胞的结合一方面可以为毒素的释放精确制导,另一方面抗体的结合本身可以抑制抗原受体下游信号传导,达到抗体本身拥有的抑癌作用。
►连接子
连接子是抗体与毒素连接的桥梁,既需要保证ADC找到肿瘤前毒素的稳定连接以防止伤害正常细胞,又要保证找到肿瘤后迅速释放毒素杀伤肿瘤细胞。目前连接子主要分为两大类,可裂解型连接子和非裂解型连接子。前者利用肿瘤微环境特异性自动裂解释放透膜的毒素以杀伤周围肿瘤细胞,即旁观者效应(bystander effect);后者通过抗体与肿瘤细胞的特异性结合,让毒素在肿瘤细胞中被释放。两者各有优势,分别在ADC中有着不同的应用。
►毒素
毒素是子弹主要发挥杀伤力的部分。目前使用的毒素主要是已上市的化疗药物,根据杀伤机制可分为微管抑制剂和DNA损伤剂。此外,一些新型的小分子药物也被用于ADC的研发,如RNAII型聚合酶抑制剂、Toll样受体激动剂、BCL-xL抑制剂等。最终目的以杀伤靶细胞导致肿瘤细胞死亡。
因此ADC通过抗体的靶向作用结合毒素的杀伤作用,ADC不仅能够提高靶向药物的治疗窗口与疗效,还能够降低细胞毒药物的非靶向毒副作用,同时具备了特异性与高效性,减少不良反应的发生。
全球上市的ADC
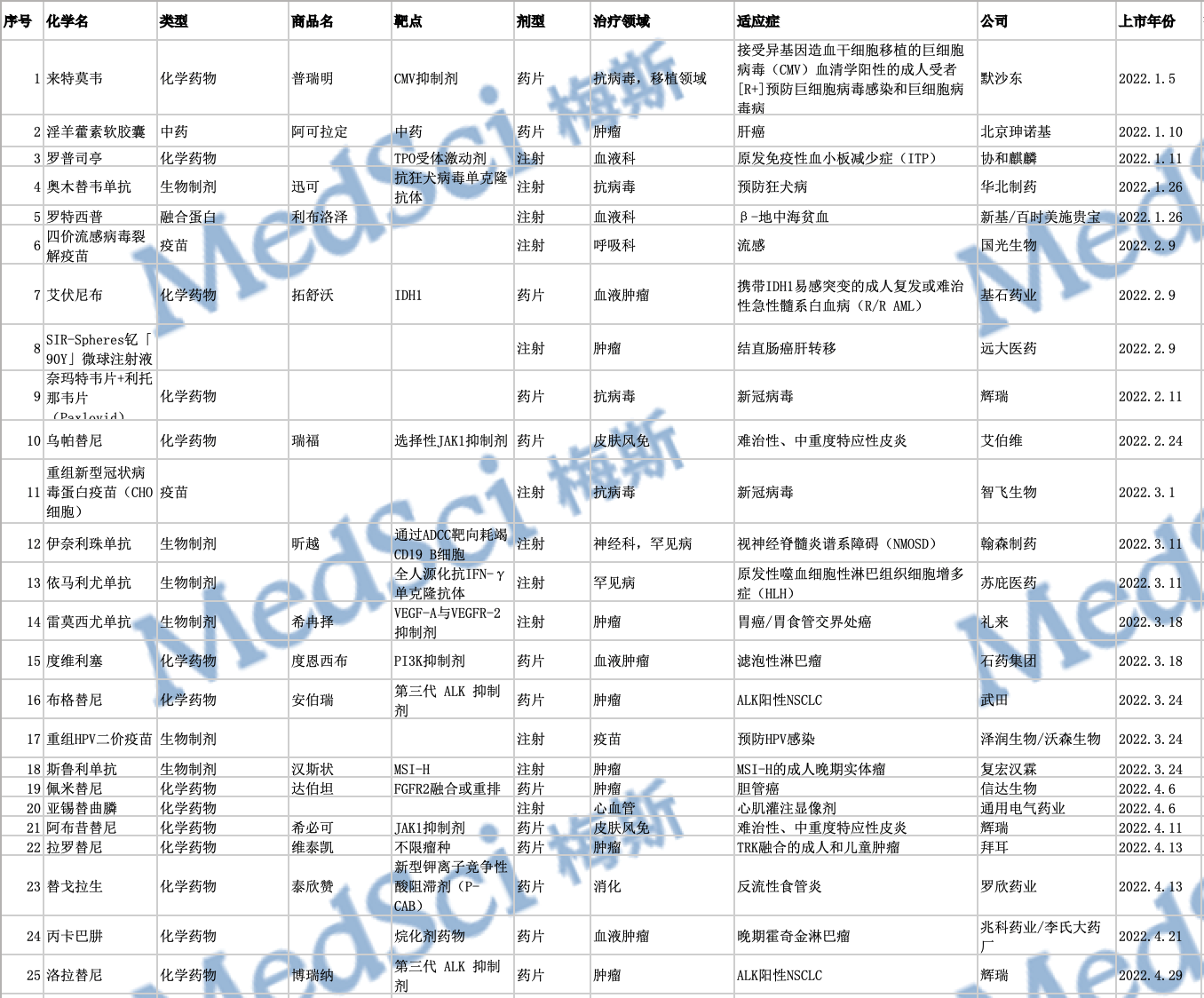
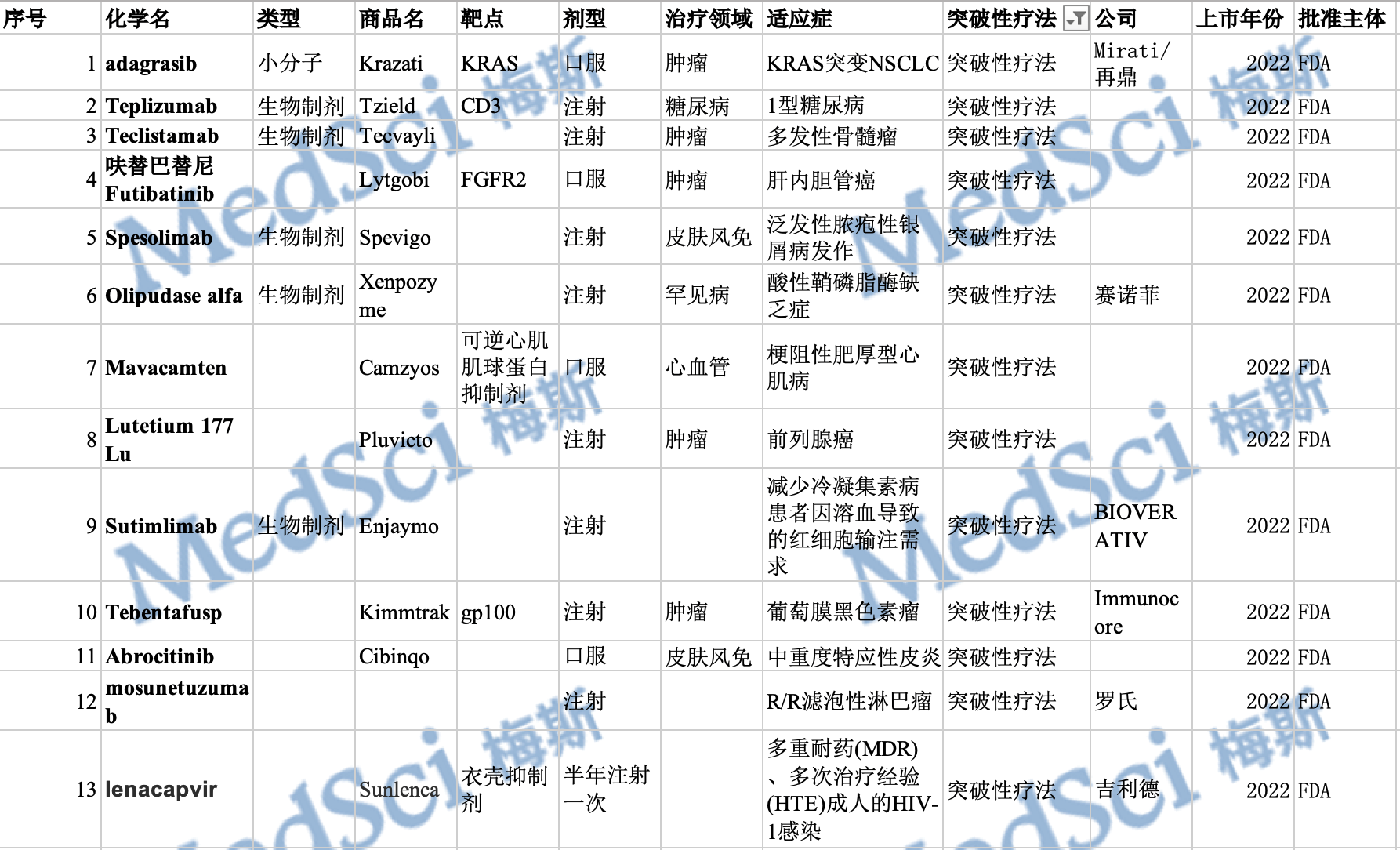
ADC药物凭借其良好的发展前景,各国药企都在加速ADC的研发。截至目前,全球已有15款ADC药物陆续上市。
1► Mylotarg(Gemtuzumab Ozogamicin)
Mylotarg由辉瑞研发,是全球第一款上市的ADC。为了满足当时大量的急性粒细胞白血病(AML)患者的需求,Mylotarg仅凭借3个II期临床试验结果就被FDA于2000年5月17日被加速批准上市。然而作为第一个匆忙上市的ADC,后续的大型III期临床试验却发现了该药可能增加患者的死亡率,存在巨大的隐患。遂于2010年6月辉瑞宣布Mylotarg自主撤市。然而故事并没有结束,在之后长达7年的时间里,各国研究者并没有放弃Mylotarg。后续一系列的临床试验结果发现,在降低药物剂量的同时,明确了该药只有在CD33蛋白高表达的AML才有效。最终在2017年,Mylotarg通过将原来9mg/m2调整至3mg/m2,这款历经17年波折的ADC再次获得FDA审批上市。
Mylotarg的结构是通过可清除腙键作为可裂解型连接子将DNA裂解剂卡奇霉素与抗CD33 IgG4抗体偶联。该药被用于治疗新确诊的成人CD33阳性AML,也可用于2岁及以上复发或初始治疗无反应的CD33阳性AML患者,是首个可用于儿童患者的药物。
更多:JCO:Gemtuzumab Ozogamicin可改善KMT2A重排型AML患儿预后、减少复发!
2►Adcetris(brentuximab vedotin)
Adcetris由武田制药和Seattle Genetics联合开发,于2011年被FDA批准上市。其构成结构是由靶向CD30的嵌合抗体IgG1与微管蛋白抑制剂MMAE通过一种蛋白酶敏感连接子Vat-Cit偶联在一起。该药物主要适用于经典霍奇金淋巴瘤(HL)与间变性大细胞淋巴瘤(sALCL),在我国于2020年被NMPA批准用于治疗复发或难治性sALCL和CD30阳性HL患者,是第二款国内获批上市的ADC。
更多:NEJM:Brentuximab Vedotin治疗儿童和青少年高危霍奇金淋巴瘤,3年无事件生存率高达92%
3►Kadcyla(Adptrastuzumab emtansine)
Kadcyla由罗氏和ImmunoGen共同研发,于2013年2月22日被FDA批准用于HER2阳性转移性乳腺癌。Kadcyla由微管抑制剂DM1通过不可清除的硫醚键连接子与靶向HER2的人源化IgG1偶联,经过受体介导的内化被溶酶体溶解,使DM1降解产物在肿瘤细胞内释放致使细胞凋亡。2020年NMPA批准上市,成为国内第一款上市的ADC。
4►Besponsa(Inotuzumab Ozogamicin)
Besponsa由辉瑞研发,用于治疗急性淋巴细胞白血病(ALL)。由于ALL是一种侵袭性高预后差的白血病,其作为孤儿药于2017年被FDA优先审批上市,同时目前也被我国批准上市。该药通过可清除的腙键将卡奇霉素与抗CD22 IgG4抗体偶联。其适用于成人复发或难治性前体B细胞ALL,为既往难以治疗的复发或难治性B细胞ALL提供了新的治疗方式。
更多:Blood:Inotuzumab ozogamicin用于复发/难治性小儿急性淋巴细胞白血病的疗效
5►Lumoxiti(Moxetumomab pasudotox)
Lumoxiti由阿斯利康研发,于2018年9月由FDA批准用于治疗复发或难治性毛细管白血病(HCL)的成年患者。HCL是一种罕见的淋巴细胞增殖性慢性白血病,进展缓慢但无法治愈。Lumoxiti由可切割的二肽连接子mc-VC-PABC偶联假单胞菌外毒素A的抗CD22免疫毒素。该药作为首个获批治疗HCL的药物标志着该疾病领域的重大进展。
更多:Blood:Moxetumomab pasudotox,抗CD22抗体,可有效根除毛细胞白血病的微小残留病灶
6►Polivy(Polatuzumab Vedotin)
Polivy由罗氏研发,是靶向CD76β的MMAE偶联药物,抗体为特意靶向B细胞表面的CD76β靶点,连接子为Vat-Cit。于2019年6月被FDA加速批准上市,用于治疗接受过2此前期治疗的复发性或难治性弥漫性大B细胞淋巴瘤。临床试验证明联合苯达莫司汀+利妥昔单抗拥有良好的治疗效果。
更多:NEJM:采用Polatuzumab Vedotin治疗初治弥漫性大B细胞淋巴瘤
7►Padcev(Enfortumab Vedotin)
Padcev由Seagen与武田制药研发,于2019被FDA批准用于治疗晚期或转移性尿路上皮癌。该药物通过Vat-Cit将MMAE连接在靶向细胞表面蛋白Nectin-4的抗体上。Nectin-4在尿路上皮癌、乳腺癌、胃癌等多种肿瘤组织中高度表达,通过介导上皮间质转化,降低细胞的黏附作用,增强肿瘤的侵袭性。该药物对于晚期或转移性尿路上皮癌效果明显且不良反应可控。
更多:Clin Cancer Res:在尿路上皮癌转移过程中NECTIN-4表达水平的降低与Enfortumab vedotin耐药相关
8►Enhertu(Trastuzumab Deruxtecan)
Enhertu由阿斯利康和日本第一三共联合开发的靶向HER2的抗体偶联药物,2019年被FDA批准用于HER2阳性乳腺癌的后线治疗,该药物由人源化抗HER2单克隆抗体通过稳定的可裂解四肽连接子与拓扑异构酶-I抑制剂(喜树碱类衍生物Dxd)连接组成。该药物在HER阳性、晚期胃或胃食管交界癌患者中,客观反应率明显高于常规化疗,总生存期较常规化疗更长。于2021年扩展用于经曲妥珠单抗治疗的HER2阳性局部晚期或转移性胃癌和胃食管结合部(GEJ)腺癌患者;2022年5月,扩展新适应症HER2阳性乳腺癌晚期二线;2022年8月5日,获批HER2低表达乳腺癌晚期后线,第一次改写乳腺癌的HER2二分类标准;2022年8月12日,获批新适应症:既往接受过全身治疗的HER2突变不可切除或转移性非小细胞肺癌(NSCLC),成为第一个获FDA批准的用于肺癌的HER2靶向疗法。
更多:NEJM:Trastuzumab deruxtecan vs Trastuzumab emtansine治疗HER2阳性转移性乳腺癌
9►Trodelvy(Sacituzumab Govitecan)
Trodelvy由吉利德研发,于2020年被FDA批准用于治疗至少2种药物治疗无效的转移性或晚期三阴性乳腺癌。三阴乳腺癌指对雌激素受体、孕激素受体、HER2受体均呈阴性反应的乳腺癌,约占所有乳腺癌中的20%,其对于激素治疗与HER2靶向药物均无应答。该药物抗体靶向肿瘤相关钙信号转导2 (TROP-2)受体,其通过水解连接子(pH 敏感连接子)CL2A 与拓扑异构酶 I 抑制剂SN-38偶联。
更多:J Clin Oncol:Sacituzumab govitecan治疗内分泌耐药的HR+/HER2– 晚期乳腺癌
10►Blenrep(Belantamab Mafodotin)
Blenrep由葛兰素史克研发,于2020年被FDA批准用于治疗既往接受过至少4种疗法的复发性或难治性多发性骨髓瘤(MM)成年患者。该药物是靶向B细胞成熟抗原的单克隆抗体于微管破坏剂单甲基auristatin-F(MMAF)偶联,通过破坏微管聚合使肿瘤细胞凋亡。
更多:靶向BCMA的ADC药物belantamab mafodotin,获得FDA咨询小组支持治疗复发或难治的多发性骨髓瘤患者
11►Akalux(Cetuximab Sarotalocan Sodium)
Akalux由乐天医药研发,于2021年9月获得日本厚生劳动省批准上市,用于治疗治疗不可切除的局部晚期或复发性头颈癌。该药物靶向表皮生长因子受体(EGFR),该受体在头颈癌、肺癌、食道癌、胰腺癌等多种实体瘤表面表达。其毒素为IRDye700DX,是一种光反应物质,可以通过光照射激活其药理反应。在药物和癌细胞结合后,通过与BioBlade激光系统医疗器械向患者照射近红外激光,激活药物中的抗体从而达到破坏癌细胞的目的,该疗法称为光免疫疗法。
12►Zynlonta(loncastuximab Tesirine)
Zynlonta由ADCTherapeutics研发,于2021年被FDA批准用于接受过2种或多种系统疗法的成人复发或难治性大B细胞淋巴瘤患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、起源于低级别淋巴瘤和高级别B细胞淋巴瘤的DLBCL。DLBCL是美国最常见的非霍奇金淋巴瘤类型,其侵袭性强、进展迅速。超过40%的一线DLBCL治疗失败,预后差。该药物是靶向CD19的ADC,该靶点是治疗B细胞恶性肿瘤的热门靶点。通过可裂解的缬氨酸-丙氨酸共价连接子偶联全人源IgG和DNA裂解剂SG3199。
更多:SOHO 2022:Loncastuximab Tesirine在复发/难治性DLBCL患者中表现出有前景的抗肿瘤活性
Lancet oncol:Loncastuximab tesirine可有效治疗复发性/难治性DLBCL!
13►爱地希(维迪西妥单抗)
爱地希是荣昌生物自主研发的ADC,同时是我国首个原创ADC,于2021年6月9日NMPA宣布上市。该药物由靶向HER2的抗体通过Mc-VC-PAB连接子和MMAE组合而成。与同类型的Kadcyla相比,该药物的抗体为拥有自主知识产权的高HER2亲和力新型人源化抗体,连接子具有胞内酶解特性,因此该药物具有更强的亲和力,更好的安全性与更强的肿瘤细胞清除能力。
更多:ASCO 2021:荣昌生物ADC新药维迪西妥单抗再次亮相大会,展示重磅临床数据!
14►Tivdak(Tisotumab Vedotin-tftv)
Tivdak是Seagen与Genmab联合研发,于2021年9月20日由FDA加速批准上市,用于治疗用于治疗复发或转移性宫颈癌患者。通过蛋白酶可切割连接子偶联MMAE与靶向组织因子(TF)的完全人源化IgG。
更多:再鼎引进的宫颈癌ADC类新药Tisotumab Vedotin
15►Elahere(mirvetuximab soravtansine)
2022年11月4日,美国FDA已批准了ImmunoGen公司靶向叶酸受体α(FRα)的前沿抗体偶联药物米维妥昔单抗索拉坦辛(Elahere)上市,用于治疗曾接受过1到3种全身治疗方案,且叶酸受体α(FRα)阳性、铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌的成人患者。
更多:首款FRα-ADC药物突出重围,获FDA加速批准治疗难治性卵巢癌
ImmunoGen的抗体 - 药物偶联物Mirvetuximab soravtansine未达到III期卵巢癌研究的主要终点
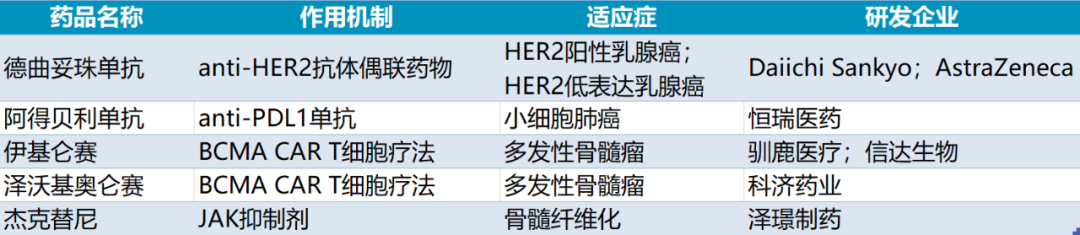
其中,中国获批上市的ADC药物有6个,分别是T-DM1、维布妥昔单抗、奥加伊妥珠单抗、维迪西妥单抗、戈沙妥珠单抗、DS-8201。
更多:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言