European Radiology:深度学习图像重建算法在低剂量肝脏CT中的应用
2024-06-06 shaosai MedSci原创 发表于上海
计算能力的稳步提升使得基于神经网络模型的深度学习图像重建(DLIR) 算法得以实现,并且能够从输入数据中学习。DLIR利用了人工智能的能力,克服了IR的局限性,同时进一步提高了图像质量。
现阶段,计算机断层扫描 (CT)是腹部肿瘤疾病诊断、分期和监测治疗反应评估的参考标准。肿瘤患者需要进行严格的随访,包括多次CT检查,因此必须尽量减少辐射剂量和累积有效剂量。
滤波反投影 (FBP)由于其在标准辐射剂量水平下的良好性能,已经成为传统图像重建算法的代表。然而,随着辐射暴露意识的提高以及计算能力的飞速发展,FBP使用已无法满足临床的需要。计算能力的稳步提升使得基于神经网络模型的深度学习图像重建(DLIR) 算法得以实现,并且能够从输入数据中学习。DLIR利用了人工智能的能力,克服了IR的局限性,同时进一步提高了图像质量。初步研究证明,DLIR算法能有效地提高图像质量,而不产生低辐射剂量。

近日,发表在European Radiology杂志的一项研究对DLIR重建的腹部CT检查进行了全面的受试者内图像质量分析,并评估了与常规应用的自适应统计迭代重建(ASiR-V)算法相比的诊断准确性。
本项研究前瞻性纳入了肿瘤患者并多所有患者进行了CT增强扫描。DLIR以高、中、低三个重建强度水平重建图像,ASiR-V以10 ~ 100%的强度水平重建图像,间隔为10%。三名放射科医生对病变进行了特征描述,两名读者评估了诊断的准确性,并计算了信噪比(SNR)、对比噪声比(CNR)、优点值(FOM)和主观图像质量,后者采用5分李克特量表。
50例患者(平均年龄70±10岁,男性23例)共发现130例肝脏病变(良性105例,转移性25例)。DLIR_H达到最高的信噪比和CNR,与ASiR-V相比为100% (p≥0.051)。DLIR_M返回的主观图像质量最高(得分:5;差:4 - 5;p≤0.001),FOM的中位升高(29%)显著(p < 0.001)。仅在≤0.5 cm的病变中发现差异:DLIR_M检测到32/33个病变,ASiR-V 50%检测到26个病变(p = 0.031)。病变正确率为93.8% (95% CI: 88.1, 97.3;130个病变中的122个)为DLIR, 87.7% (95% CI: 80.8, 92.8;130个病变中的114个)为50%的ASiR-V。
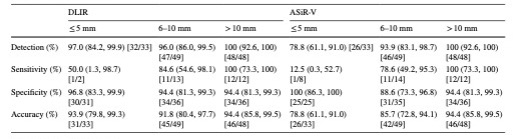
表 诊断准确性
本项研究表明,与ASiR-V相比,DLIR在评估低血管性肝脏病变方面具有更好的图像质量和更高的诊断准确性,特别是对于≤0.5 cm的病变来说更为显著。
原文出处:
Damiano Caruso,Domenico De Santis,Antonella Del Gaudio,et al.Low-dose liver CT: image quality and diagnostic accuracy of deep learning image reconstruction algorithm.DOI:10.1007/s00330-023-10171-8
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#深度学习# #肝脏CT#
0