European Radiology:基于深度学习的MRI下咽癌全自动分割和放射组学特征提取
2024-03-21 shaosai MedSci原创 发表于上海
多项研究显示,磁共振放射组学可以作为一个生物标志物预测HNSCC的治疗预效果和生存率。然而,以一层接一层的方式手工勾画肿瘤轮廓非常耗时,而且容易出现间隙。
众所周知,下咽癌 (HPC) 在所有头颈部鳞状细胞癌 (HNSCC)中预后最差。近几十年来,HPC的发病率和死广率持续上升。大多数HPC患者在发病时已经为晚期,目前化疗被认为是晚期患者的主要治疗手段。以往的研究表明,磁共振成像 (MRI) 可提供解剖学定性,在临床实践中对HNSCC分期、治疗计划和疗效评估提供了的定量功能信息。
确定肿瘤轮廓是制定放疗计划的必要条件。MRI已广泛应用于肿瘤分割的预处理。多项研究显示,磁共振放射组学可以作为一个生物标志物预测HNSCC的治疗预效果和生存率。然而,以一层接一层的方式手工勾画肿瘤轮廓非常耗时,而且容易出现间隙。因此,肿瘤自动分割工具有望提高放疗工作流程的效率。
近几年来,CNNs被广泛用于医学图像的语义分割。然而,其在HNSCC中的应用多为计算机断层成像CT或PET/CT上进行,对于MR的研究较少。

近日,发表在European Radiology杂志上的一篇研究使用卷积神经网络对MRI中的下咽癌(HPC)肿瘤进行全自动分割和放射组学特征提取,并与U-Net进行了比较。
本项研究收集了222名HPC患者的MR图像,其中178名患者用于训练,另外44名患者用于测试。使用U-Net和DeepLab V3+架构来训练模型,并使用骰子相似度系数(DSC)、Jaccard指数和平均表面距离来评估模型性能。同时,使用类内相关系数(ICC)评估了模型提取的肿瘤放射组学参数的可靠性。
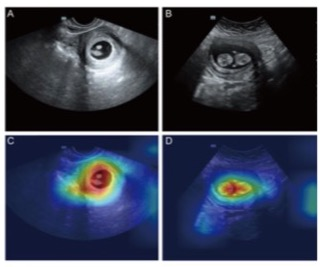
DeepLab V3+模型和U-Net模型预测的肿瘤体积与人工划定的肿瘤体积高度相关(P < 0.001)。DeepLab V3+模型的DSC明显高于U-Net模型(0.77 vs 0.75,p < 0.05),尤其是那些小于10 cm3的小体积肿瘤(0.74 vs 0.70,p < 0.001)。对于一阶特征的放射组学提取,两个模型都表现出与人工分割的高度一致(ICC:0.71-0.91)。在19个一阶特征中的7个和17个基于形状的特征中的8个,DeepLab V3 +模型提取的放射组学的ICC明显高于U-Net模型提取的放射组学(P < 0.05)。
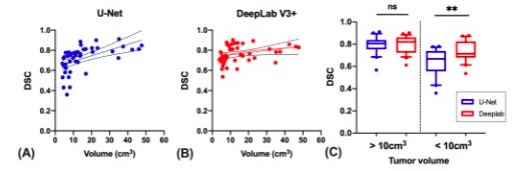
图 A,B预测肿瘤体积与DeepLab V3+模型和U-Net模型的散点图;C小肿和大肿瘤模型的DSC比较
本项研究表明,DeepLab V3 +和U-Net模型在MR图像上对HPC的自动分割和放射学特征提取方面都产生了合理的结果,而DeepLab V3 +的性能优于U-Net。这种方法在加强放疗工作流程和促进治疗结果的预测方面具有很大的潜力。
原文出处:
Yu-Chun Lin,Gigin Lin,Sumit Pandey,et al.Fully automated segmentation and radiomics feature extraction of hypopharyngeal cancer on MRI using deep learning.DOI:10.1007/s00330-023-09827-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#深度学习# #下咽癌#
70