Science Translational Medicine:基因编辑+基因工程干细胞疗法,增强脑转移肿瘤免疫治疗
2023-06-06 王聪 “生物世界”公众号 发表于上海
尽管近年来治疗方法有所改进,但晚期黑色素瘤患者的生存预后仍然有限。晚期黑色素瘤患者中约有60%会发生脑转移。虽然放疗、靶向治疗、手术等多学科治疗手段已被用于治疗黑色素瘤脑转移。
尽管近年来治疗方法有所改进,但晚期黑色素瘤患者的生存预后仍然有限。晚期黑色素瘤患者中约有60%会发生脑转移。虽然放疗、靶向治疗、手术等多学科治疗手段已被用于治疗黑色素瘤脑转移,但其总生存期仅为4-6个月。
免疫疗法彻底改变了癌症治疗格局,免疫检查点抑制剂(ICI)是近年来癌症治疗的主要突破,特别是用于治疗转移性黑色素瘤。然而,全身注射给药的免疫检查点抑制剂(ICI)临床研究显示,由于ICI单抗进入大脑和脑脊液的渗透效率有限,其在大脑内肿瘤的效果较差。因此,迫切需要开发替代治疗药物和策略。
近日,哈佛医学院的研究人员在 Science 子刊 Science Translational Medicine 上发表了题为:Gene-edited and -engineered stem cell platform drives immunotherapy for brain metastatic melanomas 的研究论文。
该研究开发了一种基因编辑+基因工程的双干细胞平台,通过局部给药,向脑转移的黑色素瘤释放溶瘤病毒和免疫调节剂,增强治疗效果。

论文通讯作者、哈佛医学院教授 Khalid Shah 表示,在出现脑转移的晚期癌症患者中,静脉和口服的全身给药不能有效地靶向脑转移,而这项研究开发出了一种新的免疫治疗方法,该方法是可持续的,并且可以局部送达肿瘤。我们相信,局部免疫疗法代表了治疗脑转移癌症的未来。
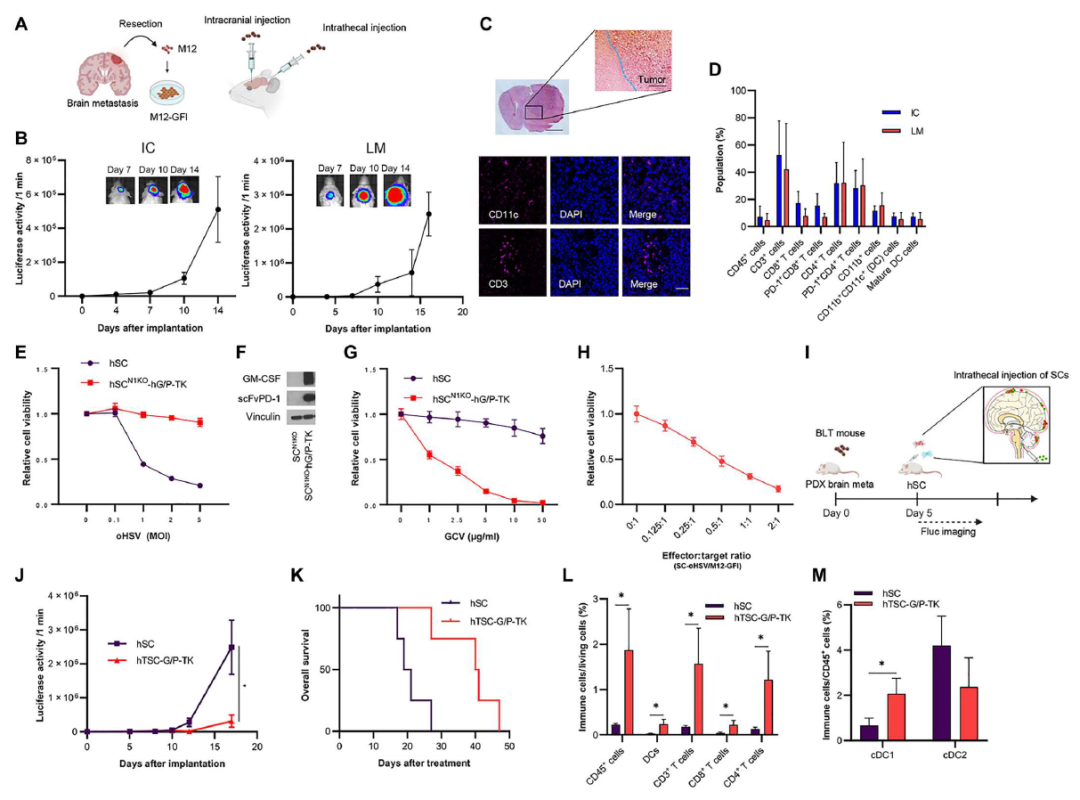
研究团队设计了一种使用工程化“双干细胞”的方法来最大限度地攻击已经扩散到大脑中的癌细胞。一种干细胞释放溶瘤性单纯疱疹病毒(oHSV),这种方式此前已经显示出减少肿瘤生长的希望。使用干细胞来递送溶瘤病毒可以增加病毒的释放量,并确保溶瘤病毒在释放到癌细胞上之前不会被循环系统中的抗体所降解。但溶瘤病毒也会破坏释放它的细胞,导致这种治疗策略难以持续。因此,研究团队使用CRISPR-Cas9基因编辑技术在第二种干细胞中敲除了Nectin 1受体,敲除后的干细胞不能被溶瘤病毒靶向,并让其释放免疫调节剂,例如粒细胞-巨噬细胞集落刺激因子(GM-CSF),增强免疫系统,帮助对抗癌症。
双干细胞可以通过鞘内注射进行局部给药,这种给药方式已被用于治疗其他疾病。与近年来出现的其他免疫疗法不同,该疗法不需要反复给药。研究团队强调,这种治疗方法还可以用于其他脑转移癌症,如肺癌和乳腺癌,研究团队正在为这些癌症设计类似的治疗方法。
值得一提的是,研究团队还设计出了一种临床前小鼠模型——PTEN基因缺陷的BRAF-V600E基因突变黑色素瘤脑转移小鼠模型,能够忠实地代表患有脑转移黑色素瘤的人类患者,进而使用这种模型来测试工程化双干细胞疗法。他们发现,该疗法成功地激活了树突状细胞和T细胞介导的免疫反应。与现有的溶瘤病毒治疗方法相比,这种双干细胞疗法显示出更强的治疗效果。
这些研究结果提供了一种有希望的基于干细胞的免疫治疗策略,可用于治疗转移到中枢神经系统中的肿瘤,研究团队表示,希望在不久的将来启动1期临床试验。
Khalid Shah 教授表示,许多看起来很有希望的生物疗法往往在1期或2期临床试验中失败,部分原因是临床前模型没有真实地复制临床环境。而这项新研究让我们意识到,在过去的20年里,从来没有像现在这样接近治愈脑转移癌症。
原始出处:
NOBUHIKO KANAYA, et al. Gene-edited and -engineered stem cell platform drives immunotherapy for brain metastatic melanomas. SCIENCE TRANSLATIONAL MEDICINE, 31 May 2023, Vol 15, Issue 698.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言