Nat Rev Cardiol:2024年最新肺动脉高压治疗方案汇总及其局限性
2024-08-12 刘少飞 MedSci原创 发表于上海
PAH的复杂血管病理生物学特征,包括肺血管细胞过度增殖、细胞外基质沉积和血管周围炎性细胞浸润,对既定治疗提出了挑战。

肺动脉高压(PAH)的目前治疗方案
靶向PAH的治疗
对于在急性血管扩张剂挑战中未显示即时血流动力学改善或对大剂量钙通道阻滞剂治疗无持续反应的PAH患者,建议使用针对前列环素、内皮素或一氧化氮途径的靶向治疗方案。以下是美国或欧洲批准的靶向PAH治疗的关键试验的主要结果总结。
前列环素类似物
前列环素类似物依前列醇(epoprostenol)在一项针对PAH患者(NYHA III-IV级)的随机、对照、开放标签的12周研究中进行评估。结果显示,静脉注射依前列醇相比传统治疗提高了运动能力(6分钟步行距离,6MWD)和血流动力学指标。值得注意的是,该研究是迄今为止唯一一项显示新药相比标准疗法能够提高生存率的PAH试验。然而,该研究中的传统背景治疗(包括抗凝剂、口服血管扩张剂、利尿剂、强心苷和补充氧气)不同于后续研究(后者可能包括其他已确立的PAH治疗作为背景治疗),且患者均患有晚期疾病。随后批准的前列环素类似物设计上具有更好的安全性和更便捷的给药途径。评估皮下曲前列尼尔、吸入伊洛前列素、吸入曲前列尼尔和口服曲前列尼尔的关键试验显示,与安慰剂相比,12周内6MWD的改善。对于皮下曲前列尼尔不耐受的情况下,可考虑使用静脉注射的曲前列尼尔。此外,口服前列环素受体激动剂司来帕格(selexipag)与安慰剂相比,减少了死亡和PAH并发症的综合发生率,且与背景治疗无关。
内皮素受体拮抗剂
同样,评估口服内皮素受体拮抗剂(ERAs)波生坦(bosentan)和安倍生坦(ambrisentan)的关键试验显示,在未接受治疗的PAH患者中,与安慰剂相比,分别在16周和12周内6MWD得到改善。随后对正在接受最多两种PAH特定背景治疗的PAH患者进行的马昔腾坦(macitentan)试验显示,与安慰剂相比,该药物减少了发病率和死亡率的综合发生率。
靶向一氧化氮途径
一氧化氮通过刺激可溶性鸟苷酸环化酶(sGC)生成环磷酸鸟苷(cGMP),后者被磷酸二酯酶5(PDE5)降解。在未治疗的PAH患者中,口服PDE5抑制剂西地那非和他达拉非分别在12周和16周治疗后,与安慰剂相比,改善了6MWD。同样,在接受ERAs或前列腺素类药物治疗或未接受其他PAH特定治疗的PAH症状患者中,sGC刺激剂利奥西呱(riociguat)与安慰剂相比,在12周内改善了6MWD。
初始联合治疗
AMBITION III-IV期试验比较了新诊断PAH患者(WHO功能II和III级)中初始安倍生坦或他达拉非单药治疗与初始安倍生坦加他达拉非联合治疗的疗效。结果显示,与单药治疗相比,初始联合治疗显著降低了临床失败综合终点的风险。该研究首次使用了‘临床失败时间’事件驱动的综合终点的扩展定义,其中‘功能等级无变化’与步行距离恶化一起被视为治疗失败。然而,两组间综合终点发生率的差异主要由PAH住院率推动。
法国登记研究中,接受ERA和PDE5抑制剂双重联合治疗的新诊断PAH患者在4个月后WHO功能等级、运动能力和血流动力学指标均有所改善。此外,两项临床试验的结果表明,接受ERA和PDE5抑制剂双重口服联合治疗且未达到预定临床疗效标准的患者,可能受益于从PDE5抑制剂转换为利奥西呱。然而,由于这两项试验均为开放标签研究,仍需进行双盲和对照研究以确认这些发现。最终,TRITON研究显示,在新诊断、未治疗的PAH患者中,三联联合治疗(马昔腾坦、他达拉非和司来帕格)与双联联合治疗(马昔腾坦和他达拉非)在PVR主要终点上无显著差异。最新的欧洲肺动脉高压治疗指南推荐,对于没有心肺合并症的PAH患者(特发性、遗传性、药物相关或结缔组织病相关),采用初始联合治疗,而对于有心肺合并症的患者,采用初始口服单药治疗。
重要的是,PAH药物只有在患者能够耐受剂量、给药途径和不良反应特征的情况下才有效。药物的治疗潜力可能会影响患者应对不良反应的能力或意愿。例如,对于具有挽救生命潜力和疾病修饰特性的药物,不良反应特征较差的药物更容易被接受,而对于疗效较低的药物则不然。值得注意的是,同一类药物中的不同药物可能具有不同的副作用。在比较多种ERA的临床安全性的荟萃分析中,波生坦治疗的异常肝功能风险增加,而安倍生坦或马昔腾坦治疗则未见此风险。关于前列环素疗法,随着皮下、口服和吸入剂型的开发,静脉治疗的并发症和负担将减轻。然而,联合治疗会导致各个单独药物的不良反应积累,可能影响耐受性。
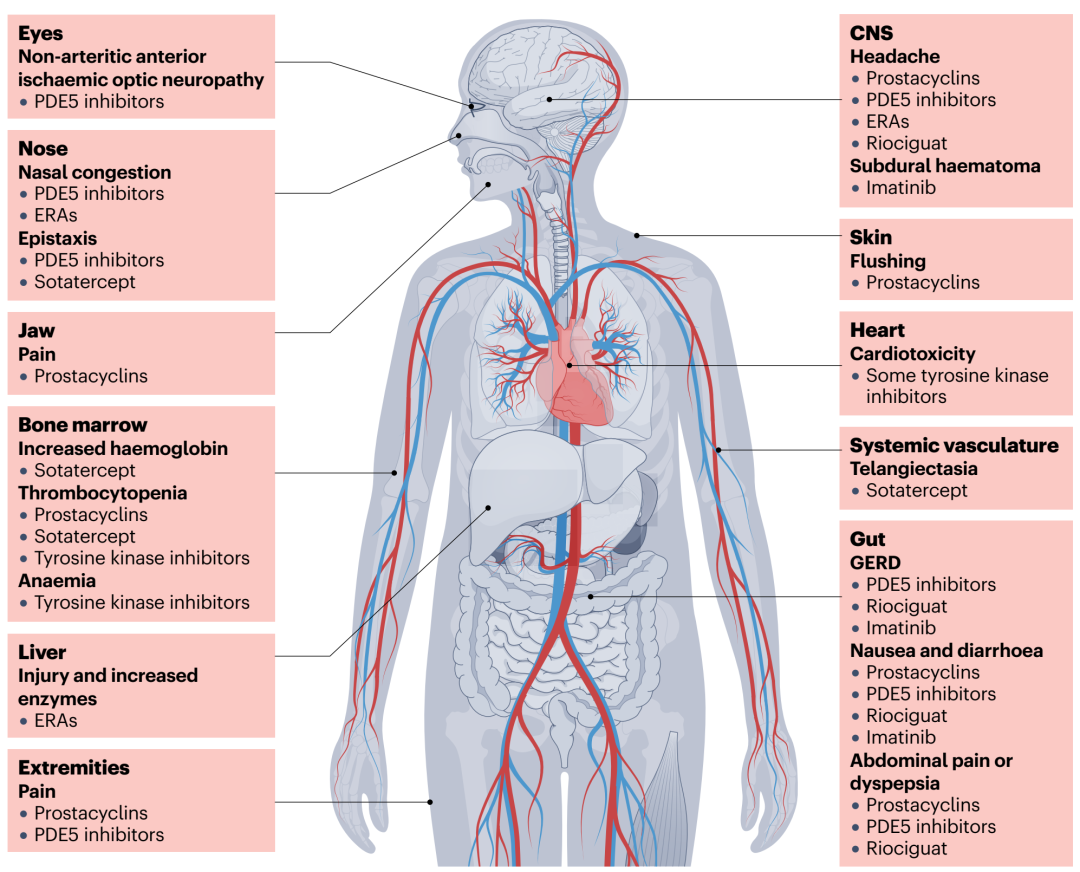
图 2:已批准和正在进行研究的肺动脉高压疗法的主要不良反应概述。联合治疗将导致每种药物的不良反应累积。CNS,中枢神经系统;ERAs,内皮素受体拮抗剂;GERD,胃食管反流病;PDE5,磷酸二酯酶5。
钙通道阻滞剂
对于特发性、遗传性或药物相关的PAH患者,若急性血管反应性试验结果为阳性,可能会从高剂量钙通道阻滞剂治疗中获益。不幸的是,这些患者在长期治疗中的初期效果往往无法持续。在一项法国国家注册研究中,12.6%的特发性PAH患者对急性血管扩张剂有急性血流动力学反应,但只有6.8%的患者在1年内对钙通道阻滞剂治疗有持续反应。在一项对1904名接受血管反应性测试的特发性、遗传性或药物诱发的PAH患者进行的多中心回顾性分析中,只有162名患者符合血管反应者标准。在中位随访60个月期间,总体生存率为86.7%。然而,在开始钙通道阻滞剂治疗后1年,只有53.2%的患者继续接受这种单药治疗。有趣的是,除了之前定义的血流动力学反应者标准外,这项研究还显示,初次血管反应性测试期间的肺动脉顺应性、低风险状态和随访期间的低血清NT-proBNP水平与生存率相关。因此,对急性血管扩张剂挑战反应积极的患者在接受钙通道阻滞剂治疗时应定期进行客观测试的重新评估。值得注意的是,在所有PAH治疗中,钙通道阻滞剂治疗仍然是唯一可以预先识别可能反应者的“个性化医学”工具。
目前治疗的局限性
PAH的复杂血管病理生物学特征,包括肺血管细胞过度增殖、细胞外基质沉积和血管周围炎性细胞浸润,对既定治疗提出了挑战。目前PAH治疗的作用机制主要局限于通过纠正血管活性因子的失衡来实现血管扩张。评估这些治疗的临床试验主要集中于根据6MWD或由疾病进展或住院引起的发病率和死亡率终点来确定其益处;迄今为止,没有临床试验证明哪种药物组合对个人最有效,也没有提供确凿的疾病修饰证据。因此,医生缺乏证据来预测哪种药物或药物组合对特定患者最有效。虽然缺乏允许预先识别可能反应者的个性化医学方法(如开处方钙通道阻滞剂时),但“巨量数据”和组学工具可能有助于填补这一证据空白。此外,需要新的策略来解决肺部病理重塑,并阻止或逆转PAH的进展。过去几十年的转化医学和临床研究已识别出支撑PAH中增殖、代谢和炎症异常的新致病途径,为新的治疗方向提供了见解。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#肺动脉高压#
57