Nature:加入IL-15增强为CAR-T细胞治疗实体肿瘤带来希望
2024-12-24 儿童肿瘤前沿 儿童肿瘤前沿 发表于陕西省
Andras Heczey 团队研究表明,IL - 15 增强型 GPC3 CAR - T 治疗实体瘤,控制率 66%、应答率 33%,安全性佳,单细胞测序解析其优势,为抗癌新策略。
嵌合抗原受体T细胞(CAR-T)在复发难治性B细胞白血病中已经取得了80%以上的完全应答率。传统放化疗对于体积较大的肿块以及转移性病灶疗效有限,因此需要寻找新的有效策略治疗实体肿瘤。目前,CAR-T治疗实体肿瘤的疗效不及B系白血病,部分原因可能是肿瘤微环境中的抑制信号阻碍了免疫应答,并且缺少IL-15等支持T细胞存活和发挥抗肿瘤功能的支持性细胞因子。
IL-15属于γ链细胞因子家族,对CD8+T细胞记忆形成、线粒体代谢以及T细胞扩增和持久性至关重要。临床前研究表明,IL-15与CAR-T共表达,能够显著提高CAR-T细胞的增殖能力、持久性和抗肿瘤能力。GPC3在部分实体肿瘤,特别是肝癌上显著表达,其在非肿瘤组织中不表达,因此是免疫治疗的理想靶点。
近日,Andras Heczey 团队于 Nature 发表题为 Interleukin-15-armoured GPC3 CAR T cells for patients with solid cancers 的临床研究,共纳入24名患者——12名接受普通型GPC3 CAR-T,12名接受IL-15增强型GPC3 CAR-T(15.GPC3 CAR-T)。结果表明GPC3 CAR-T组未产生显著的临床应答,15.GPC3 CAR-T组肿瘤控制率为66%,应答率为33%,无患者发生严重不良事件。该研究表明,IL-15能够增强GPC3 CAR-T在患者体内的扩增、生存以及抗肿瘤能力。

首先,作者评估了所有接受GPC3 CAR-T的24名患者的安全性。所有患者回输CAR-T细胞前均经历了氟达拉滨联合环磷酰胺的淋巴细胞清除预处理,回输一次CAR-T,观察期28天。回输了GPC3 CAR-T的12名患者中,回输剂量为1x107/m2(6人)或3x107/m2(6人),该剂量安全但并未产生临床应答。回输了15.GPC3 CAR-T的12名患者中,回输剂量均为3x107/m2。IL-15增强组的CRS相关事件多于普通组,3名患者在给予安全开关iC9诱导药物rimiducid后,CRS症状迅速解除。该部分研究表明,GPC3 CAR-T和15.GPC3 CAR-T在临床应用中均安全,CAR-T相关副作用能够被有效控制。
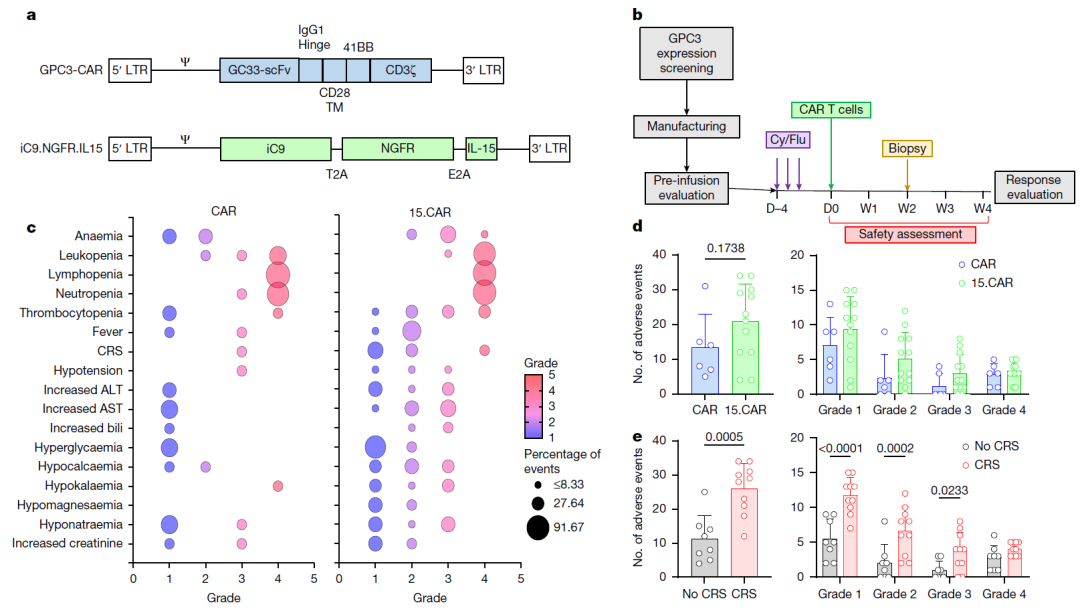
图1:普通型GPC3 CAR-T和IL-15增强型GPC3 CAR-T的结构简图、患者治疗流程图以及安全性特征
其次,作者评估了患者的肿瘤应答情况。接受3x107/m2剂量的GPC3 CAR-T组患者均无应答,接受相同剂量15.GPC3 CAR-T的12名患者中,4名疾病进展、4名疾病稳定、4名部分应答。其中,2名肿瘤负荷降低26%,1名肿瘤负荷降低12.8%,2名患者的AFP水平较回输前显著下降。该部分研究表明,接受15.GPC3 CAR-T细胞治疗的疾病控制率为66.7%,应答率为33.3%。
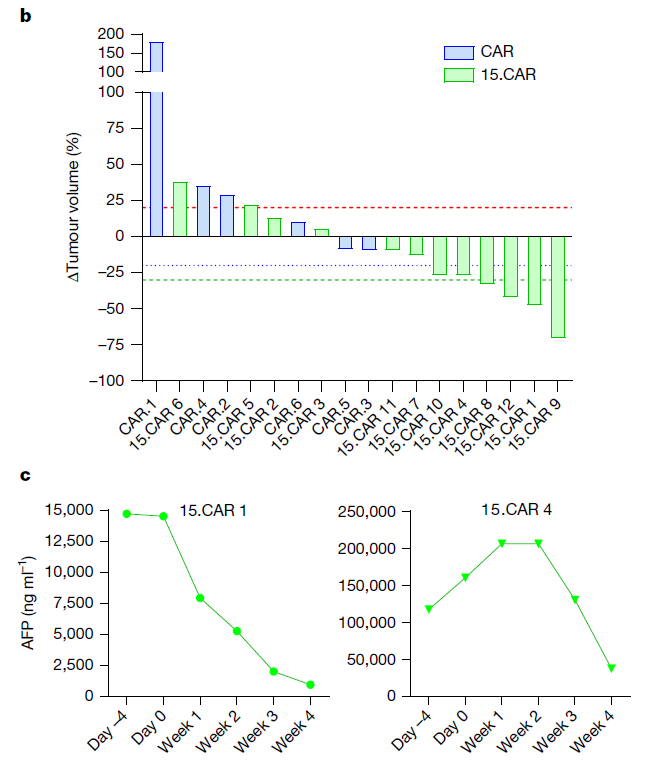
图2:抗肿瘤应答的特征
再次,为了对比GPC3 CAR-T和15.GPC3 CAR-T的基线基因差异,作者利用单细胞转录组测序分析了36722个CAR-T产品阶段细胞,鉴定出12个独立细胞簇中基因表达存在差异富集。15.GPC3 CAR-T细胞中,CD8、细胞溶解活性相关基因表达增加,共刺激受体和TCF7下调,且IL-15 共表达使CAR-T细胞表现出较低的糖酵解和较高的氧化磷酸化特征。在蛋白水平,15.GPC3 CAR-T的中央记忆细胞降低,效应记忆和效应细胞增加,PD-1和TIM3表达与CAR-T组相似,但LAG3表达更高。15.GPC3 CAR-T在外周血中的扩增能力显著优于GPC3 CAR-T,在15.GPC3 CAR-T队列中,应答者体内的CAR-T细胞扩增能力显著优于非应答者。该部分的研究表明,15.GPC3 CAR-T在产品阶段已经处于执行功能的效应细胞状态,并且在体内扩增能力更强,这些可能是15.GPC3 CAR-T疗效更好的原因。
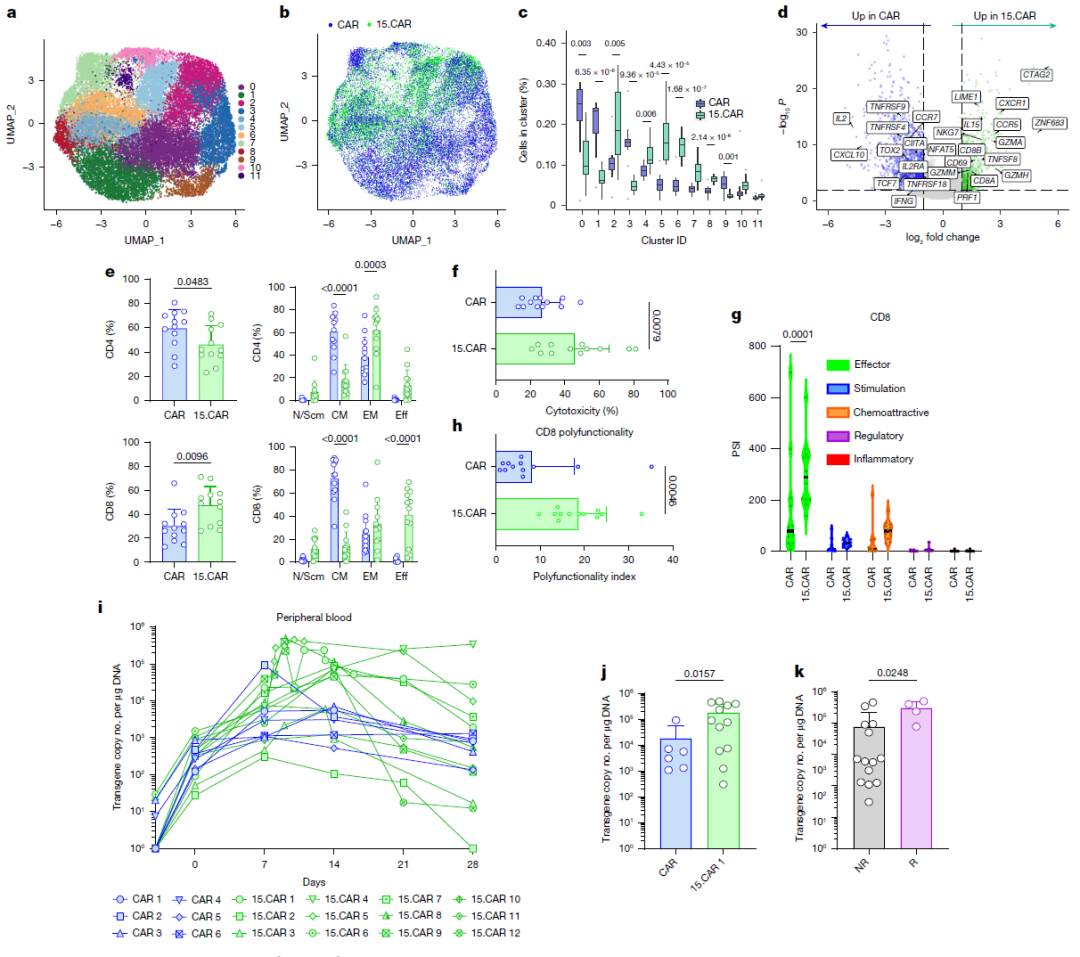
图3:GPC3 CAR-T和15.GPC3 CAR-T细胞特征对比以及患者体内扩增情况
最后,为了进一步探究15.GPC3 CAR-T细胞扩增和杀伤肿瘤能力提高的原因,作者将回输2-3周后外周血和肿瘤活检中的CAR-T细胞与回输前产品进行对比,单细胞测序的结果表明,回输后外周血中GPC3 CAR-T和15.GPC3 CAR-T细胞与产品相比,NK样分化、细胞毒性效应功能和耗竭相关基因上调,低分化记忆细胞、细胞因子信号相关基因及对应基因集下调,两种CAR-T细胞接触肿瘤细胞后启动效应分化导致增殖能力下降。15.GPC3 CAR-T组应答者和非应答者中与细胞毒性等相关基因上调,与低分化初始和记忆亚群相关基因下调。与非应答者的细胞相比,应答者的15.GPC3 CAR-T细胞显示出AP1家族成员FOS、FOSB、JUN、JUNB和JUND以及与I型干扰素(T1IFN)信号传导相关基因的上调,以及SWI/SNF染色质重塑复合物中基因抑制。该部分研究通过单细胞测序的方法进一步揭示了与15.GPC3 CAR-T治疗患者应答相关的基因特征。
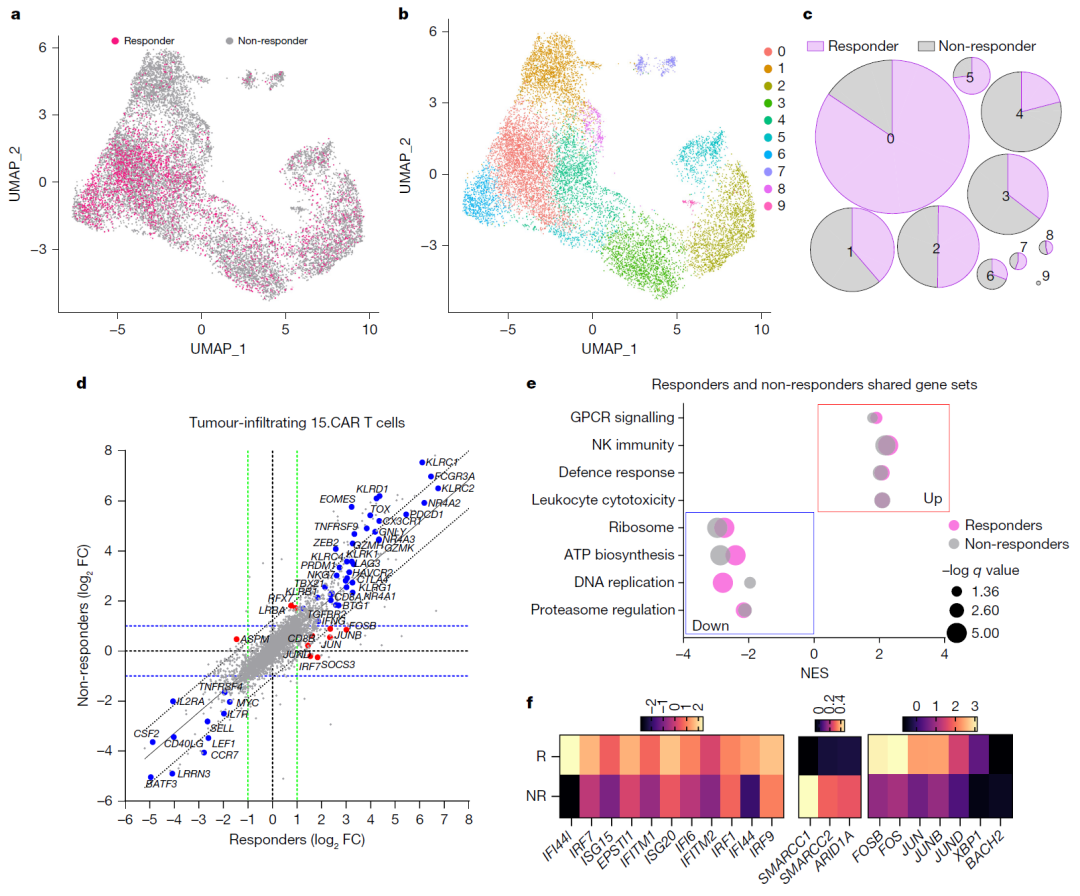
图4:对比15.GPC3 CAR-T队列中应答者与非应答者的单细胞基因表达谱
综上所述,接受15.GPC3 CAR-T细胞治疗患者的抗肿瘤反应率高于GPC3 CAR-T,部分患者肿瘤体积缩小、血清标志物降低,显示出较好的抗肿瘤活性。IL-15增强型CAR-T治疗是安全的,IL-1/IL-6抑制剂和iC9开关能够迅速解除CRS症状和相关毒性。与此同时,单细胞测序解析了15.GPC3 CAR-T的多组学特征和基因表达变化,为阐释其疗效提高提供了依据。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#实体肿瘤# #嵌合抗原受体T细胞#
5