目前,CAR-T治疗已经在某些血液肿瘤取得了成功,但事实上,细胞因子释放综合征(CRS)一直被视为CAR-T细胞治疗最大的阻碍。尽管能够在CAR-T细胞治疗之前使用药物管理CRS,但是不能在CAR-T细胞输注后控制。
CRS是在肿瘤患者完成CAR-T细胞输注后,大量免疫细胞被激活并快速增殖,引起IL-6、IL-1、IL-12、TNF-α、IFN-α、GM-CSF等细胞因子的过度级联释放,最终形成“细胞因子风暴(cytokine storm)”。
这些细胞因子介导的过度免疫反应会引起患者发热、肌痛、低血压、呼吸困难、凝血障碍、终末器官功能障碍等临床表现,这些是目前临床中最常见的、高发的CAR-T细胞的毒副作用。
CAR-T治疗相关毒性的预防策略,一方面可以通过CRS和神经毒性的预测性生物标志物来进行检测,通过密集的监测及时做出反应;另一方面是设计更加安全的CAR-T细胞疗法,而目前已经达成共识的策略是给CAR-T装上“安全开关”,在人为可控下进行治疗,且在不良反应发生前及时踩刹车。
目前,有不少公司在研发携带安全开关的CAR-T细胞,例如Bellicum、Cellectis、Autolus Therapeutics、Poseida Therapeutics、Ziopharm Oncology以及Precigen等。
日前,Bellicum Pharmaceuticals宣布旗下靶向Her2的CAR-T疗法BPX-603的新药研究申请(IND)获得美国FDA的批准。BPX-603是该公司首款双开关GoCAR-T®候选产品,同时结合了共刺激MyD88/CD40的激活开关和CaspaCIDe®安全开关。

▲ CID技术平台(图片来源:Bellicum)
通过病毒载体,将特定DNA的分子导入靶细胞,使靶细胞表达CID蛋白。CID蛋白包括信号区域和结合区域,rimiducid分子没有和CID结合区域结合起来的时候,信号是关闭的。当与CID蛋白结合区域结合成二聚物后,二聚物会开启下游信号的级联反应。
事实上,Bellicum是这方面的领导者之一,该公司基于核心技术CID技术平台(化学诱导的二聚体化技术),开发了一系列显著降低细胞因子风暴副作用的免疫疗法,通过给信号域引入并结合特殊设计的CID,给CAR-T疗法添加一个分子开关rimiducid来控制信号通路的开闭,使得细胞疗法变得更可控,从而解决了个体差异大、剂量难以控制、易出现严重副作用等问题,对治疗效果进行质量调控。
Bellicum的核心技术是CID技术平台(化学诱导的二聚体化技术),在该平台的基础上,Bellicum 开发了一系列显著降低细胞因子风暴副作用的免疫疗法。通过给信号域引入并结合特殊设计的CID,给CAR-T疗法添加一个分子开关rimiducid来控制信号通路的开闭,使得细胞疗法变得更可控,从而解决了个体差异大、剂量难以控制、易出现严重副作用等问题,对治疗效果进行质量调控。
值得一提的是,该公司还成功开发了“双安全开关”的CAR-T细胞,于2019年发表的研究论文 Two-Dimensional Regulation of CAR-T Cell Therapy with Orthogonal Switches 中,Bellicum初步证实了这种新颖的、可调节的双开关系统可以以药物依赖性方式促进CAR-T细胞扩增并且延长持久性,同时提供了安全开关以减轻毒性。
GoCAR-T技术,使CAR-T细胞包含两个共刺激信号结构域活化开关。GoCAR-T细胞在抗原不存在的条件下存活、在抗原存在的条件下增殖,并且只有当肿瘤细胞和Rimiducid同时存在的情况下T细胞杀伤功能才会被激活。
获批临床的双开关CAR-T
BPX-603是Bellicum公司双开关GoCAR-T®的首款候选产品,同时结合了共刺激MyD88/CD40的激活开关和CaspaCIDe®安全开关,用于治疗Her2阳性实体瘤。
诱导型MyD88/CD40(iMC)
MyD88/CD40是激活和增殖的信号分子。MyD88蛋白在细胞受到压力、生长因子、细菌或病毒刺激后发挥作用,CD40是在抗原呈递细胞中发现的一种共刺激蛋白。
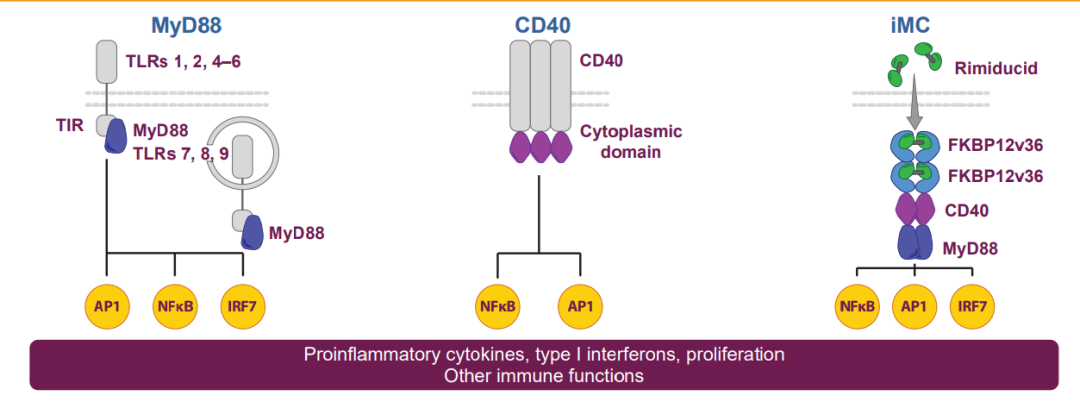
▲ iMC(图片来源:Bellicum)
激活和增殖的信号分子。MyD88蛋白在细胞受到压力、生长因子、细菌或病毒刺激后发挥作用,CD40是在抗原呈递细胞中发现的一种共刺激蛋白,先前,MyD88和CD40的作用在树突状细胞治疗中已有研究,Bellicum的新技术把它们应用到了以T细胞免疫疗法中。
诱导型MyD88 / CD40(iMC)在给予二聚化剂rimiducid时,可以为CAR-T细胞提供可控的共刺激作用,并且增强了其增殖和存活以及对抗血液瘤和实体肿瘤模型的活性。rimiducid(Rim,AP1903)具有两个对称的表面,其与FKBP12的F36V变体(Fv)具有高亲和力(Kd~0.1nM),导致iMC的寡聚化,并实现MyD88和CD40共诱导信号传导。
CaspaCIDe®安全开关
Caspase-9是细胞凋亡信号通路的启动酶,激活后会产生信号级联反应,包括最终导致细胞凋亡的Caspase-3的活化。Caspase-9可以被小分子化合物CID诱导二聚化,从而启动CAR-T细胞的凋亡通路。
CaspaCIDe是用来消除毒性细胞的安全开关技术,主要应用在造血干细胞移植和TCR治疗的候选药品中,如BPX-501、BPX-701。如果患者在治疗中出现了严重的副作用,rimiducid分子将会激活CID分子上的Caspase-9信号域,从而消除全部或部分的毒性细胞,减轻治疗中的严重副作用。
Bellicum公司总裁兼首席执行官Rick Fair表示:“本次获得FDA的批准,是Bellicum一个重要的里程碑,增加了临床试验,以评估我们新颖的GoCAR-T技术。我们期待着今年晚些时候在表达HER2的实体瘤患者中启动BPX-603的1/2期试验。”
新型可控细胞免疫疗法的领导者
Bellicum公司专注于开发用于治疗血液肿瘤、实体瘤以及罕见遗传性血液疾病的新型可控细胞免疫疗法,除了BPX-603,还拥有两款进入临床试验的候选产品。
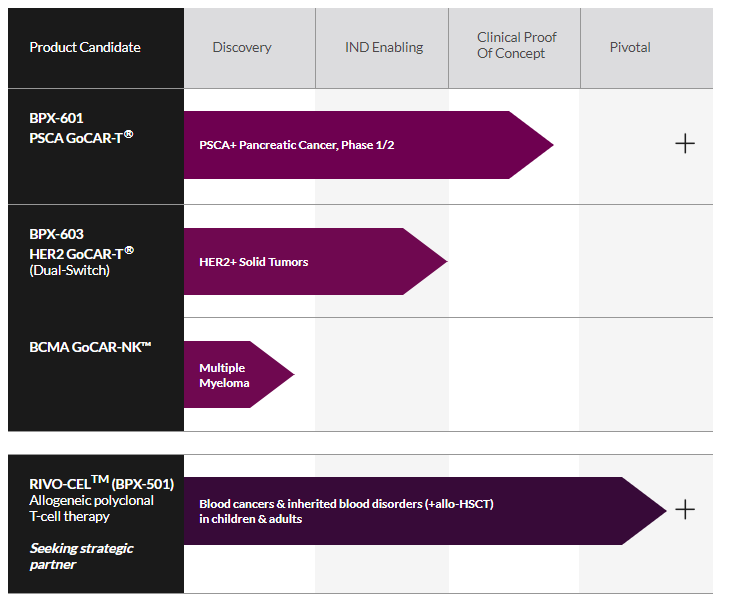
▲ Bellicum公司的研发管线(图片来源:Bellicum)
该公司研发管线介绍
BPX-501
BPX-501是目前Bellicum发展最快的细胞疗法药物,这种药物主要用于造血干细胞移植(HSCT)患者出现的移植物抗宿主病(GVHD)。目前该药物在单倍体造血干细胞移植上拥有良好的初期数据。Bellicum先导产品BPX-501已经在儿童白血病、淋巴瘤和遗传性血液病单倍体造血干细胞移植治疗中取得了良好的早期结果。
单倍体造血干细胞移植往往伴随GVHD风险,其中单倍体半相合移植GVHD风险更大。在单倍体半相合移植治疗中通常需要去除T细胞来减少移植物抗宿主病的风险,但缺乏供体T细胞会导致移植病人的感染率增加。加入BPX-501可以降低感染率、缩短住院时间,获得更好的治疗效果。
BPX-501利用专有的CaspaCIDe安全开关技术,导入rumiducid激活剂,控制消除有毒性的T细胞,成功解决了医生不愿进行高GVHD风险的单倍体半相合移植的问题。
欧洲委员会和美国食品和药物管理局(FDA)授予了BPX-501和rimiducid联合疗法的孤儿药资格。
BPX-601
BPX-601药物目前开展了实体瘤CAR-T免疫治疗的1期治疗计划。它是公司GoCAR-T系列产品的候选药物,目的是治疗表达前列腺干细胞抗原(PSCA)的多种恶性实体瘤,包括前列腺癌、胰腺癌、膀胱癌、食道癌和胃癌。
BPX-701
BPX-701是一种用于急性髓细胞白血病(AML)和骨髓增生异常综合征(MDS)TCR细胞免疫治疗的候选药物,它的靶点是黑色素瘤特异性抗原。
综上, Bellicum专有的“安全开关”技术给目前细胞治疗发展过程中所遇到的难题提供了很好的解决方案,我们也期待着其后续临床进展顺利,早日为众多患者带来安全有效的治疗方案。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#CAR-#
63
#FDA批准#
76
了解一下
141
#CAR-T细胞治疗#极有潜力,虽然难度巨大。这种双安全开关可以减少大家的顾虑。
180