AJH:多发性骨髓瘤BCMA CAR-T后的抗骨髓瘤治疗结局,仍有待提高
2022-10-10 聊聊血液 聊聊血液
BCMA CAR-T 细胞疗法在复发/难治MM中显示出令人鼓舞的结果,在既往中位3-9线治疗(包括既往抗 CD38单抗治疗)的患者中也可获得较高缓解率73%-95%。然而即使在BCMA CAR-T 之
尽管过去二十年多发性骨髓瘤 (MM) 的治疗取得了巨大的发展,结局也有了实质性的改善,但 MM 仍然无法治愈,绝大多数患者都会发生疾病进展。患者会复发或对蛋白酶体抑制剂 (PI)、免疫调节剂 (IMiD) 或抗 CD38 单克隆抗体 (MoAbs) 难治,导致预后不良,中位总生存期 (OS) 仅有5.6个月,而细胞遗传学高危患者的预后更差。
BCMA CAR-T 细胞疗法在复发/难治MM中显示出令人鼓舞的结果,在既往中位3-9线治疗(包括既往抗 CD38单抗治疗)的患者中也可获得较高缓解率73%-95%。然而即使在BCMA CAR-T 之后,患者仍会不可避免地继续复发,而BCMA CAR-T 复发后患者的预后数据和患者管理建议仍缺乏。
近日American Journal of Hematology发表了上海长征医院杜鹃教授为通讯作者的一篇文章,作者描述了I/II 期临床试验中 HDS269B 治疗进展后,接受后续抗骨髓瘤治疗 (subsequent anti-myeloma therapies ,sAMT) 的20例患者的结局,并探讨了可能的后续治疗策略,但总的来说,CAR-T 治疗后患者所需的最佳策略仍有待确定。

作者回顾性分析了49例接受 HDS269B 治疗的患者,其中20例患者在2018年5月至2022年5月期间接受CAR-T后的sAMT。
在 CAR-T 后接受治疗的20例患者中,治疗之间的中位时间为310.5天。基线临床特征见表1。患者的中位年龄为61岁,自诊断的中位时间为4.3年。7例患者 (35%) 的 ECOG 评分为3-4,而分别有60%和45%的患者为 ISS III 和R-ISS III,25%的患者伴髓外病变。由于5例患者的 FISH 不可用,仅20%的患者为细胞遗传学高危,定义为存在del(17p)、t(4;14) 或t(14;16)。既往治疗线的中位数为5,包括既往至少接受过一种 PI 和一种 IMiD 治疗。3例患者 (15%) 接受过抗CD38单抗,8例患者 (40%) 既往接受过自体干细胞移植。所有患者均为三类暴露,CAR-T治疗时无三类或五类难治患者。

患者在疾病进展后启动后续治疗,其中包括含抗 CD38单抗方案 (n= 8)、含泊马度胺方案 (n= 4) 和第二轮 CAR-T (n= 11);其他患者接受既往方案再次治疗,如来那度胺/沙利度胺和硼替佐米的三联或四联治疗或含V-DECP/DECP 方案。
 患者中位治疗线数为2,20例患者在 CAR T 后接受sAMT,由于3例患者无法评估,因此 ORR 和 CBR 评估的总数为17例(表1)。首次 sAMT 的 ORR 为35%(6/17),临床获益率为65%(11/17):2例患者达到CR,1例患者VGPR,3例患者PR,2例患者MR,3例患者 SD。
患者中位治疗线数为2,20例患者在 CAR T 后接受sAMT,由于3例患者无法评估,因此 ORR 和 CBR 评估的总数为17例(表1)。首次 sAMT 的 ORR 为35%(6/17),临床获益率为65%(11/17):2例患者达到CR,1例患者VGPR,3例患者PR,2例患者MR,3例患者 SD。
9例患者 (45%) 接受了3次以上sAMT。在接受达雷妥尤单抗治疗的8例患者中有6例缓解,其中1例VGPR,4例PR,1例SD。4例接受含泊马度胺治疗患者中,PR 和MR各1例,而2例患者SD。此外11例患者接受第二轮 CAR-T 作为挽救治疗,包括 CD19-BCMA 双靶点CAR-T (n= 7)、人 BCMA CAR-T (n= 3) 或通用CAR-T (U CAR-T,n= 1);但U CAR-T患者在输注后1个月发生早期死亡,因此未进行缓解评估。接受抗人 BCMA CAR-T 的3例可评估患者的 ORR 为67%,包括2例 CR和1例PD;此外CD19-BCMA 双靶点CAR-T 的7例患者中,仅1例达到SD,而其他患者的最佳缓解为PD。
CAR-T 后 (HDS269B) 复发患者开始 sAMT 后的中位 OS 和 PFS 分别为11.9个月和4.5个月。

尽管接受二次 CAR-T 再治疗的人数很少,但在既往鼠 BCMA CAR-T 治疗后接受抗人 BCMA 治疗的患者显示生存期延长,中位 OS 未达到,中位 PFS 为14.3个月,比接受 CD19-BCMA 双靶点 CAR-T 的患者更长(中位 OS 和 PFS 分别为8.1个月和1.1个月)。但这需要在更大的患者系列中进行更长时间的随访和确认,而前瞻性比较研究最佳。

本研究中,RRMM患者在BCMA CAR-T 后接受后续抗骨髓瘤治疗的临床结局较差,中位 PFS 和 OS 分别仅有4.5个月和11.9个月,显著短于既往报道,该差异可能与体能状态、既往治疗史、难治状态、治疗选择有限、患者偏好和生活质量等有关。
目前关于 BCMA CAR-T 治疗后进展的患者的治疗选择的数据有限,根据报道,对于 BCMA CAR-T 治疗后复发和/或难治的患者,主要评估了含卡非佐米、抗CD38单抗、塞利尼索或泊马度胺的再治疗。但本研究中的患者为大量预治疗,并已用尽可用选择,特别是当时没有elotuzumab、panobinostat、belantamab mafodotin 和双特异性 T 细胞结合单抗等药物。
影响 CAR-T 细胞活性的因素是多方面的,包括肿瘤相关因素、微环境成分和预制 T 细胞的质量(生产工艺可能导致产品相关特征的变化)。肿瘤抗原丢失通常由克隆演变/转移导致,也包括某些情况的其他原因导致,如胞啃(trogocytosis)。但抗原阳性复发的原因比较复杂,包括 T 细胞耗竭和衰老、共刺激结构域、产生抗药抗体 (ADA) 和免疫逃逸等,可能造成 CAR-T 细胞持久性差。
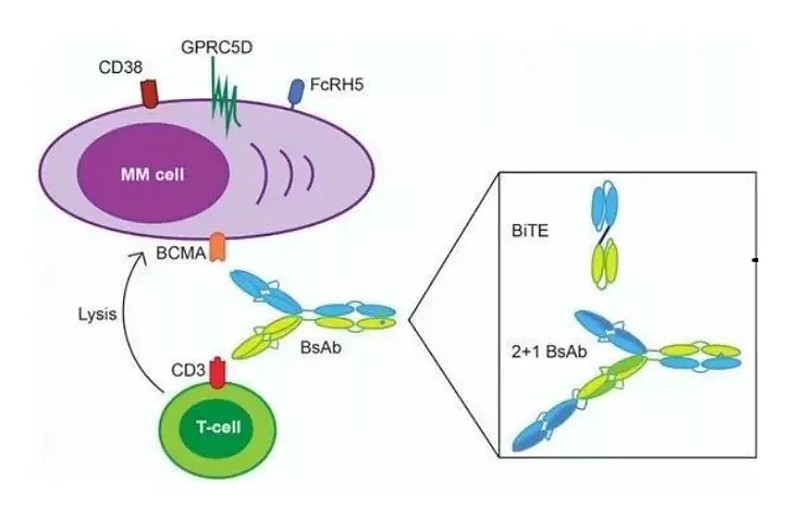
尽管最佳策略尚未确立,但初步证据表明,靶向不同 BCMA 或 BCMA 后产品的 CAR-T 细胞可能有效。在接受全人 BCMA 靶向 CAR-T 细胞产品的4例患者中报告了深度缓解。同样,本研究中接受人抗 BCMA CAR-T 治疗的患者的 OS 趋势优于接受 CD19-BCMA 双靶点治疗的患者。虽然样本量非常有限,但本研究证实了人抗 BCMA CAR-T 治疗具有令人印象深刻的效力和持久性,特别是相较于 CD19-BCMA 双靶向治疗,这表明全人源 CAR-T 治疗可能具有降低免疫原性的优势,从而促使 CAR-T 细胞持久性更好(尽管仍会在先前鼠 BCMA CAR-T 治疗后复发)。最近GPRC5D CAR-T 细胞 (OriCAR-017) 自体治疗被证实ORR可达75%。
双特异性抗体 (BsAbs) 招募 T 细胞到肿瘤细胞的治疗也sAMT显示一定前景。Talquetamab (双特异性 IgG4 抗体) 的 ORR 约为70%,其中30%的患者RRMM 的1期试验 (NCT03399799) 中接受过抗 BCMA 治疗;cevostamab( FcRH5xCD3 双特异性抗体)的 I 期试验治疗了28例 (17.5%) 既往接受过≥1次 CAR-T 的患者,在> 90 mg的目标剂量水平下,既往暴露于 CAR-T 的患者的 ORR 为44.4%(4/9例患者);teclistamab(BCMA xCD3单抗)治疗CAR-T 暴露患者的 ORR 为45%。鉴于与 CAR-T 细胞产品相比的疗效,T细胞衔接抗体可能是一种更有吸引力的免疫治疗选择,但目前仅在临床试验中可用。
总的来说,CAR-T 细胞疗法在 MM 患者的治疗取得了可喜的结果,但大多数晚期 MM 患者最终都会发生疾病进展,因此需要新的策略来进一步改善 CAR-T 细胞治疗的结局,但CAR-T 治疗后患者所需的最佳策略仍有待确定。尽管如此,随着在真实世界环境中积累更多数据和后续各种抗骨髓瘤治疗的使用,评估可持续性对于优化抗 BCMA CAR-T 治疗后复发患者的治疗方案至关重要,因此有必要对后续抗骨髓瘤治疗方案进行头对头比较,以提高其在临床中的实际应用。
参考文献
Dongjian Chen, Xiaoxian,g Wang, Zhi Chen,et al. Subsequent anti-myeloma therapy after maturation antigen (BCMA) chimeric antigen receptor (CAR)-T cell (HDS269B) treatment in patients with relapsed/refractory multiple myeloma.Am J Hematol . 2022 Oct 5. doi: 10.1002/ajh.26745
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言