Nature重磅:通用型癌症疫苗来了,同时激活T细胞和NK细胞,加速消灭癌细胞
2022-05-28 nagashi “生物世界”公众号
大多数癌症疫苗都靶向癌细胞表达的特异性抗原,帮助免疫系统识别和攻击这些变异的细胞。然而,这些抗原的性质和免疫原性(激发免疫反应的能力)对每个人而言都是独特的。
https://www.nature.com/articles/s41586-022-04772-4#citeas随着生物学和医学的发展,人类对癌症以及自身免疫系统的认知愈渐加深,科学家们也意识到免疫系统才是对抗癌症最具杀伤力的武器。近些年来,癌症免疫治疗的兴起也让越来越多的科研团队开始专注于癌症疫苗。
值得注意的是,大多数癌症疫苗都靶向癌细胞表达的特异性抗原,帮助免疫系统识别和攻击这些变异的细胞。然而,这些抗原的性质和免疫原性(激发免疫反应的能力)对每个人而言都是独特的,并且癌细胞经常通过变异和改变抗原呈递来实现免疫逃逸,这些因素都限制了通用型癌症疫苗的开发。
2022年5月25日,美国 Dana-Farber 癌症研究所的研究团队在国际顶尖学术期刊 Nature 上发表了题为:A vaccine targeting resistant tumours by dual T cell plus NK cell attack 的研究论文。
该研究开发了一种新型癌症疫苗,能克服癌症免疫中的个体差异,即通过靶向 MICA/MICB 应激分子激活两种主要类型的免疫细胞—— T 细胞和 NK 细胞,引起独立于肿瘤抗原的协同全面攻击。初步结果表明了这一癌症疫苗在小鼠和恒河猴中的效力和安全性。

癌症疫苗(Cancer Vaccines),是一种通过靶向肿瘤细胞相关抗原来激活人体免疫系统,发挥特异性抗肿瘤效应的治疗性和预防性免疫治疗策略。
目前,我们所熟知的一些癌症疫苗都属于预防性疫苗,如预防宫颈癌的人乳头瘤病毒(HPV)疫苗,而大多数治疗性癌症疫苗的临床试验结果都不尽如人意。其中很大一部分原因在于癌细胞抗原的多样性和肿瘤免疫逃逸机制。
如果能开发一种通用型的治疗性癌症疫苗,将深刻地改变当今癌症治疗格局。

Kai Wucherpfennig
在这项最新研究中,Kai Wucherpfennig 团队提出了一种癌症疫苗的新设计,这种疫苗靶向两种表面蛋白 MICA 和 MICB,它们可以激活 T 细胞和 NK 细胞的配体,加速免疫系统消灭肿瘤。

新设计的癌症疫苗可以增加肿瘤细胞表面的MICA/B的表达量
MICA/MICB 是一种细胞应激分子,在正常组织中表达量很少,但是在多种肿瘤细胞中表达量明显上调。研究表明,MICA/MICB 可以与 T 细胞和 NK 细胞表面的 NKG2D 受体结合而被效应细胞识别,介导对肿瘤细胞的杀伤作用。
然而,狡猾多端的肿瘤细胞并不会心甘情愿地任人鱼肉,它们通过蛋白水解过程对 MICA/MICB 进行分解切割,减少它们激活免疫细胞的可能性,从而逃避免疫攻击。但这种全新设计的癌症疫苗能够阻止肿瘤细胞的这种切割效应,提升肿瘤表面的的 MICA/MICB 蛋白的水平。
不仅如此,这个过程还可以激活树突状细胞向 T 细胞进行肿瘤抗原呈递,提升 NK 细胞的细胞毒性,最终更易引发 T 细胞和 NK 细胞协同双重攻击。
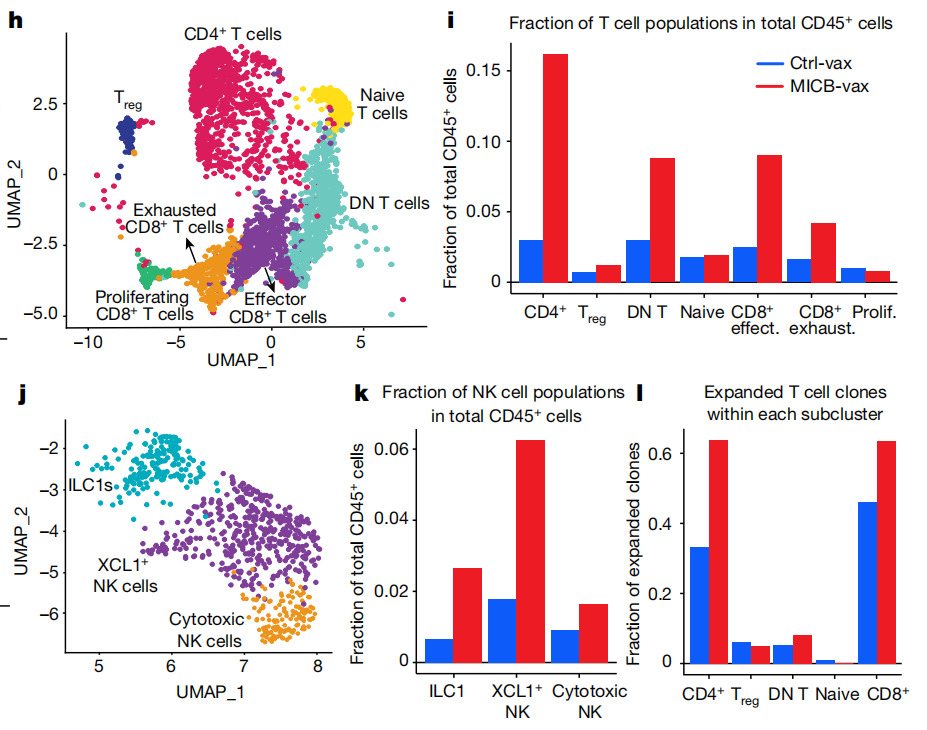
新设计的癌症疫苗激活T细胞和NK细胞,引发协同双重攻击
为了验证这种癌症疫苗的有效性和安全性,研究团队在小鼠和恒河猴模型中进行了初步测试,结果表明这种疫苗能够增进对普通肿瘤及耐药肿瘤的免疫保护,并且没有明显的副作用。
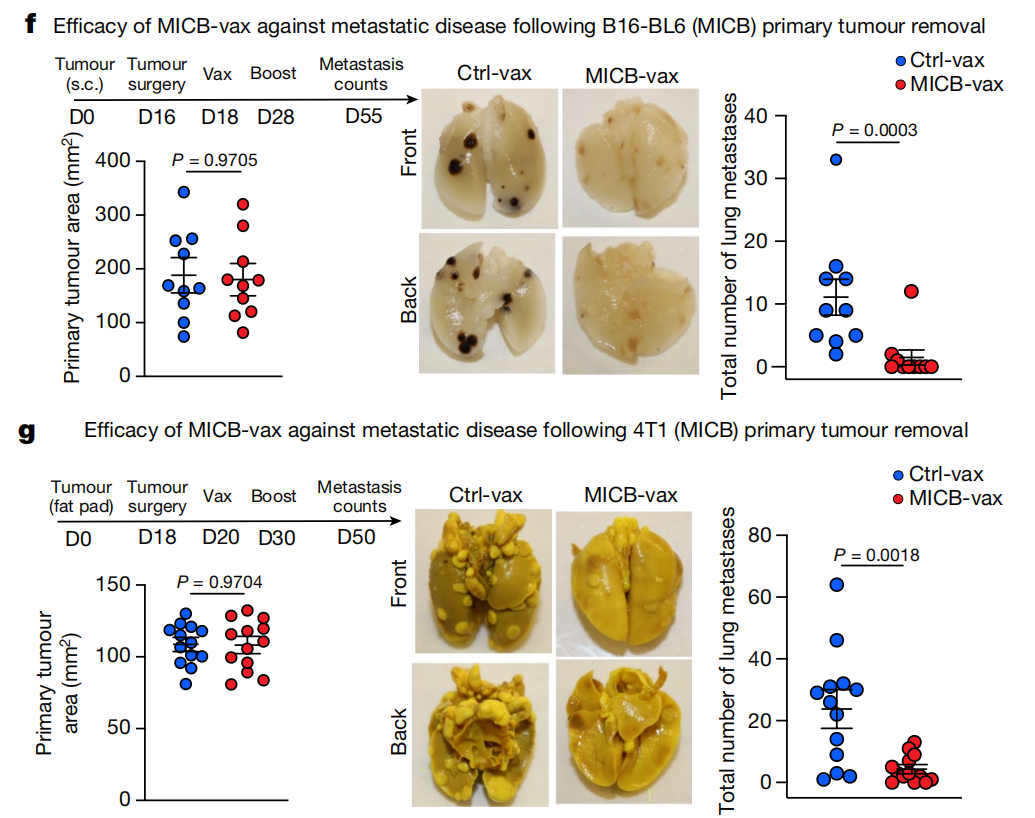
新设计的癌症疫苗在小鼠和恒河猴模型中的效力和安全性
总而言之,这项研究展示了一种全新癌症疫苗,它可以阻止肿瘤细胞对 MICA/MICB 应急分子的切割,激活 T 细胞和 NK 细胞,引起独立于肿瘤抗原的协同全面攻击,对耐药肿瘤具有良好的治疗效果。

研究模式图
虽然尚需进一步的临床试验来评估这种癌症疫苗在人类中的潜力,但这依然是治疗性癌症疫苗的一个重大进步,未来希望遵循这种设计思路的癌症疫苗能够为人类带来更多福祉,为广大癌症患者带来新希望。
原始出处:
Badrinath, S., Dellacherie, M.O., Li, A. et al. A vaccine targeting resistant tumours by dual T cell plus NK cell attack. Nature (2022). https://doi.org/10.1038/s41586-022-04772-4.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Nat#
94
#癌细胞#
149
#重磅#
0