自然疗法中的神奇成分:人参多糖对现代肥胖问题的革命性解决方法!
6小时前 梅斯循证中医药 MedSci原创 发表于陕西省
该研究揭示了PGP在调节HFD诱导的肥胖小鼠中的潜在作用及其作用机制,结果表明,PGP显著减轻了HFD小鼠的体重和脂肪积累,同时降低了血清中的TG和TC水平,并改善了肝功能。
自2012年起,肥胖首次被美国临床内分泌学家协会正式划归为慢性疾病范畴,并且已经成为全球范围内日益凸显的公共卫生议题。当前,肥胖的治疗主要依赖于生活方式的调整、药物治疗以及减重手术。该病症不仅严重损害个体的生活质量,还导致医疗开支的大幅上升。
此外,肥胖与多种代谢综合征的进展密切相关,这些综合征包括心血管疾病、胰岛素抵抗、血脂异常、高血糖以及肝脂肪变性。因此,及时采取预防和治疗措施以应对肥胖症已成为当务之急。研究显示,肥胖与肠道微生物群的失衡存在密切联系,众多肠道细菌被发现能够增加宿主的能量吸收、中枢食欲和脂肪储存,从而促进肥胖的发生和发展。
人参被发现能够促进粪肠球菌产生不饱和长链脂肪酸,从而有助于减轻肥胖小鼠的体重。同时,人参多糖(PGP)亦被证实具有降低血糖、提升代谢水平的功效。尽管如此,关于PGP改善肥胖的具体机制尚未明确。因此,研究PGP对肠道微生物群落结构、多样性以及对宿主代谢的影响显得尤为必要。
近日,一篇名为“Ginseng polysaccharide components attenuate obesity and liver lipid accumulation by regulating fecal microbiota and hepatic lysine degradation”的文章探讨了PGP的代谢调控机制。

图1 论文首页
PGP减轻了HFD诱导的肥胖小鼠的体重和脂肪积累
为验证PGP的潜在抗肥胖效应,该研究首先对高脂饮食(HFD)诱导的肥胖(DIO)小鼠进行了体重变化的评估。结果表明,每日经口给予PGP对DIO小鼠体重增长具有显著的抑制效果(图2A-B),且PGP干预能够逆转HFD引起的脂肪比例增加(图2C)。进一步的脂肪组织成像及重量分析显示,相较于HFD组,PGP组的内脏白色脂肪组织(iWAT)和棕色脂肪组织(BAT)的体积及重量均有所减少(图2E、F、H)。值得注意的是,PGP组的皮下白色脂肪组织(eWAT)重量略有增加(图2G)。由此可见,PGP能够减轻HFD诱导的肥胖小鼠体重增加及脂肪积累,表明PGP对DIO小鼠具有潜在的抗肥胖作用。
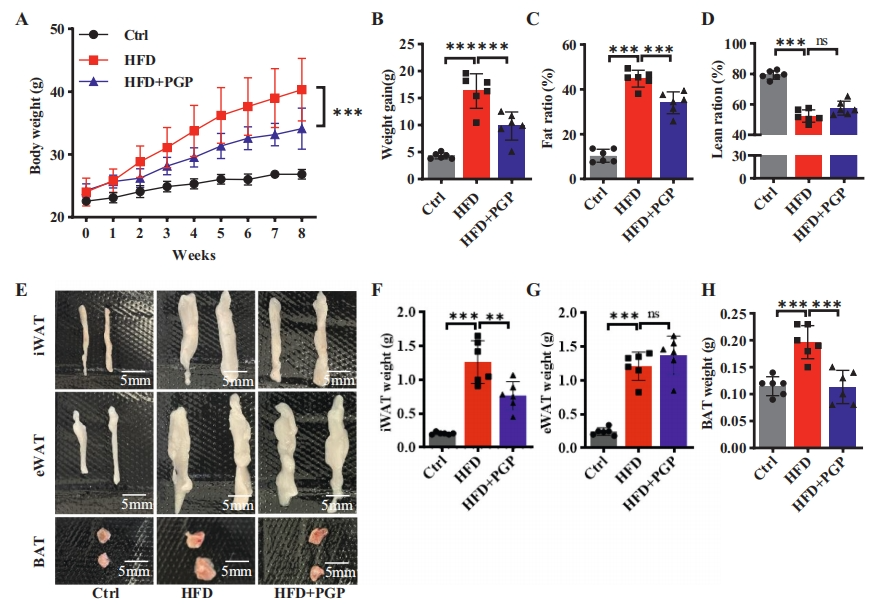
图2 PGP对HFD喂养小鼠体重和体脂的影响
PGP减轻了HFD引起的肥胖小鼠的高脂血症
脂质代谢功能障碍方面,研究通过检测血脂水平来研究PGP对HFD诱导的小鼠脂质代谢的影响。与HFD组相比,PGP显著降低了血清中的甘油三酯(TG)和总胆固醇(TC)水平,但对低密度脂蛋白胆固醇(LDL-C)和高密度脂蛋白胆固醇(HDL-C)水平无明显影响(图3A)。结果揭示,PGP能够缓解HFD诱导的小鼠高脂血症,但对降低血糖水平无明显效果。
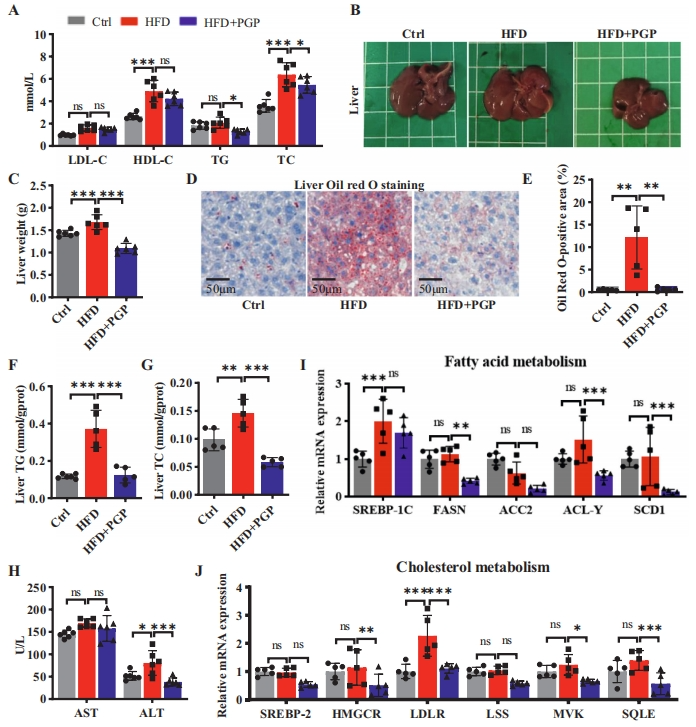
图3 PGP对HFD喂养小鼠血脂水平和肝脏稳态的影响
PGP可调节肝脂质代谢,改善肝损伤
脂肪肝的存在导致肝脏中积累了大量脂质,这破坏了肥胖状态下肝脏的正常生理功能。相较于对照组,HFD组的肝脏相对重量显著增加,并且颜色变浅。然而,对小鼠施以PGP后,肝脏的相对重量明显减少,并且其颜色得以恢复(图3B-C)。进一步的肝脏组织病理学检查揭示,HFD组的肝组织切片中存在大量脂滴积聚。值得注意的是,与HFD组相比,HFD+PGP组的脂滴大小和数量显著减少(图3D-E)。
此外,PGP治疗显著降低了由HFD引起的肝脏中TG和TC的升高(图3F-G)。血清中的天门冬氨酸氨基转移酶(AST)和丙氨酸氨基转移酶(ALT)是评估肝损伤的两个关键指标,结果表明,HFD组的血清AST和ALT水平高于对照组,而HFD+PGP组在接受预防性治疗后,ALT水平有所降低(图3H)。
为深入研究PGP在调节过程中对肝脏脂质代谢潜在机制的影响,研究探讨了PGP对脂肪酸及胆固醇代谢途径相关基因mRNA水平的作用。结果显示,PGP显著下调了脂肪酸代谢相关基因,包括FASN、ACC2、ACL-Y以及SCD1的表达水平,而对SREBP-1C的mRNA水平无显著影响(图3I)。
在胆固醇代谢方面,PGP抑制了肝组织中SREBP-2、LDLR、LSS、MVK以及SQLE的表达,但对HMGCR mRNA水平无影响(图3J)。综合分析表明,PGP能够减轻HFD诱导的肥胖小鼠肝脏脂质积累和损伤,这可能与其抑制脂肪酸和胆固醇代谢关键酶的活性有关。
PGP通过抑制脂肪酸和胆固醇代谢的关键基因来改善PA处理的AML12和HepG2细胞中的脂质积累
为深入探究PGP在体外对肝细胞脂质代谢的改善作用,研究构建了AML12和HepG2细胞两种脂质积累模型。尼罗红染色结果表明,25、50、100 μg/mL浓度的PGP显著抑制了PA诱导的AML12和HepG2肝细胞内脂质积累,并呈现出显著的剂量依赖性(图4A-B),效果与二甲双胍相似。进一步观察发现,100 μg/mL浓度的PGP显著降低了两种脂质积累细胞模型中的TG水平(图4C)。此外,PGP降低了PA诱导的AML12细胞中TC的水平(图4D),而HepG2细胞模型中未进行此研究。结果显示,PGP改善了PA诱导的肝细胞中的脂质积累,与肥胖小鼠肝组织的研究结果相一致。
研究还采用qPCR方法检测了未处理及PGP或Met处理的AML12细胞中脂肪酸和胆固醇代谢相关基因的表达水平。如图4E-G所示,PA处理显著提高了脂肪酸代谢基因SREBP-1C、FASN、ACL-Y的mRNA水平,而PGP处理逆转了这一趋势。与小鼠肝组织的研究结果相似,在PGP处理的AML12细胞中,胆固醇代谢关键基因如HMGCR、LDLR或LSS被抑制,但PGP介导的SREBP-2、MVK或SQLE的增加未见明显变化(图4H-M)。综上所述,PGP通过抑制脂肪酸和胆固醇代谢关键基因的表达,对肝细胞的脂质积累发挥积极影响。
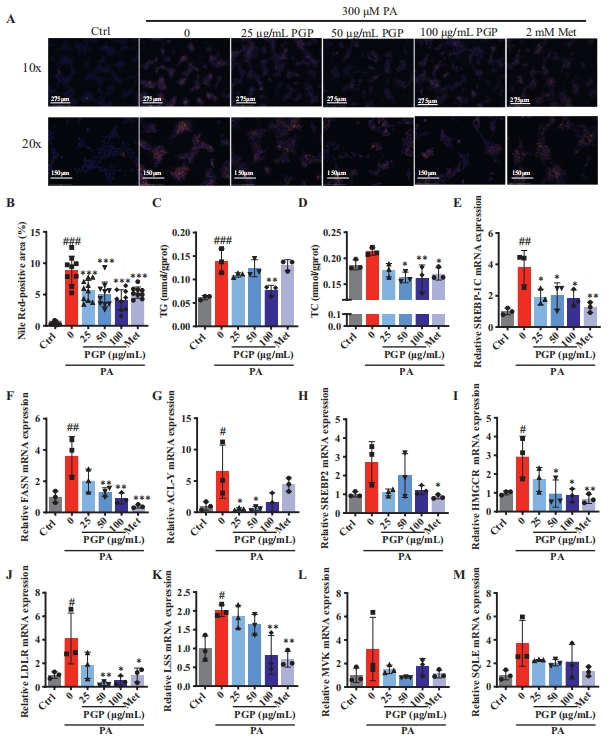
图4 PGP对PA诱导的AML12细胞脂质积累的影响
结论
该研究揭示了PGP在调节HFD诱导的肥胖小鼠中的潜在作用及其作用机制,结果表明,PGP显著减轻了HFD小鼠的体重和脂肪积累,同时降低了血清中的TG和TC水平,并改善了肝功能。
参考文献:
Liu Q, Zhang Z, Ji P, Liu J, Chen B, E M, Qi H, Hou T, Huang Q, Ding L, Guo C, Zhao D, Yang W, Wang Z, Li X. Ginseng polysaccharide components attenuate obesity and liver lipid accumulation by regulating fecal microbiota and hepatic lysine degradation. Int J Biol Macromol. 2024 Jun;269(Pt 1):131872. doi: 10.1016/j.ijbiomac.2024.131872
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#肥胖# #人参多糖#
5