疾病控制率近95%!“变革性”药物为晚期肺癌患者带来希望
2023-10-20 医学新视点 医学新视点 发表于上海
在本次大会上,肺癌ADC药物百花齐放,研究进展层出不穷。《医学新视点》基于大会研究摘要,整理了ADC药物热门研究的最新结果。
▎药明康德内容团队编辑
抗体偶联药物(ADC)是一类以单克隆抗体为载体,将小分子细胞毒性药物以靶向方式高效地运输至目标肿瘤细胞中的靶向生物制剂。与传统化疗相比,ADC结合了单克隆抗体的高选择性和细胞毒药物的高效力特性,可显著提高疗效并降低全身毒性。
在癌症治疗领域,ADC凭借在诸多适应证中的优异表现,已经逐渐成为医学领域新的焦点,被誉为癌症治疗的“变革性药物”。2023年欧洲肿瘤内科学会(ESMO)大会将于当地时间10月20日至24日在西班牙马德里召开。作为全球最具影响力的肿瘤学会议之一,ESMO官方近日披露了本次大会的研究摘要。在本次大会上,肺癌ADC药物百花齐放,研究进展层出不穷。《医学新视点》基于大会研究摘要,整理了ADC药物热门研究的最新结果。
治疗驱动基因异常的晚期肺癌,Dato-DXd疗效令人鼓舞!
对于驱动基因异常(AGA)的晚期或转移性非小细胞肺癌(NSCLC)患者而言,一旦靶向治疗和含铂化疗方案失去作用,这部分患者的治疗选择将变得十分有限。Dato-DXd是一种靶向TROP2的ADC药物。TROPION-Lung05试验旨在≥1线靶向治疗和含铂化疗治疗进展的AGA晚期或转移性NSCLC患者中评估Dato-DXd的疗效和安全性。本次ESMO大会公布了全球、开放标签、2期TROPION-Lung05试验的初步分析结果。
TROPION-Lung05试验纳入了EGFR、ALK、ROS1、NTRK、BRAF、MET 14外显子跳跃突变或RET突变的晚期或转移性NSCLC患者,并给予Dato-DXd(6mg/kg Q3W)治疗。试验主要终点为盲态独立中央审评(BICR)确认的客观缓解率(cORR)。
整体而言,共有137例患者(中位年龄61岁)接受≥1剂Dato-DXd;71.5%的患者既往接受≥3线治疗;56.9%的患者伴有EGFR突变。分析结果显示,整体患者的cORR为35.8%、疾病控制率(DCR)为78.8%、中位持续缓解时间(DOR)为7.0个月。
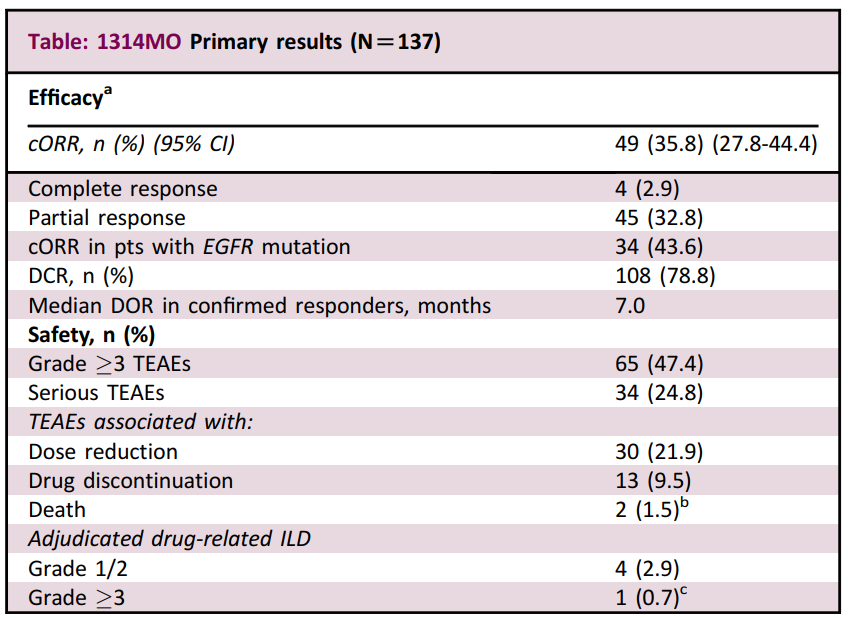
▲TROPION-Lung05试验初步分析结果(图片来源:参考资料[1])
总体而言,对于接受过多线治疗的AGA晚期NSCLC患者而言,Dato-DXd具有令人鼓舞的抗肿瘤疗效和有临床意义的持久疗效。此外,Dato-DXd治疗安全性可控,安全性特征提高与既往Dato-DXd相关研究报道的安全性一致。
聚焦双靶点ADC!BL-B01D1有望成为3代靶向药耐药后新选择!
BL-B01D1是一种由EGFRxHER3双特异性抗体通过可裂解连接子与新型拓扑异构酶Ⅰ抑制剂有效载荷结合的“first-in-class”新型ADC药物。在本次ESMO大会中,来自中山大学肿瘤防治中心的张力教授将报告BL-B01D1治疗NSCLC的1期试验的更新结果。
该试验纳入了局部晚期或转移性的NSCLC患者,并给予BL-B01D1(2.5、3.0、3.5 mg/kg D1D8 Q3W治疗,或5.0、6.0 mg/kg D1 Q3W)治疗。整体而言,截至2023年3月31日,共有114例标准治疗失败的NSCLC患者入组并接受≥1剂BL-B01D1治疗。
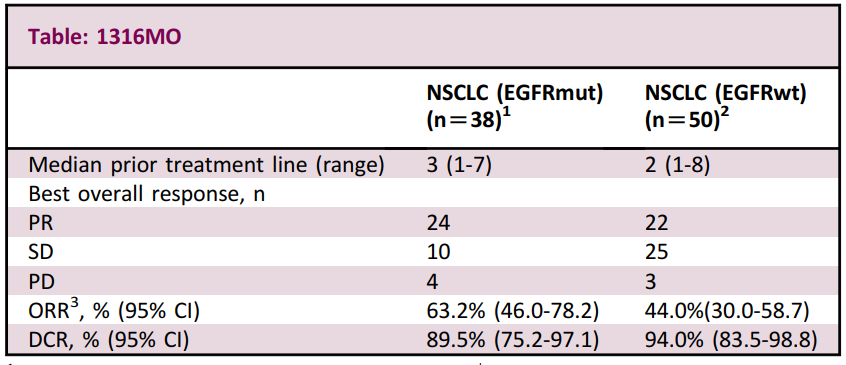
▲BL-B01D1治疗NSCLC的1期试验分析数据(图片来源:参考资料[2])
统计数据显示,88例患者的疗效可评估,EGFR突变和EGFR野生型NSCLC患者的客观缓解率(ORR)分别为63.2%和44.0%、DCR分别为89.5%和94.0%、中位无进展生存期(PFS)分别为6.9个月和5.2个月(中位PFS尚未成熟)。
整体而言,对于接受过多线治疗的局部晚期或转移性NSCLC患者而言,BL-B01D1治疗的疗效令人鼓舞(尤其是对于EGFR突变患者),且安全性可耐受。
ABBV-637联合奥希替尼有望治疗复发/难治性肺癌
ABBV-637是一种由EGFR靶向抗体和BCL-XL抑制剂组成的ADC药物。当前这项1期剂量递增和扩展研究评估了ABBV-637联合奥希替尼二线和三线治疗的安全性和初步疗效。试验纳入了奥希替尼起效但后续疾病进展的复发/难治性EGFR突变NSCLC患者,并给予ABBV-637+奥希替尼治疗。试验终点包括治疗相关不良事件(TEAE)、ORR、DCR等。
共有42例患者(中位年龄65岁)接受治疗,其中64%的患者既往接受过≥2线治疗。ABBV-637治疗的中位持续时长为113天,最常见的TEAE为天冬氨酸氨基转移酶升高(38%)、丙氨酸氨基转移酶升高(33%)、恶心(33%)和疲劳(21%)。
疗效分析结果显示,三线治疗队列患者的ORR为14%、DCR为73%;二线治疗队列患者的ORR为10%、DCR为65%。总体而言,ABBV-637联合奥希替尼治疗复发/难治性EGFR突变NSCLC患者显示出一定的临床疗效和可管理的安全性。
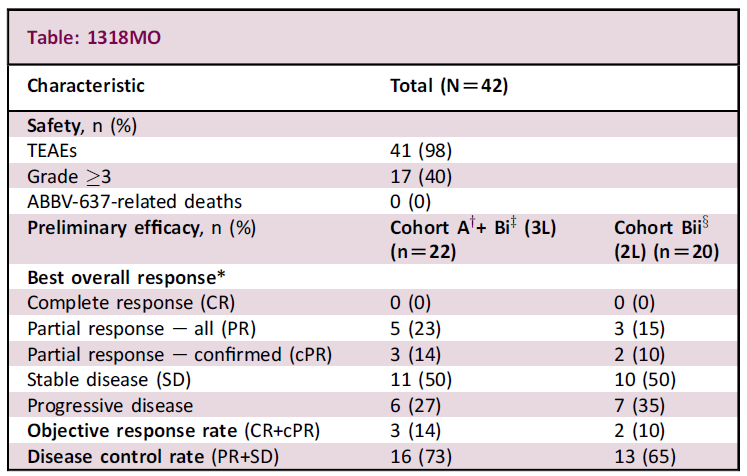
▲ABBV-637疗效数据(图片来源:参考资料[3])
HER3-DXd为脑转移患者的治疗带来希望
中枢神经系统(CNS)转移通常与肺癌患者更差的预后有关。HER3-DXd(patritumab deruxtecan)是一种靶向HER3的ADC。既往2期HERTHENA-Lung01研究的分析结果显示,HER3-DXd治疗EGFR-TKI和含铂化疗耐药的EGFR突变晚期NSCLC具有良好的疗效和可控的安全性。该试验纳入了伴有稳定脑转移的患者,本次ESMO大会报道了该试验颅内疗效的探索性分析结果。
整体而言,有95例患者基线合并脑转移、23例靶病灶可评估、72例仅有非靶病灶。晚期治疗中,患者既往中位接受过3线系统性治疗。分析结果显示,BICR确认的CNS ORR为20%(既往脑部未接受过放疗的患者颅内ORR更高,达到了37%)。患者中位DOR为8.5个月。
值得一提的是,有60%的患者达到CNS最佳疗效(即疾病稳定)。在具有靶病灶的患者中,15/23例患者的肿瘤直径之和减小(ORR为22%)。总体而言,HER3-DXd对EGFR突变NSCLC CNS转移具有持久的疗效。当前这项试验的分析结果进一步支持,系统性治疗对脑转移患者是可行的。
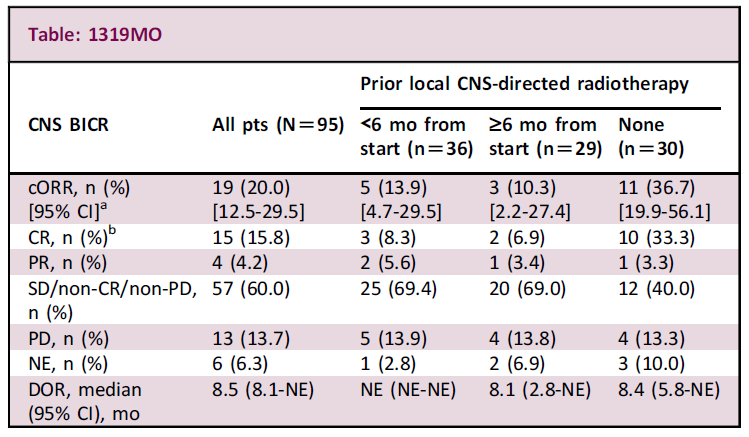
▲HER3-DXd疗效数据(图片来源:参考资料[4])
乳腺癌“明星药物”在转移性肺癌中疗效几何?
约有20%的HER2突变NSCLC患者在确诊转移时伴有脑转移。德曲妥珠单抗(T-DXd)是最具代表性和最受关注的新一代ADC之一,具有卓越的抗HER2疗效。研究摘要显示,T-DXd是“首个”针对HER2突变晚期NSCLC的靶向HER2疗法。本次ESMO大会报告了ESTINY-Lung(DL)-01、02研究中,T-DXd在基线有/无脑转移人群中的疗效和安全性的事后汇总分析。
分析评估了DL-01研究HER2突变队列(6.4 mg/kg;35例和56例),以及DL-02研究T-DXd 5.4 mg/kg(32例和70例)或6.4 mg/kg队列(19例和31例)有/无脑转移的患者,并汇总分析6.4mg/kg组。具有稳定基线脑转移的患者符合纳入条件。
总体而言,在接受T-DXd 5.4 mg/kg或6.4 mg/kg治疗的患者中,分别有31%和38%的患者具有基线可检测的脑转移。其中,分别有46.9%和55.6%为未经治脑转移。两剂量下的系统性ORR相似。
分析结果显示,两种剂量下患者的颅内ORR分别为25.0%(5.4mg/kg)和18.5%(6.4mg/kg),分别有4例和1例患者达到颅内完全缓解。在具有基线脑转移的患者中,两剂量下分别有13/32例和20/54例患者发生颅内进展;而在基线无脑转移的患者中,分别有1/70例和8/87例患者发生颅内进展。有或无脑转移患者的安全性结果大致相似,但有脑转移患者具有更高≥3级TEAE发生率的趋势。
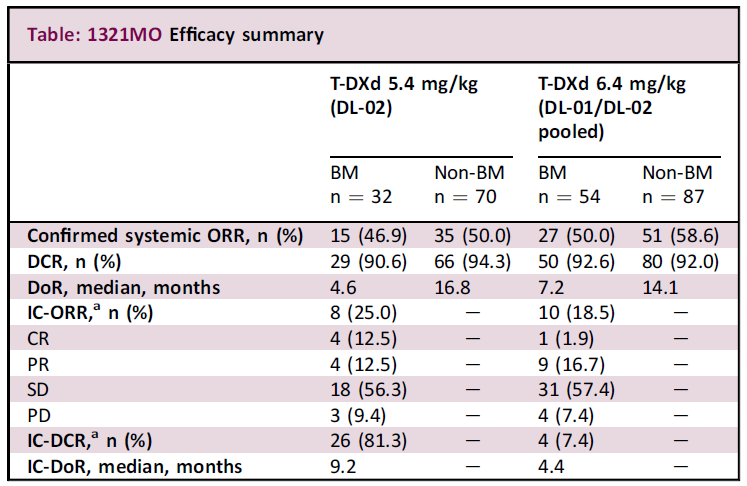
▲T-DXd疗效数据(图片来源:参考资料[5])
总体而言,T-DXd在HER2突变转移性NSCLC中具有可观的颅内疗效,一些患者甚至达到颅内完全缓解。此外,基线脑转移的存在并不影响T-DXd治疗的全身疗效。
参考资料
[1] L. Paz-Ares et al., TROPION-Lung05: Datopotamab deruxtecan (Dato-DXd) in previously treated non-small cell lung cancer (NSCLC) with actionable genomic alterations (AGAs). 2023 ESMO abstract 1314MO.
[2] L. Zhang et al., BL-B01D1, a first-in-class EGFRxHER3 bispecific antibodydrug conjugate, in patients with non-small cell lung cancer: Updated results from first-in-human phase I study. 2023 ESMO abstract 1316MO.
[3] J.K. Rotow1 et al., First-in-human study of ABBV-637, an EGFR-targeting BCLXLeinhibiting antibody-drug conjugate combined with osimertinib (OSI) in relapsed/refractory, EGFR-mutated non-small cell lung cancer (NSCLC). 2023 ESMO abstract 1318MO.
[4] M.L. Johnson et al., Intracranial efficacy of HER3-DXd in patients with previously treated advanced EGFR-mutated NSCLC: Results from HERTHENA-Lung01. 2023 ESMO abstract 1319MO.
[5] B.T. Li et al., Trastuzumab deruxtecan (T-DXd) in patients (pts) with HER2 (ERBB2)-mutant (HER2m) metastatic nonesmall cell lung cancer (NSCLC) with and without brain metastases (BMs): Pooled analyses from DESTINY-Lung01 and DESTINYLung02. 2023 ESMO abstract 1321MO.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言