Brain:南京大学生命科学学院通过体内自组装siRNA治疗Machado-Joseph病的神经病理学和炎症
2024-09-25 xiongjy MedSci原创 发表于上海
实验通过体内自组装的siRNA,将包裹siRNA的小胞外囊泡递送至大脑特定区域,有效抑制了致病蛋白mATXN3的表达,改善了YACMJD84.2转基因小鼠的运动功能,减少了小脑萎缩和神经炎症。
Machado-Joseph病(MJD),也称为脊髓小脑性共济失调3型(SCA3),是一种常染色体显性遗传的致命性共济失调,主要特征是小脑共济失调,原因是ATXN3基因的CAG重复扩展。目前,尚无有效的治疗方法。小干扰RNA(siRNA)作为一种潜在的治疗策略,可以特异性靶向致病的突变型ATXN3蛋白(mATXN3)。然而,由于大脑疾病的治疗难点是如何跨越血脑屏障,siRNA的递送效率仍然是其临床应用的主要障碍。

该研究提出了一种基于合成生物学的新策略,利用宿主肝脏作为组织载体,通过静脉注射合成构建体,使肝脏能够产生并分泌小胞外囊泡(sEV),这些囊泡内包裹了靶向mATXN3的siRNA。合成构建体由细胞巨细胞病毒(CMV)启动子驱动,编码突变型ATXN3-siRNA及一种靶向神经元的狂犬病毒糖蛋白(RVG)标签。在注射进入小鼠体内后,肝脏重编程产生自组装的siRNA,并通过内源循环系统将包裹有siRNA的sEV递送到小脑皮层和脊髓小脑束,在这些区域抑制ATXN3基因的表达。
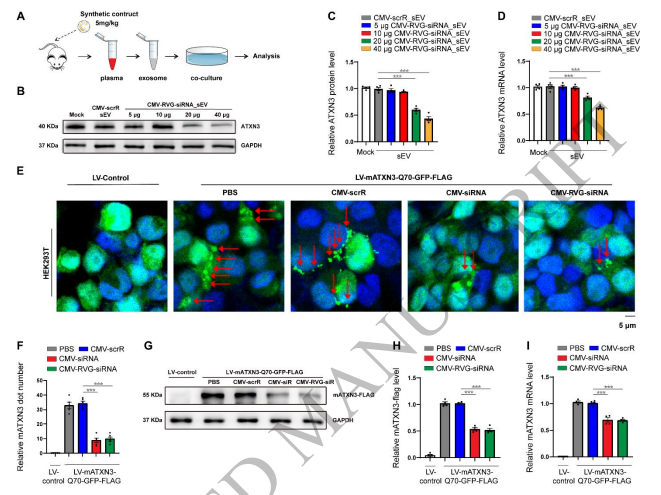
图1:用于评估 mATXN3-siRNA 活性的体外模型
研究的实验结果显示,在携带人类突变型ATXN3基因的YACMJD84.2转基因小鼠模型中,经过8至12周的治疗后,运动功能显著改善,小脑萎缩现象减少。此外,小脑皮层内的浦肯野细胞数量显著增加,髓鞘基本蛋白的丧失得到缓解,神经毒性核包涵体的数量和神经胶质纤维酸性蛋白(GFAP)的表达也显著减少。研究还表明,使用合成构建体产生的siRNA能够跨越血脑屏障,靶向大脑中的mATXN3基因,有效改善了共济失调小鼠的运动能力和神经病理学表型,缓解了神经炎症。进一步的试验结果显示,通过静脉注射合成构建体不仅可以成功递送siRNA至小脑皮层和脊髓小脑束,还显著抑制了病变蛋白mATXN3的表达。
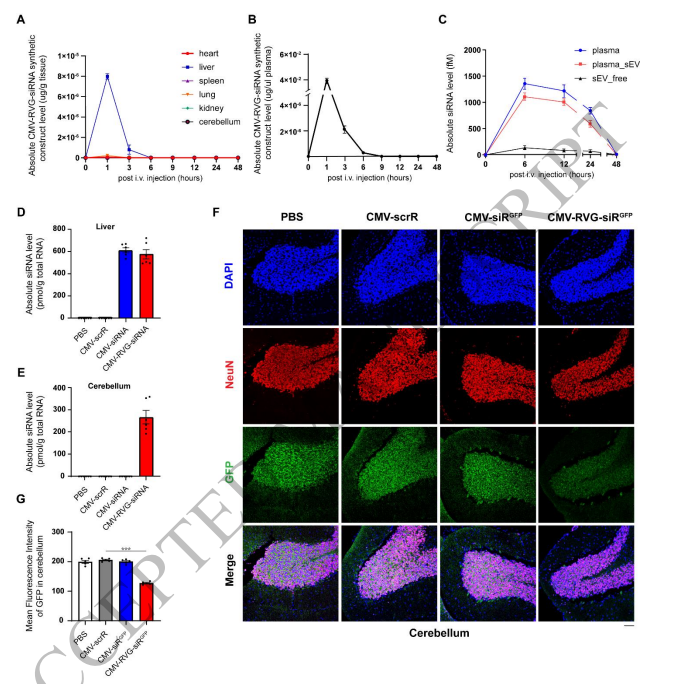
图2:体内监测自组装 siRNA 的输送过程
本研究提出的合成生物学策略成功解决了siRNA治疗小脑共济失调的主要挑战,展示了未来临床治疗的潜力。这一策略通过利用体内自组装siRNA系统,有效减轻了小脑萎缩和神经炎症,并恢复了运动功能,为治疗MJD提供了一个新的方向。未来的研究可以进一步优化这一策略,探索其对其他神经退行性疾病的应用潜力。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#合成生物学# #3型脊髓小脑性共济失调# #神经病理学#
57