难治性荨麻疹新“克星”!《柳叶刀》:治疗4周起效,12周症状显著改善!
2023-11-30 医学新视点 医学新视点 发表于上海
分析结果显示:与安慰剂组相比,中重度、临床难治性CSU患者接受ligelizumab治疗12周后,荨麻疹相关症状发生显著改善。
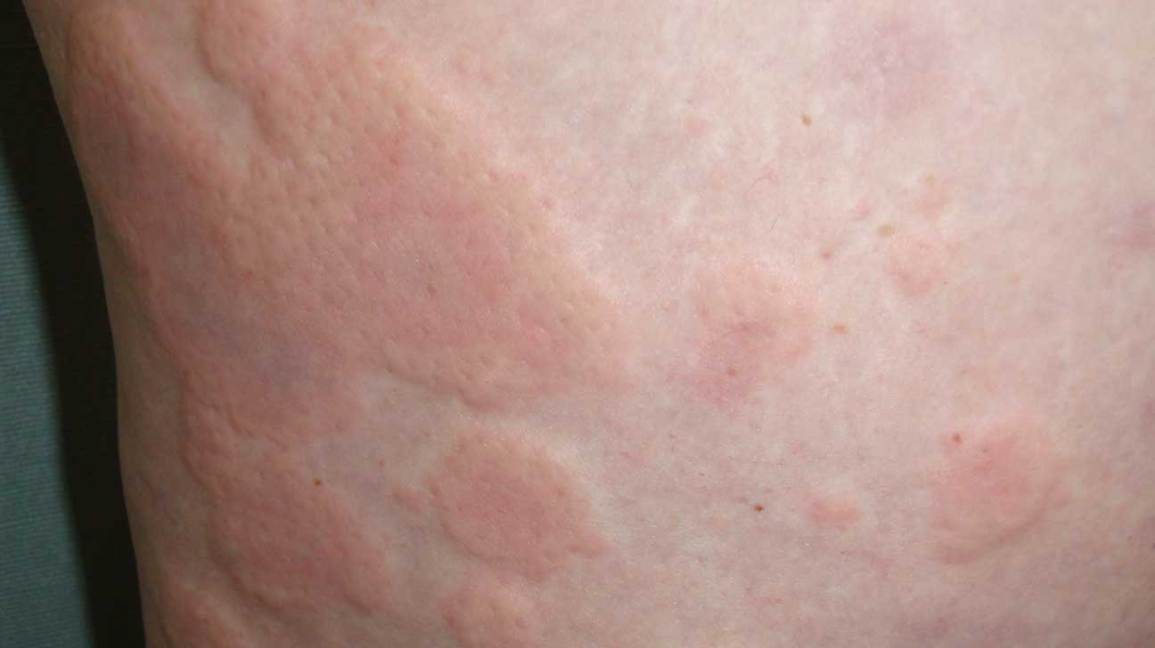
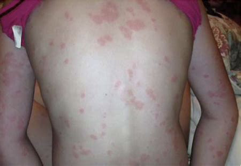
慢性自发性荨麻疹(CSU)是慢性荨麻疹中最常见的类型,其特征为在无特定外部触发因素的情况下发生瘙痒性荨麻疹、血管性水肿或两者均持续超过6周。在全球范围内,约有1%~2%的人群受到CSU的影响,且其中至少40%的个体发生了血管性水肿。CSU相关症状将对日常活动和睡眠产生不利影响,并对整体生活质量产生潜在负面影响。
近日,《柳叶刀》(THE LANCET)重磅发表两项3期随机对照试验(PEARL-1和PEARL-2)结果。分析结果显示:与安慰剂组相比,中重度、临床难治性CSU患者接受ligelizumab治疗12周后,荨麻疹相关症状发生显著改善。值得一提的是,研究中所有活性药物治疗组(包括ligelizumab治疗组)在第4周就已经显示出荨麻疹相关症状的改善。论文强调,PEARL系列研究为“在CSU患者中开展的规模最大的3期试验”。

截图来源:THE LANCET
根据中国及国际治疗指南,CSU的一线治疗为标准剂量的第二代非镇静H1抗组胺药(H1-AH);在标准剂量的H1-AH疗效不佳时(2周后症状持续存在),可在获得患者知情同意的情况下将原抗组胺药加至2~4倍剂量作为二线治疗;三线治疗包括生物制剂(奥马珠单抗)等。临床难治性CSU患者亟需更多有效治疗选择。
Ligelizumab是新一代、高亲和力、人源化单克隆抗免疫球蛋白(Ig)E抗体。临床前研究显示,与活性对照药物相比,ligelizumab很更好地抑制IgE与高亲和力IgE受体(FcεRI)的结合、嗜碱性粒细胞的活化以及B细胞介导的IgE的产生,并减少被动全身过敏反应。
PEARL-1和PEARL-2是设计相同的两项3期、随机、双盲、活性对照和安慰剂对照、平行组研究,旨在中重度、H1-AH难治性CSU患者(年龄≥12岁)中评估ligelizumab的疗效和安全性。其中,PEARL-1在28个国家的164家研究中心开展;PEARL-2在27个国家的183家研究中心开展。两项研究包含4周的筛选期、52周的治疗期和12周的后续随访期。
两项研究入组患者以3:3:3:1的比例被随机分配至72 mg ligelizumab、120 mg ligelizumab、300 mg奥马珠单抗或安慰剂组,每4周给药一次,共52周。其中,被分配至安慰剂组的患者从第24周开始接受120 mg ligelizumab治疗。研究的主要终点均为成人患者第12周时“每周荨麻疹活动评分(UAS7;0~42分,分值越高代表症状越严重)”相对基线的变化。
2018年10月17日~2021年9月30日,共有1072例患者(成人1034例;青少年38例)被纳入PEARL-1研究;2018年10月20日~2021年10月26日,共有1078例患者(成人1023例;青少年55例)被纳入PEARL-2研究。总体而言,两项研究的成人患者中女性占比72%。PEARL-1和PEARL-2中分别有879例和873例成人患者完成了52周的治疗期,各研究组基线时平均UAS7范围为29.37~31.0分。
分析结果显示,PEARL-1和PEARL-2研究均达到主要疗效终点,即接受ligelizumab治疗的患者第12周时UAS7相对基线的变化要优于安慰剂(p<0.0001),但不优于奥马珠单抗。具体而言:
-
PEARL-1研究中72 mg ligelizumab组和安慰剂组UAS7相对基线变化的差值为-8.0;PEARL-2研究中相应差值为-10.0;
-
PEARL-1研究中72 mg ligelizumab组和奥马珠单抗组患者UAS7相对基线变化的差值为0.7;PEARL-2研究中相应差值为0.4;
-
PEARL-1研究中120 mg ligelizumab组和安慰剂组UAS7相对基线变化的差值为-8.0;PEARL-2研究中相应差值为-11.1;
-
PEARL-1研究中120 mg ligelizumab组和奥马珠单抗组UAS7相对基线变化的差值为0.7;PEARL-2研究中相应差值为-0.7;
-
汇总数据显示,两项研究中,接受两种剂量ligelizumab治疗的患者第12周时UAS7相对基线的变化要优于安慰剂(p<0.0001),但与奥马珠单抗组患者的变化趋势相似。其中,72 mg ligelizumab组与奥马珠单抗组患者的治疗差异为0.51(p=0.78);120 mg ligelizumab组与奥马珠单抗组患者的治疗差异为-0.004(p=0.50)。
此外,分析还发现,与安慰剂组相比,不同剂量ligelizumab组第12周时实现荨麻疹完全缓解(即UAS7=0)、瘙痒症状缓解、血管性水肿症状完全缓解、生活质量显著改善的患者比例更高。
值得关注的是,活性药物治疗组(包括ligelizumab治疗)约三分之一的患者达到关键次要终点,即在第12周时实现荨麻疹完全缓解,而安慰剂组患者实现荨麻疹完全缓解的比例仅为8%。安全性方面,两项研究均未发现ligelizumab或奥马珠单抗新的安全性信号。
总之,两项3期关键性试验(PEARL-1和PEARL-2)的分析结果表明,中重度、临床难治性CSU患者接受不同剂量(72 mg或120 mg)的ligelizumab治疗,第12周时荨麻疹相关症状的改善情况要显著优于安慰剂治疗。
论文强调,这两项大型、多中心3期研究的结果进一步确立了IgE在CSU发病机制中的核心作用,并进一步支持将抗IgE作为H1-AH难治性CSU患者的主要治疗策略。
参考资料
[1] Marcus Maurer et al., Efficacy and safety of ligelizumab in adults and adolescents with chronic spontaneous urticaria: results of two phase 3 randomised controlled trials. THE LANCET. Doi: 10.1016/S0140-6736(23)01684-7
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











受益良多,谢谢分享
132
#慢性自发性荨麻疹# #Ligelizumab# #单克隆抗免疫球蛋白#
144