Nature:这些年,挂在审批路上的药物
2016-11-26 佚名 制药在线
了解临床试验失败的原因对于药物发展是至关重要的。近期,《自然》杂志刊登了Clarivate Analytics公司的首席科学家Richard K. Harrison对过去三年内在临床Ⅱ期和Ⅲ期止步的药物案例的分析结果。在过去三年内(2013-2015),从临床Ⅱ期到审批通过之间共有218个被报道的失败案例,其中174案例有明确的失败原因。了解临床试验失败的原因对于药物发展是至关重要的。近期,《自然
了解临床试验失败的原因对于药物发展是至关重要的。近期,《自然》杂志刊登了Clarivate Analytics公司的首席科学家Richard K. Harrison对过去三年内在临床Ⅱ期和Ⅲ期止步的药物案例的分析结果。在过去三年内(2013-2015),从临床Ⅱ期到审批通过之间共有218个被报道的失败案例,其中174案例有明确的失败原因。
了解临床试验失败的原因对于药物发展是至关重要的。近期,《自然》杂志刊登了Clarivate Analytics公司的首席科学家Richard K. Harrison对过去三年内在临床Ⅱ期和Ⅲ期止步的药物案例的分析结果。在过去三年内(2013-2015),从临床Ⅱ期到审批通过之间共有218个被报道的失败案例,其中174案例有明确的失败原因。
临床试验失败原因的分析
大多数药物的临床试验由于缺乏疗效(52%)或安全性(24%)而被中止,也有一些药物由于战略(15%)、商业(6%)和操作(3%)等各种原因而被放弃,如图1a。Richard对这些药物所属领域也做了分析,其中抗肿瘤领域的临床试验中止率最高(32%),其余的中枢神经系统疾病领域(17%)、肌肉骨骼类疾病领域(13%)、心血管疾病领域(7%)、消化系统类疾病领域(7%)、代谢类疾病领域(6%)以及传染性疾病领域(5%),如图1b。
相对于其他领域,抗肿瘤领域和中枢神经系统领域较高的临床试验中止率一定程度上也反映了临床试验数量的庞大。有数据表明,在2013年至2015年期间,抗肿瘤领域和中枢神经系统领域的临床Ⅱ期和Ⅲ期试验数量分别为5821项和2796项,几乎等于或仅仅略小于同时段其他领域临床试验数量之和。这两个领域较高的临床试验中止率也恰好反映了疾病的复杂和多变性。
Richard对临床试验发展过程中的数据进行分析发现,如图1c,d,临床Ⅱ期试验的失败主要原因为缺乏有效性(48%)或安全性(25%),或者两者兼具。同样的,有效性的缺乏也是临床Ⅲ期试验失败的首要原因,其次是安全性的缺乏,约占比例14%。虽然后期临床试验中由于安全性缺乏而被中止的比例有所减少,但对于医药企业来说,这种失败来的晚不如来得早。事实上,临床Ⅲ期中由于缺乏有效性而被中止的案例数量已经减少了,但这并不能从所占比例上反映出来。
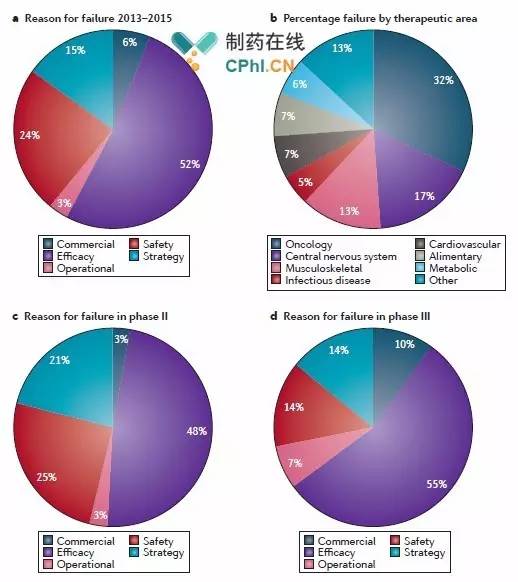
图1 2013-2015年间临床试验终止率分析
战略上的调整导致新药申请被中止的原因不外乎两种,发展方向的调整或企业间的并购,这两种原因所导致的试验中止率在临床Ⅱ期和Ⅲ期分别为21%和14%。这也从另一个方面反映了在医药行业内企业并购案例的增加。有数据显示,在过去4年中,医药行业的企业并购案数量由2012年的248次增加到了2015年的468次,增长了近1倍。也可以这样理解,并购企业越多,就会有越多重复或竞争的项目,这就迫使并购后的企业不得不放弃或对发展领域和方向做出调整。
此外,由于经济原因而被迫中止的案例在临床Ⅱ期占3%,而在临床Ⅲ期占比10%,这表明,临床Ⅱ期较低的经济投入降低了商业风险,而临床Ⅲ期的经济基础需求增大后使企业做出了更严格的效益成本分析。
Richard的团队将2013-2015年的数据与之前相同时期(2008-2010,2011-2012)的数据作对比,以分析临床领域和药物发展阶段的影响趋势。每一领域的临床试验失败率都随时间而发生改变,如图2a。抗肿瘤领域自始至终都占有最大的临床试验中止率,且其中止率由2008-2010年的23%增长到了2013-2015年的32%。消化疾病领域的临床试验中止率降低比率最大,由2008-2010年的18%降低至2013-2015年的7%。
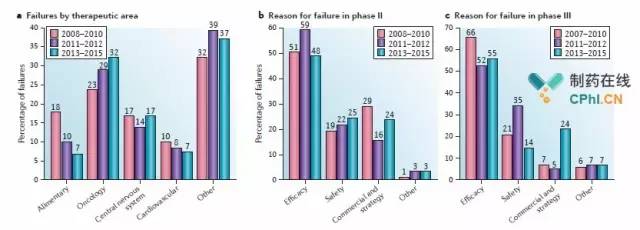
图2 不同时期药物临床试验终止率的对比及分析
回顾药物临床试验的历史发展趋势,药物有效性的缺乏一直都是临床Ⅱ期和Ⅲ期的终止原因,如图2b,c,这也解释了为何每一时期由该原因所导致的终止率都达到近一半。将2008-2010年与2013-2015年对比可发现,临床Ⅲ期由于药物有效性的缺乏而导致的终止案例比率下降了11%,由于安全性的缺乏而导致的终止比率下降了7%,与此同时,由于经济原因和战略调整而导致的试验终止率由7%增长到了24%。
总结与观望
Richard以及他的团队经过对数据的分析,观察到了过去7年间临床Ⅱ期和Ⅲ期试验终止原因的变化频率。药物有效性的缺乏仍是试验终止的最大原因,但这或许有望通过试验人群的增多、选择合适的生物标记物、深入理解疾病的生理学以及改善目标人群的筛选来改善这一现状。尽管由于安全性的缺乏而导致试验终止的比率在临床Ⅱ期增加,在临床Ⅲ期降低,这说明在开发周期的早期消除不安全因素的方法是奏效的。
在2010-2012年间,来自于40家大中型医药企业的药物中,只有20%进入到了临床Ⅱ期和临床Ⅲ期,而在2013-2015年期间,这个比例增长到了25%。由临床Ⅲ期成功进入到下一阶段的比率由2010-2012年间的55%增长到了2013-2015年间的58%,略有增长。在最后的监管审查阶段,成功率由2010-2012年间的84%增长到了2013-2015年的91%。总的来说,这样的趋势能够给制药行业和病人以鼓励。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Nat#
105
大多数药物的临床试验由于缺乏疗效(52%)或安全性(24%)而被中止,也有一些药物由于战略(15%)、商业(6%)和操作(3%)等各种原因而被放弃
123
涨知识了
119
药物临床试验任重道远。
75