【JCO】屡败屡战:罗米地辛+CHOP治疗初治PTCL的III期研究阴性结果及评述
2024-04-01 聊聊血液 聊聊血液 发表于陕西省
《Journal of Clinical Oncology》近日更新了Ro-CHOP III期研究随访6年的最终分析结果,Ro-CHOP 与 CHOP 治疗成人 PTCL 患者的结局无差异。
外周 T 细胞淋巴瘤 (PTCL) 是一组罕见但极具异质性的血液恶性肿瘤,呈侵袭性且预后不良。其标准一线治疗策略借鉴其他侵袭性淋巴瘤,但侵袭性 B 细胞淋巴瘤方案(即以蒽环类药物为基础的多药方案,包括CHOP)治疗T 细胞淋巴瘤的疗效不佳,约70%的 PTCL 患者在一线治疗后发生复发性或难治性疾病。通过“加用”或“替代”蒽环类药物改善结局的尝试也失败,大多数 T 细胞淋巴瘤存在困难且未满足的医学挑战。
Ro-CHOP研究及其更新
鉴于HDAC抑制剂罗米地辛(Romidepsin)治疗复发/难治性PTCL的初步疗效,2013年法国淋巴瘤研究协会(LYSA)启动一项罗米地辛联合CHOP方案对比标准CHOP治疗一线外周T细胞淋巴瘤(PTCL)的Ro-CHOP III期研究,中位随访27.5个月的初步结果于2022年发表于《Journal of Clinical Oncology》,证实Ro-CHOP联合方案较CHOP未改善PFS、缓解率或OS,但增加≥3级治疗相关TEAE。虽然归咎于Ro-CHOP方案的高TEAE 发生率(93.8 vs 69.7%),可能限制了基石CHOP的强度,但总体而言,Ro-CHOP在既往未经治疗的 PTCL 患者中未显示出获益。
《Journal of Clinical Oncology》近日更新了Ro-CHOP III期研究随访6年的最终分析结果,Ro-CHOP 与 CHOP 治疗成人 PTCL 患者的结局无差异。但探索性分析表明,滤泡辅助性T细胞(TFH)淋巴瘤患者有一定获益(Ro-CHOP与CHOP组的中位PFS分别为19.5和10.6个月,P=0.039),但OS无差异(P=0.342)。
此外事后分析表明,患者二线治疗效果不佳(中位PFS2仅3.3个月,中位OS2仅11.5个月),但BV联合方案二线治疗具有潜在获益(含BV方案对比不含BV方案:中位PFS2分别为8.6和2.8个月,P=0.002;中位OS2有优化的趋势,分别为22.9和11.5个月,P=0.082)。

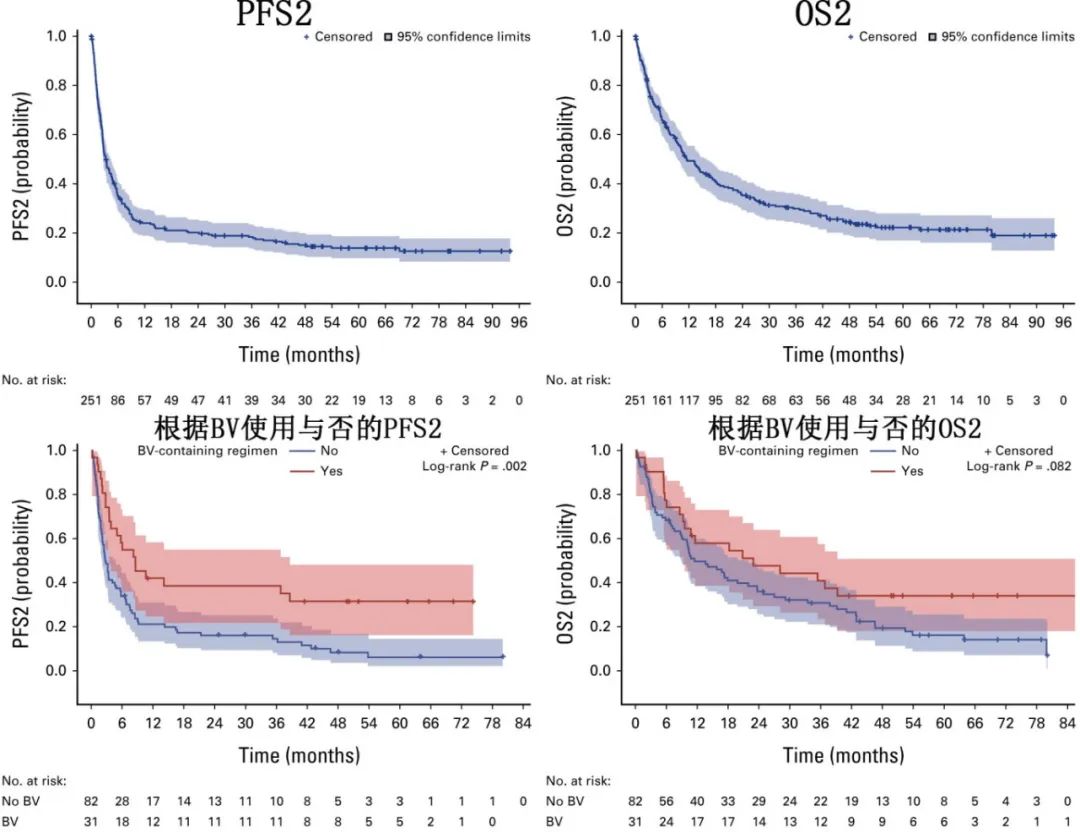
虽然Ro-CHOP 与 CHOP的PFS和OS无差异,但事后分析中分为TFH表型和非TFH表型进行分析,结果TFH表型中Ro-CHOP组的PFS接近翻番(19.5个月vs 10.6个月,HR=0.703,p=0.0395)。
上述事后分析是建立在对TFH淋巴瘤独特生物学的日益认识的基础上,其特征包括参与染色质修饰和微环境的基因突变,如TET2、RHOA、DNMT3A和IDH2,且经常在克隆性造血背景下发生。因此TFH淋巴瘤对表观遗传学治疗(包括罗米地辛)的疗效更好,这也得到多个研究的证实。但应注意,在启动Ro-CHOP研究(2013年)之前还并不知道这一点。
将这一结果与另一项大型前瞻性随机研究ECHELON-2进行比较,后者表明在表达CD30的PTCL患者中,BV-CHP与CHOP相比可改善PFS和OS,且间变性大细胞淋巴瘤亚型最可能从BV中获益,从而开启了PTCL基于亚型的治疗时代;且加用BV并未像Ro-CHOP研究那样降低化疗剂量强度。BV是一种新的标准治疗,对部分PTCL患者具有较高的治愈率。
该研究的经验教训
一.T细胞淋巴瘤中化疗的治愈率可能高于一般认知。一般认为一线化疗治疗PTCL长期生存率较低,未经治疗的患者应尝试无化疗方案。但近期大型前瞻性研究发现CHOP化疗治愈率较高。例如在RoCHOP研究中,单纯CHOP治疗的患者中位生存期为50.4个月;在ECHELON-2研究的CHOP组中,5年PFS和OS分别为43%和61%,表明有相当数量的患者可通过有限期化疗治愈,化疗仍是可以考虑的基础平台。
二.不仅要了解该罕见疾病的异质性,还要将异质性纳入试验设计。如上所述,HDAC抑制剂和BV显示出亚型特异性的疗效,且使用其他新型靶向药治疗复发/难治性PTCL时也观察到生物学驱动和组织学特异性疗效(下表)。
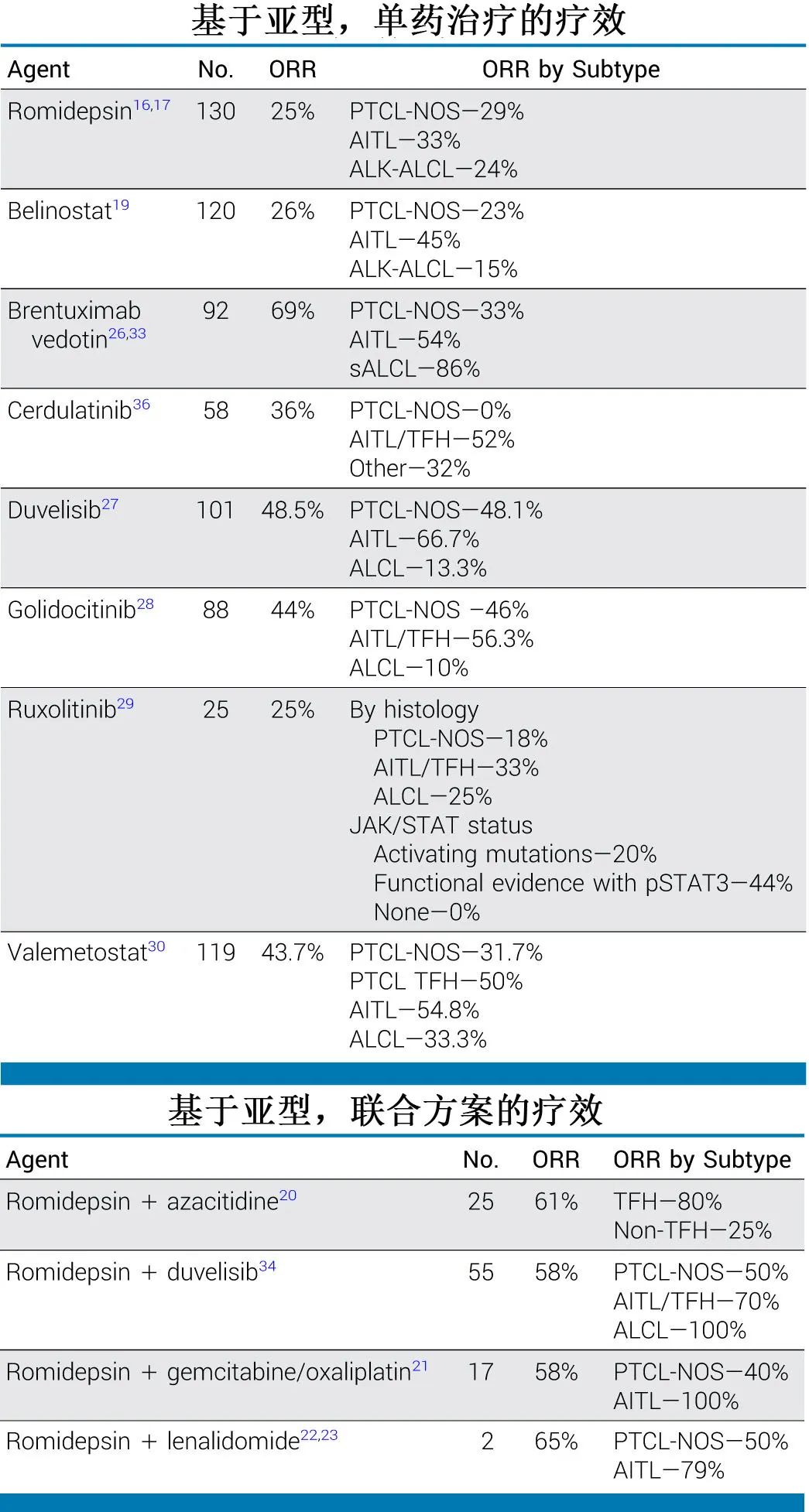
即使在近期随机研究的标准CHOP组,结局也因组织学类型而异:ALCL的治愈率高于AITL,而AITL的治愈率高于PTCL-NOS(下表)。

根据经验,某些罕见的PTCL亚型(如成人T细胞白血病/淋巴瘤和肝脾T细胞淋巴瘤)很少单纯通过化疗治愈,需要使用其他方案。在更常见的PTCL亚型中,p53、CDKN2A、DNMT3A异常、TP63重排以及与GATA-3亚型一致的表达模式似乎可识别出不太可能从化疗中获益的人群,而DUSP22重排和TBX21亚型可能对化疗更敏感。这些结果尚未影响治疗,但在研究基于化疗的新方案时需要在研究设计和解读中认识并考虑这些预测因素。
三.罕见疾病可能没有第二次治疗机会。由于事后分析具有获益,前瞻性评估Ro-CHOP 治疗TFH淋巴瘤应该也是可行的;即使没有预先计划,AITL患者几乎占入组的一半,仍有足够的效力。如果是前瞻性分析,则该研究结果可能是阳性的,TFH淋巴瘤也就有了新的标准一线方案,使得大多数患者在5年时存活。然而,该研究的阴性结果导致其PTCL 适应症撤回,从而影响了其用于复发性 PTCL 的可及性,并阻碍了未来的临床试验。罗米地辛目前未纳入一线治疗,但探索其他 HDAC 抑制剂联合其他新药的研究正在进行中。
罕见病试验的成本和后勤问题,导致开展亚型特异性或亚型富集的随机研究比较困难。如果试验组使用过于乐观的目标,或对照组使用过于悲观的预测,则其研究功效不足,不太可能推动该领域的发展。同样,如果试验不完善患者人群或未预先计划亚组分析,则也不太可能推动该领域的发展。未来的随机研究应丰富最具生物学和临床意义的亚型,尽可能前瞻性的为特定队列提供效力。
失败是成功之母
一刀切的方法不可能改变 PTCL 的治疗,但随着多种有希望的药物正在 T 细胞淋巴瘤中开发,应进一步探索亚型特异性疗效,以富集可以获益的患者,并尽量减少不会获益的患者。简单地理解异质性还不够,还必须同时将这些知识(尽管尚不完善)应用于未来的研究设计,通过利用 PTCL 特定子集的脆弱性,可以进一步优化治疗。将患者人群作为验证性研究的重点,必须研究者、行业、监管机构和患者之间通力合作,并且这是“自古华山一条路”。
参考文献
1. Camus V,et al. Romidepsin plus cyclophosphamide, doxorubicin, vincristine, and prednisone versus cyclophosphamide, doxorubicin, vincristine, and prednisone in patients with previously untreated peripheral T-cell lymphoma: Final analysis of the Ro-CHOP trial.J Clin Oncol . 2024 Feb 16:JCO2301687. doi: 10.1200/JCO.23.01687.
2. Mehta-Shah N,et al.Failing Forward in Peripheral T-Cell Lymphoma.J Clin Oncol . 2024 Mar 26:JCO2302658. doi: 10.1200/JCO.23.02658.
3. Luan, Y., Li, X., Luan, Y. et al. Therapeutic challenges in peripheral T-cell lymphoma. Mol Cancer 23, 2 (2024). https://doi.org/10.1186/s12943-023-01904-w
4. Bachy E, Camus V, Thieblemont C, et al: Romidepsin plus CHOP versus CHOP in patients with previously untreated peripheral T-cell lymphoma: Results of the Ro-CHOP phase III study (conducted by LYSA). J Clin Oncol 40:242-251, 2022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#PTCL# #罗米地辛# #CHOP治疗#
34