论文解读| Guixue Wang/ Juhui Qiu教授团队揭示内皮细胞在动脉粥样硬化中吞噬凋亡细胞碎片的新角色
14小时前 Genes and Diseases Genes and Diseases 发表于陕西省
本研究通过单细胞和批量RNA测序分析,揭示了内皮细胞在动脉粥样硬化中吞噬凋亡细胞碎片的新机制。
动脉粥样硬化是一种慢性炎症性疾病,其主要特征是脂质在血管壁内膜下的沉积,这最终导致血管狭窄、血栓形成和器官损伤。在这一过程中,血管内皮细胞的功能障碍和细胞死亡扮演着重要角色。尽管巨噬细胞等专职吞噬细胞在清除凋亡细胞和细胞碎片方面发挥着关键作用,但在晚期动脉粥样硬化斑块中,凋亡细胞的过度积累和坏死核心的形成表明清除机制不足。
重庆大学的Guixue Wang/ Juhui Qiu教授团队在本刊发表题为“Coupled single-cell and bulk RNA-seq analysis reveals the engulfment role of endothelial cells in atherosclerosis”的研究论文,通过单细胞和批量RNA测序分析,揭示了内皮细胞在动脉粥样硬化中吞噬凋亡细胞碎片的新机制。
1、内皮细胞吞噬凋亡细胞碎片
研究人员首先在人主动脉和 Apoe-/-小鼠动脉粥样硬化斑块中发现,TUNEL标记的凋亡细胞碎片定位于Pecam1+内皮细胞内,表明内皮细胞具有吞噬细胞碎片的能力(图1A、B)。
2、内皮细胞亚群的异质性
通过对Apoe-/-小鼠主动脉进行单细胞RNA测序,研究人员发现内皮细胞分为2个不同的亚群,其中一个亚群与血管损伤相关通路(如细胞外结构组织、内皮细胞迁移、伤口反应和伤口愈合)显著相关,表明内皮细胞在动脉粥样硬化中存在表型转换(图1C–F)。
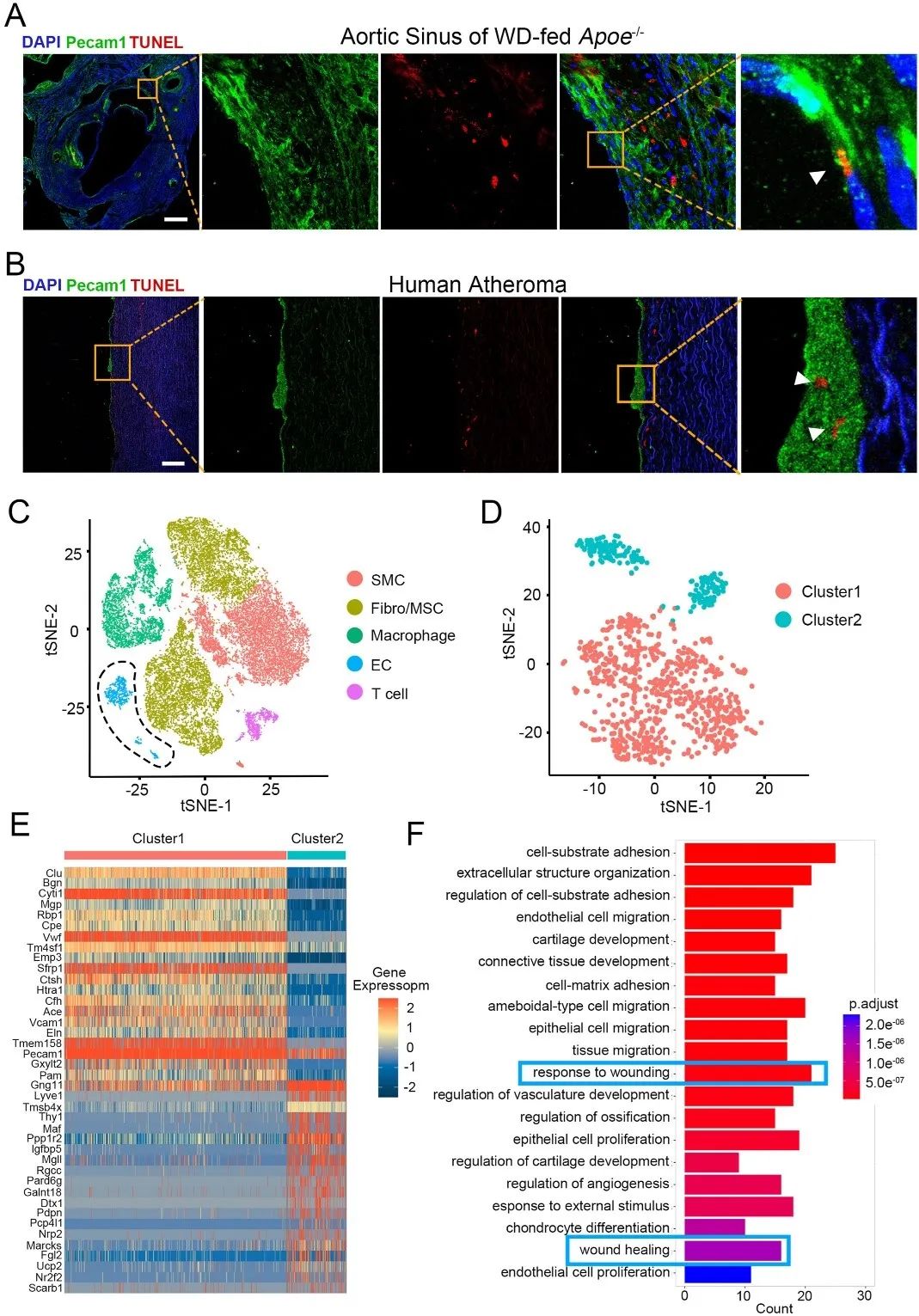
图1 通过单细胞RNA测序发现,动脉粥样硬化主动脉中的内皮细胞吞噬凋亡细胞碎片表现出独特的特征(原文中Figure 1)
3、SR-B1与吞噬功能相关
研究团队进一步分析了3个血管损伤相关RNA-seq数据集,发现清道夫受体B类1型(SR-B1)可能在内皮细胞吞噬中发挥重要作用。单细胞RNA-seq和批量RNA-seq均表明,SR-B1在小鼠主动脉的一个独特内皮细胞亚群中高表达,并与细胞粘附连接和细胞骨架的重组密切相关,这对于吞噬功能是必要的(图2)。
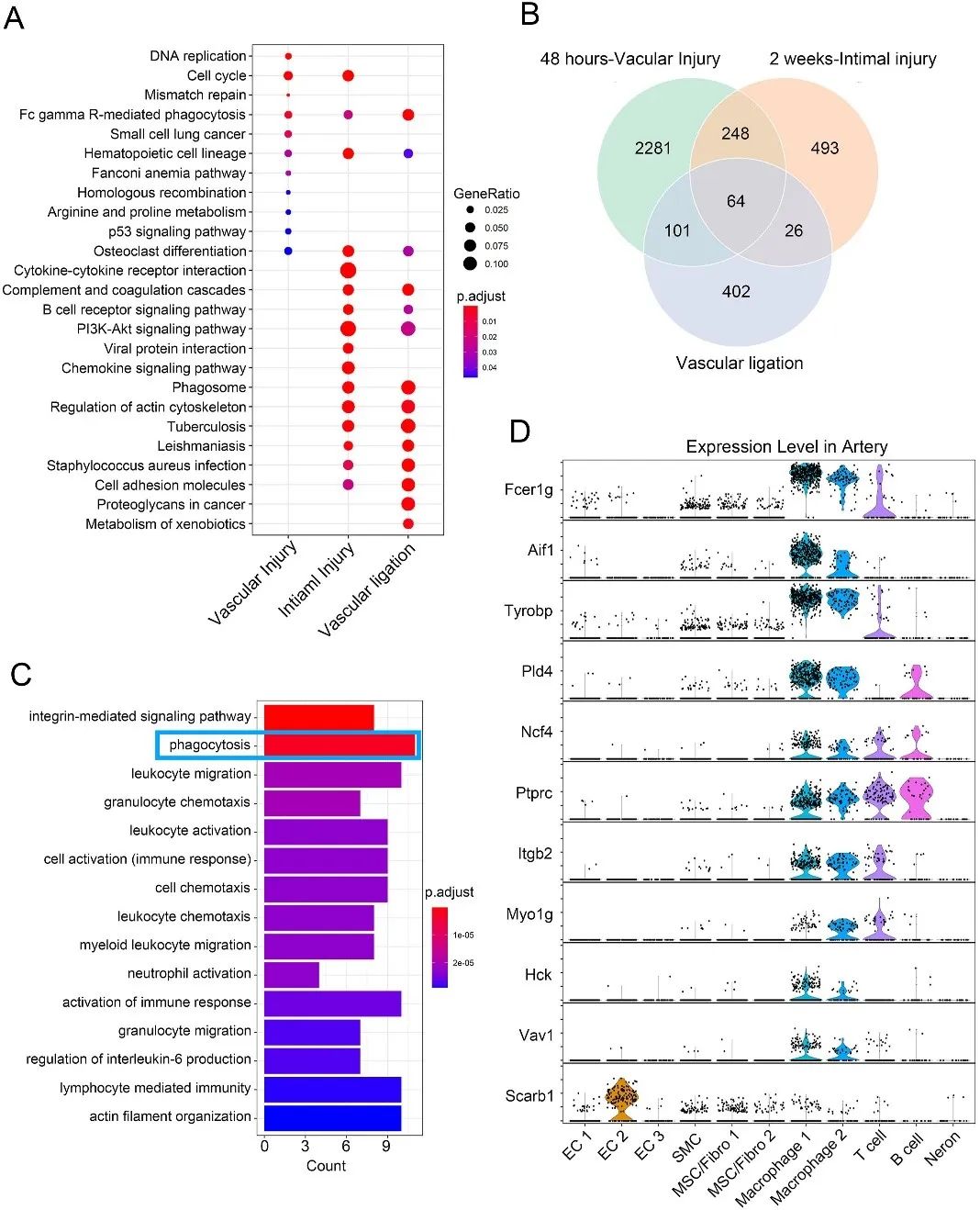
图2 SR-B1在受损的血管细胞中表达增加,并与主动脉内皮细胞共定位(原文中Figure 3)
3、SR-B1对内皮细胞吞噬凋亡细胞碎片至关重要
使用SR-B1的选择性抑制剂BLT-1抑制SR-B1依赖的选择性吞噬作用,发现内皮细胞通过SR-B1介导细胞碎片的吞噬(图3),SR-B1对于内皮细胞在小鼠和人类主动脉动脉粥样硬化斑块中吞噬凋亡细胞碎片至关重要。
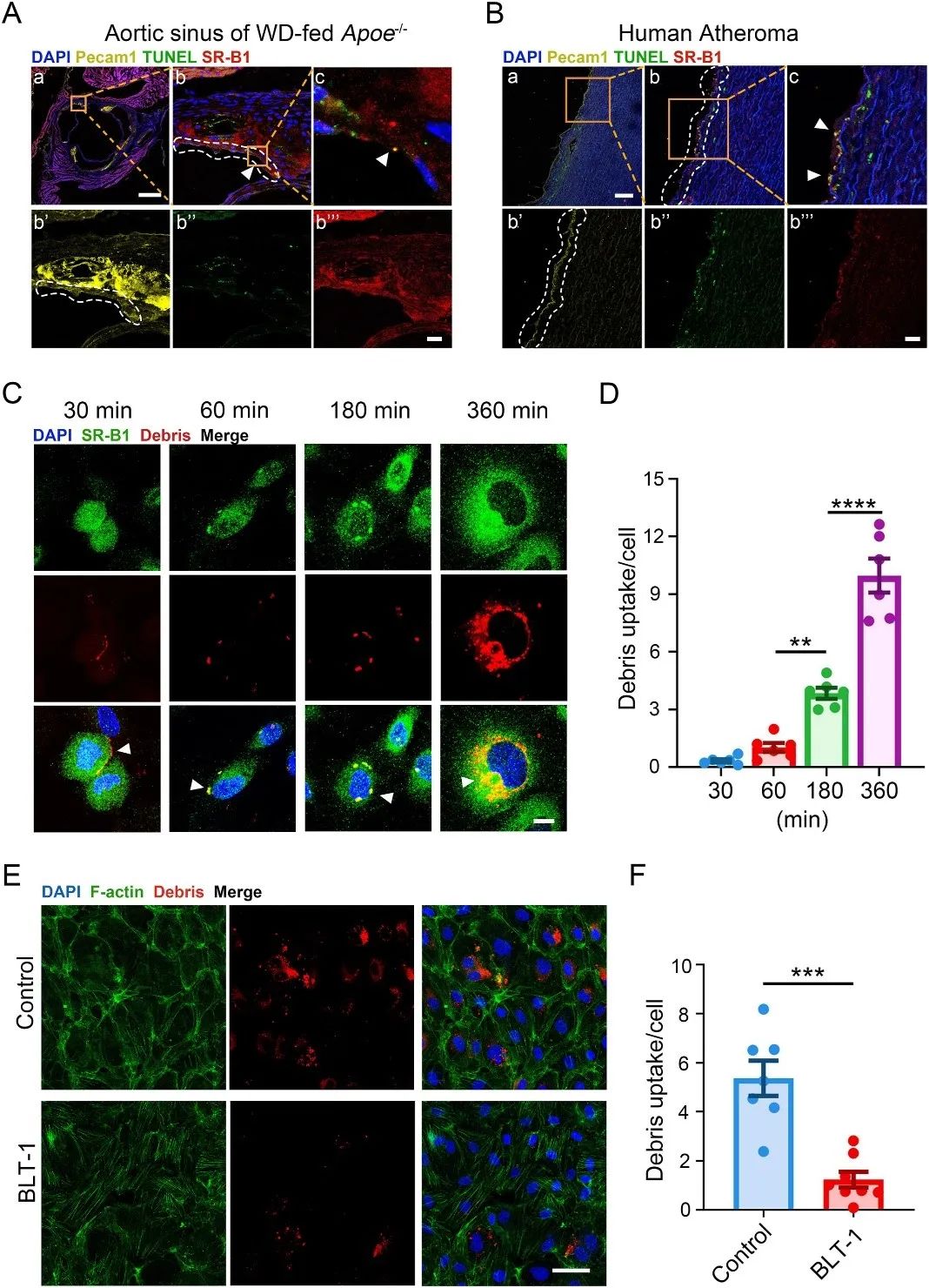
图3 SR-B1 促进血管内皮细胞吞噬凋亡细胞碎片(原文中Figure 6)
综上所述,该研究首次揭示了内皮细胞在动脉粥样硬化中作为非专业吞噬细胞吞噬凋亡细胞碎片的能力,并鉴定了SR-B1作为介导这一过程的关键受体。此外,该研究还发现内皮细胞吞噬和处理细胞碎片导致与细胞粘附连接和细胞骨架重组相关的一系列事件。这些发现为理解动脉粥样硬化中凋亡细胞清除的机制提供了新的视角,并可能为开发新的治疗策略提供靶点。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304224000473
引用这篇文章:
Xu J, Wang J, Zhang H, et al. Coupled single-cell and bulk RNA-seq analysis reveals the engulfment role of endothelial cells in atherosclerosis. Genes Dis. 2024;11(5):101250.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#动脉粥样硬化# #内皮细胞#
4