AJRCCM:大鼠肺动脉高压模型的单细胞测序研究新发现
2021-10-31 刘少飞 MedSci原创
鉴于在 PAH 动物模型中测试的许多新疗法尚未转化为床边,需要更全面地了解这些模型的细胞和分子景观,以阐明机制见解并增强临床前工作预测药物疗效的能力在人类。
Single-cell Study of Two Rat Models of Pulmonary Arterial Hypertension Reveals Connections to Human Pathobiology and Drug Repositioning.
两种大鼠肺动脉高压模型的单细胞研究揭示了与人类病理生物学和药物重新定位的联系
通讯作者:Jason Hong, M.D. 导师:Prof. Xia Yang.
Division of Pulmonary and Critical Care Medicine
David Geffen School of Medicine at UCLA
200 UCLA Medical Plaza, Suite 365-B, Box 951693
Los Angeles, CA 90095
尽管肺动脉高压 (PAH) 的管理取得了进展,但它仍然是一种无法治愈的进行性疾病,其特征是严重的肺血管重构、生活质量差和长期预后不佳。值得注意的是,目前的疗法侧重于缓解症状,并不能逆转血管重塑,这是 PAH 的关键病理特征。缺乏针对 PAH 潜在机制的疗法可能部分是因为我们对致病细胞类型及其特定分子途径的了解有限。人们越来越认识到,除了肺血管细胞外,肺中的其他细胞类型,包括各种免疫细胞群,也可能在 PAH 和其他肺部疾病中发挥重要作用。然而,据我们所知,尚未在最广泛使用的 PAH 临床前模型,即野百合碱 (MCT) 和 Sugen 缺氧 (SuHx) 大鼠模型中进行系统比较这些不同细胞类型的综合评估。
对常用的肺动脉高压(PAH)模型的细胞和分子以及转录组了解甚少。单细胞转录组学可以增强对临床前模型的分子理解,并促进其合理使用和解释。本研究的目的是确定PAH大鼠模型的肺中失调的基因,信号通路和细胞类型并对其进行优先排序,以评估与人PAH的相关性并确定候选药物的位置。
研究方法:在MCT,Sugen-hypoxia和对照大鼠的肺组织进行单细胞RNA-seq,以鉴定改变的基因和细胞类型,然后使用流分选细胞,RNA原位杂交和免疫荧光进行验证。通过从患者肺部组织学以及与人类PAH遗传基因和已知疾病基因的整合来评估与人类PAH的相关性。使用Connectivity Map预测候选药物。
研究结果:
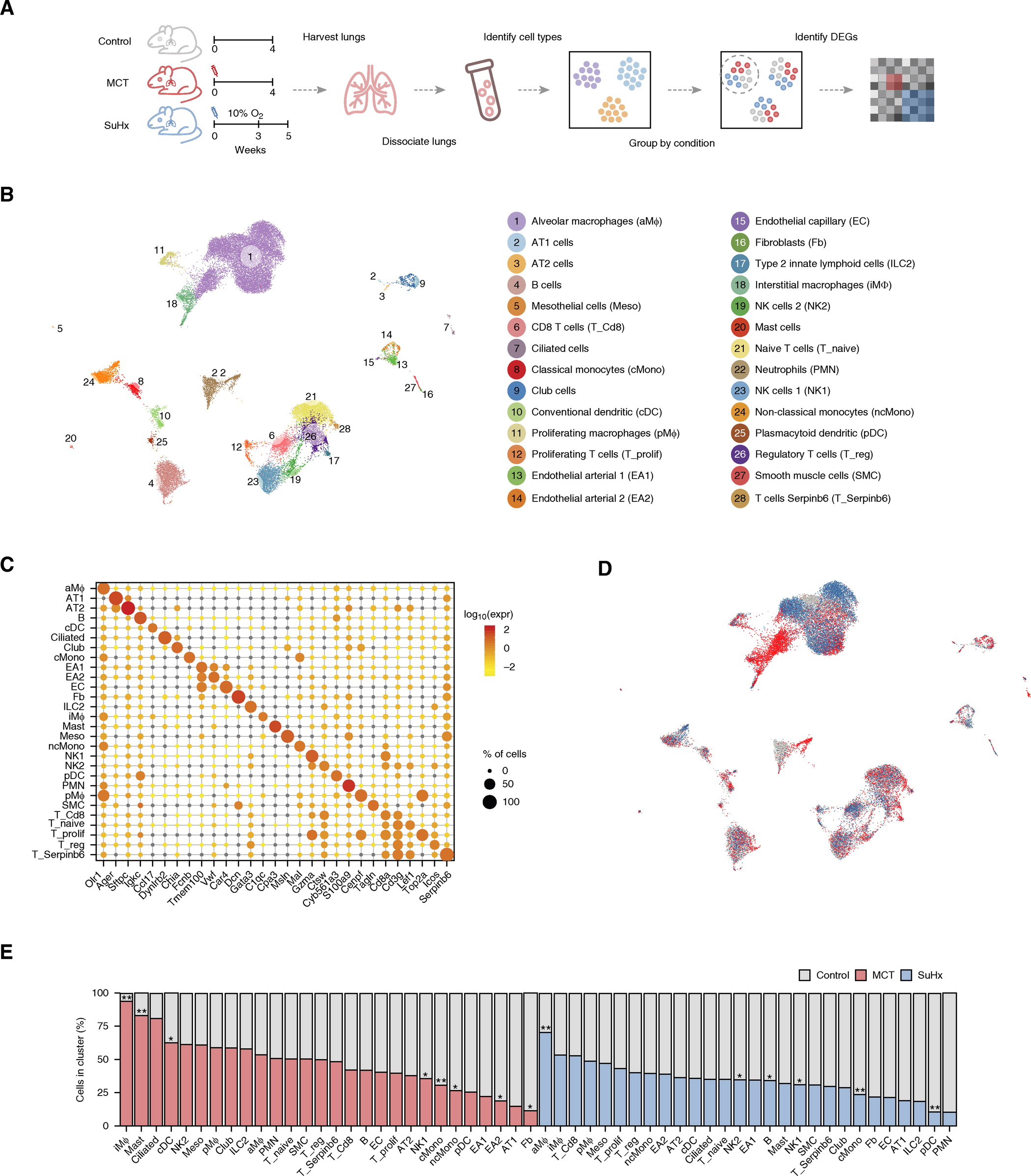
1.scRNA-seq可鉴定大鼠肺中的多种细胞群以及揭示具有细胞类型特异性的信号通路
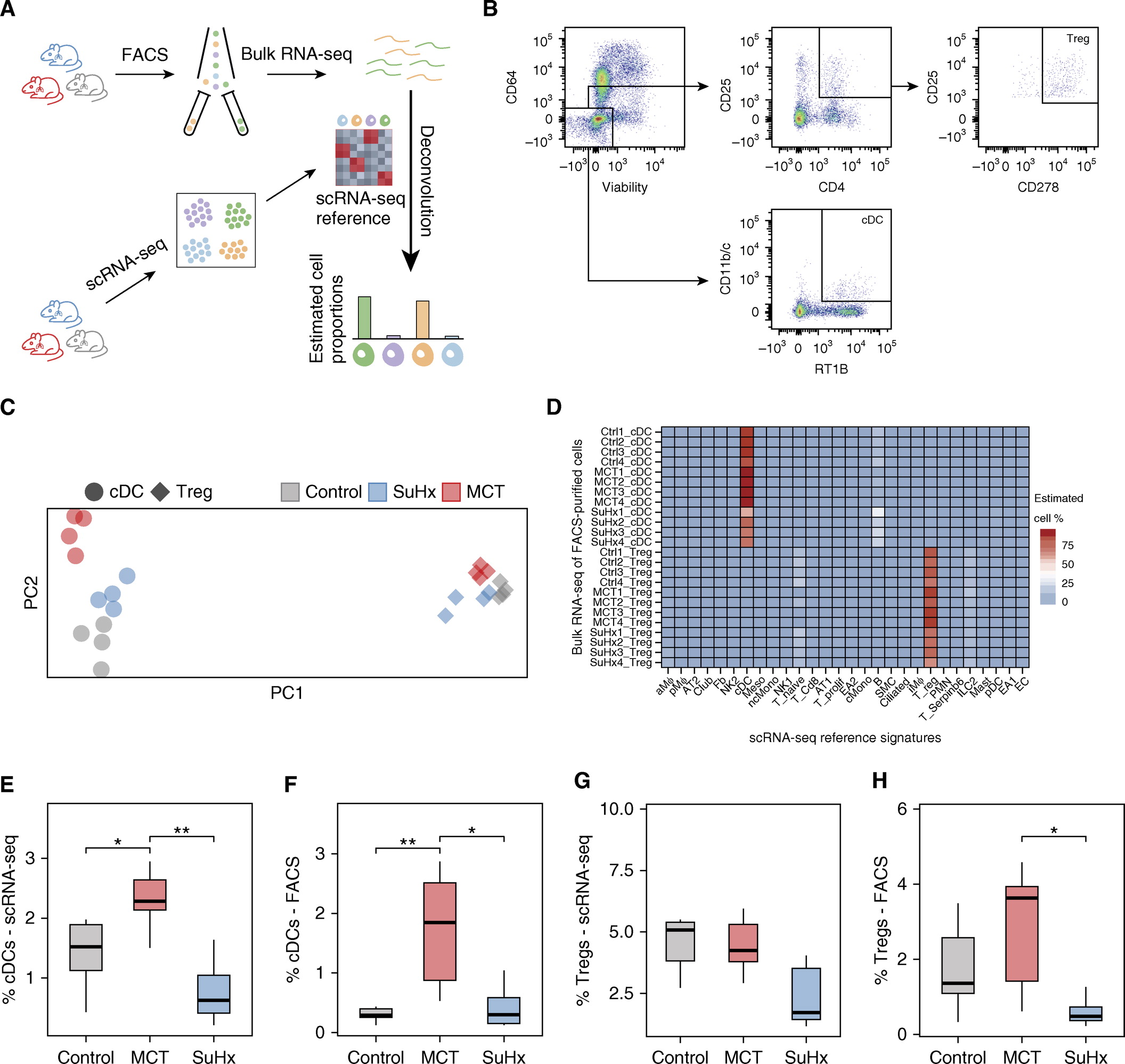
2.流式细胞分选及RNA-seq验证scRNA-seq细胞类型的特征和细胞比例。
3.scRNA-seq在PAH模型中揭示具有细胞类型特异性的差异表达基因(DEGs)。
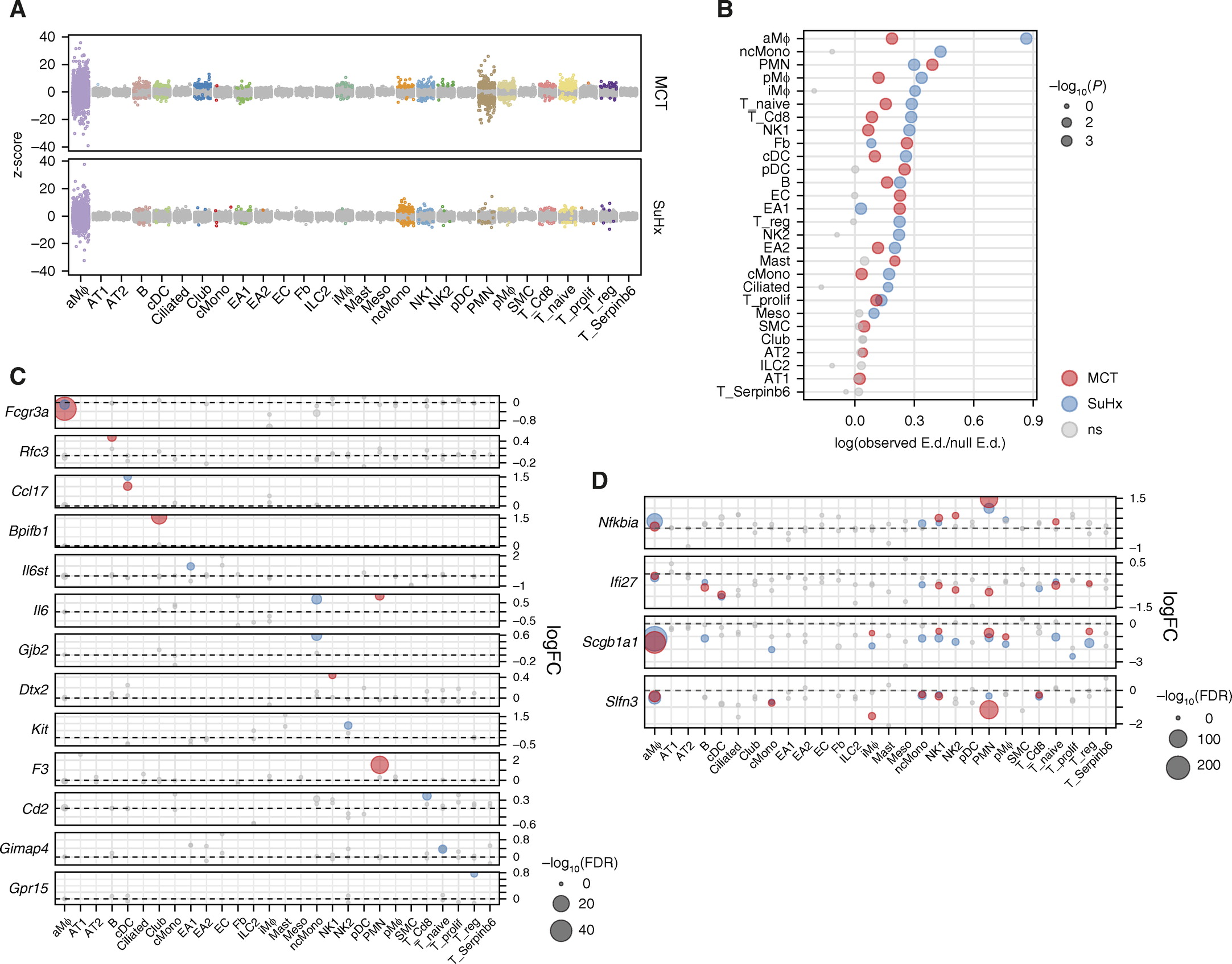
4.scRNA-seq在PAH模型中揭示具有细胞类型特异性的信号通路。其中干扰素(IFN)信号的强烈下调,两种模型最显着的共性是跨细胞类型的TNFα/NF-κB信号传导的广泛上调。
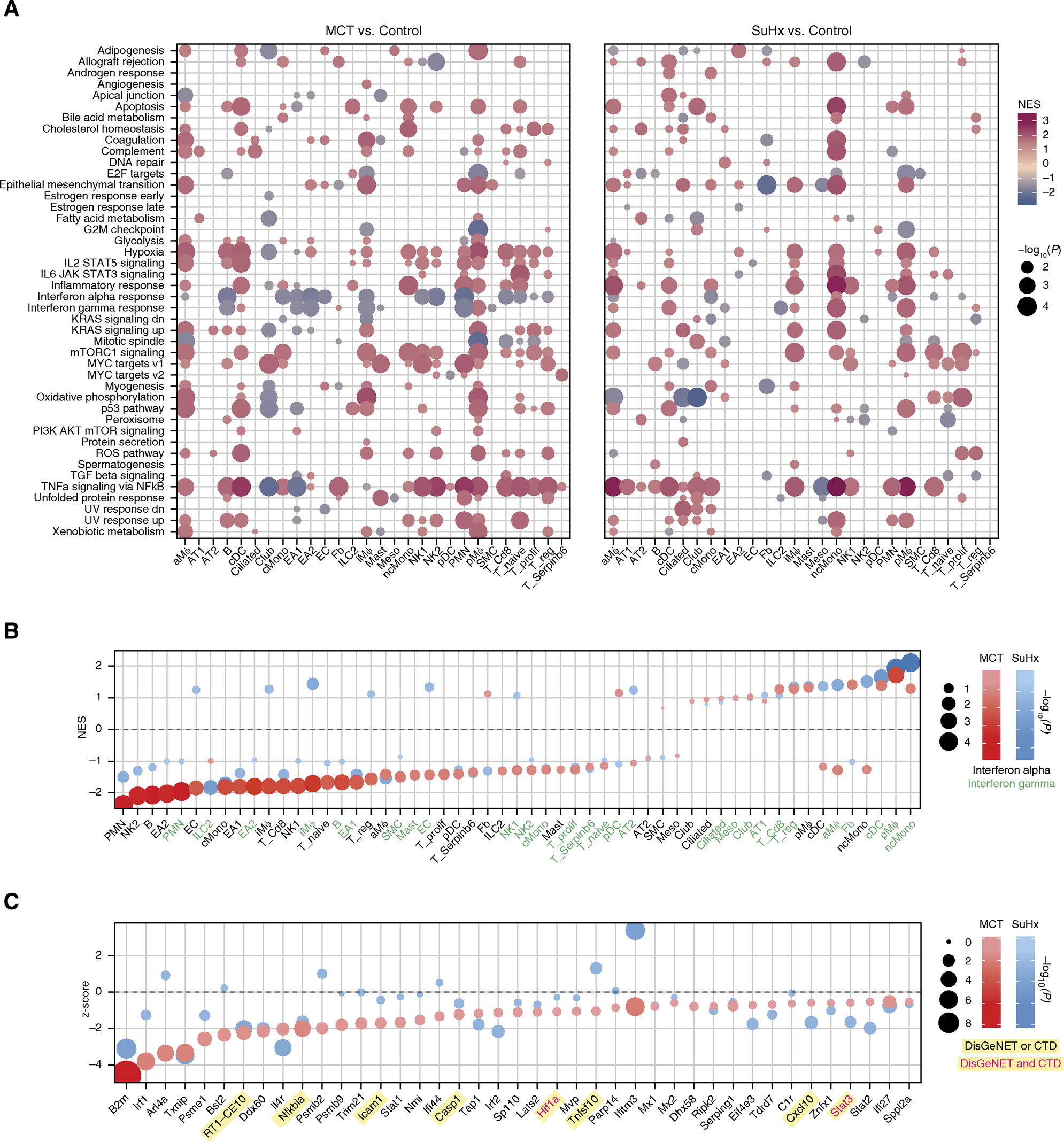
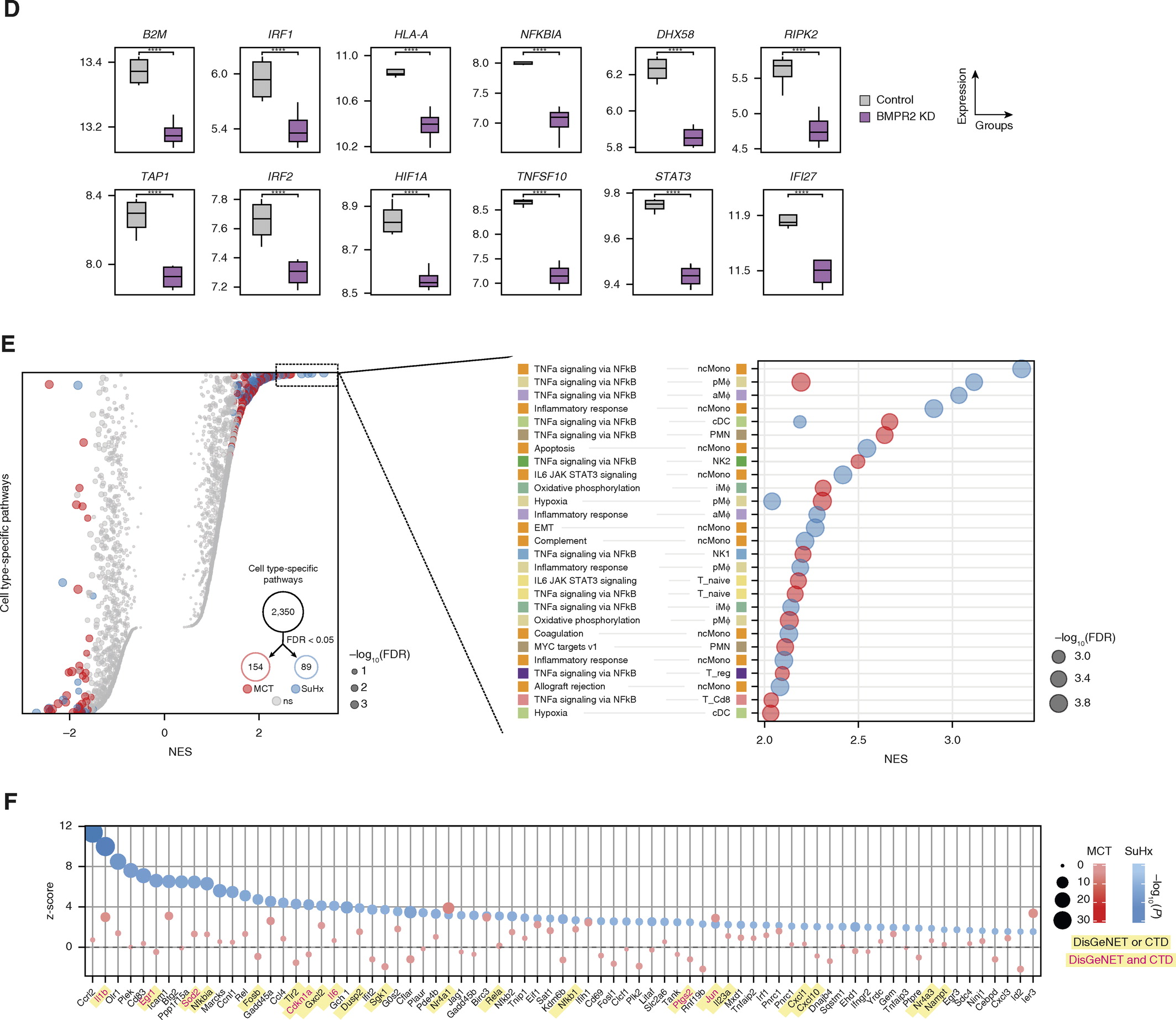
5.使用RNA原位杂交和免疫荧光进行差异基因的验证。
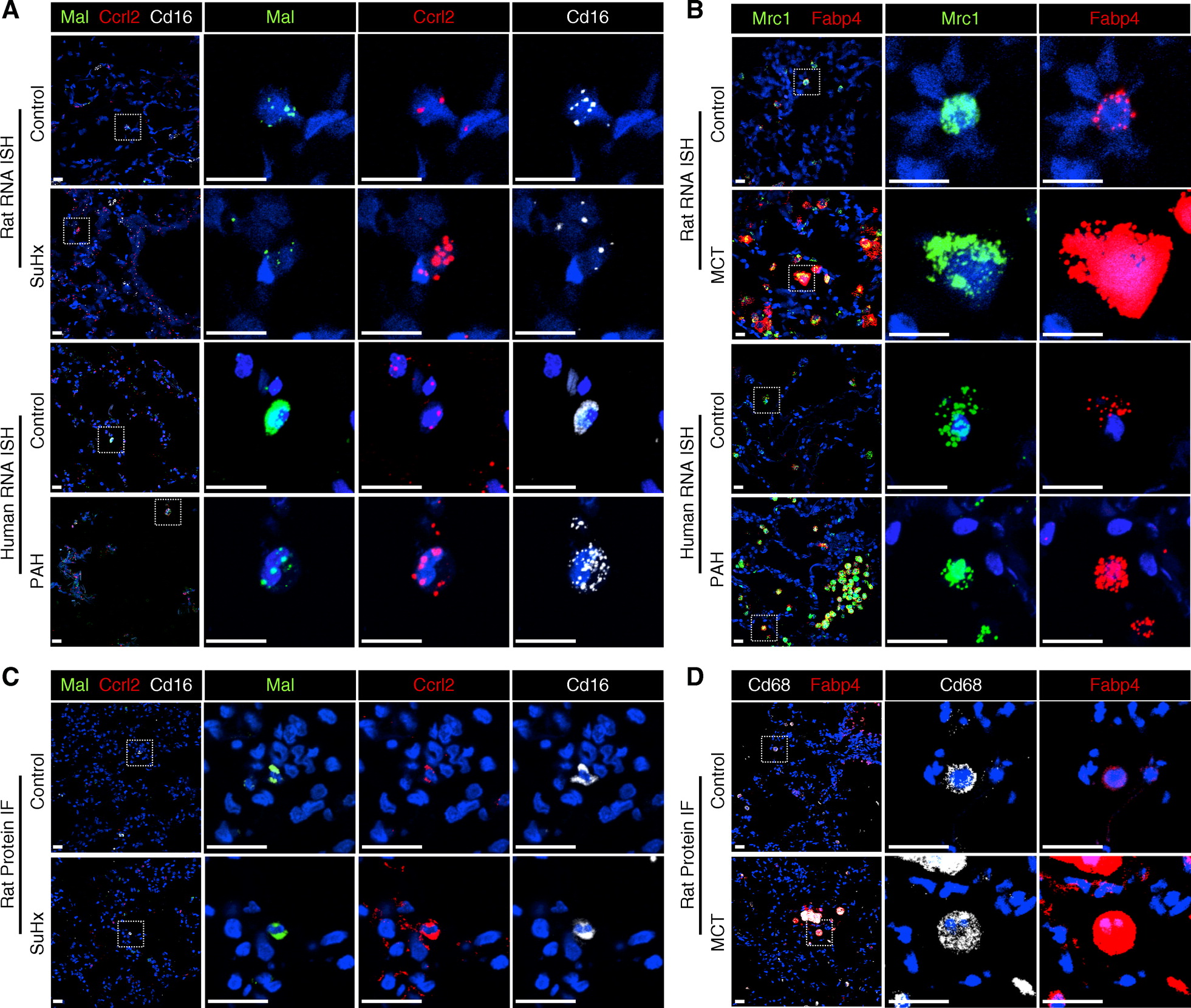
6.对大鼠scRNA-seq 差异基因与人PAH基因的整合分析支持与人的相关性。
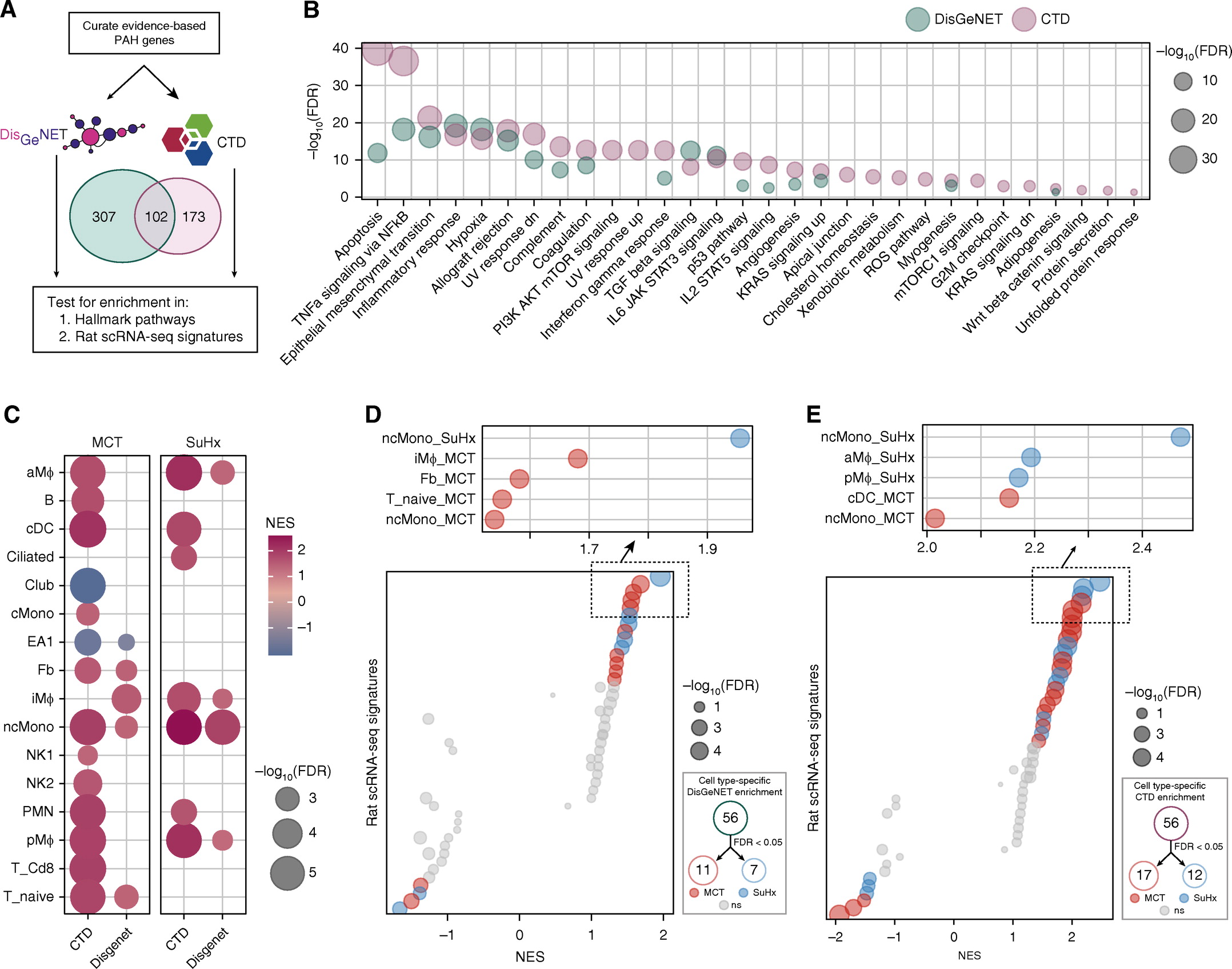
7.scRNA-seq发现与人PAH相关的血管细胞类型。例如,研究最深入的PAH基因Bmpr2在MCT EA1中被下调,而在EA2中则未下调;而在SuHx血管细胞中未观察到下调,
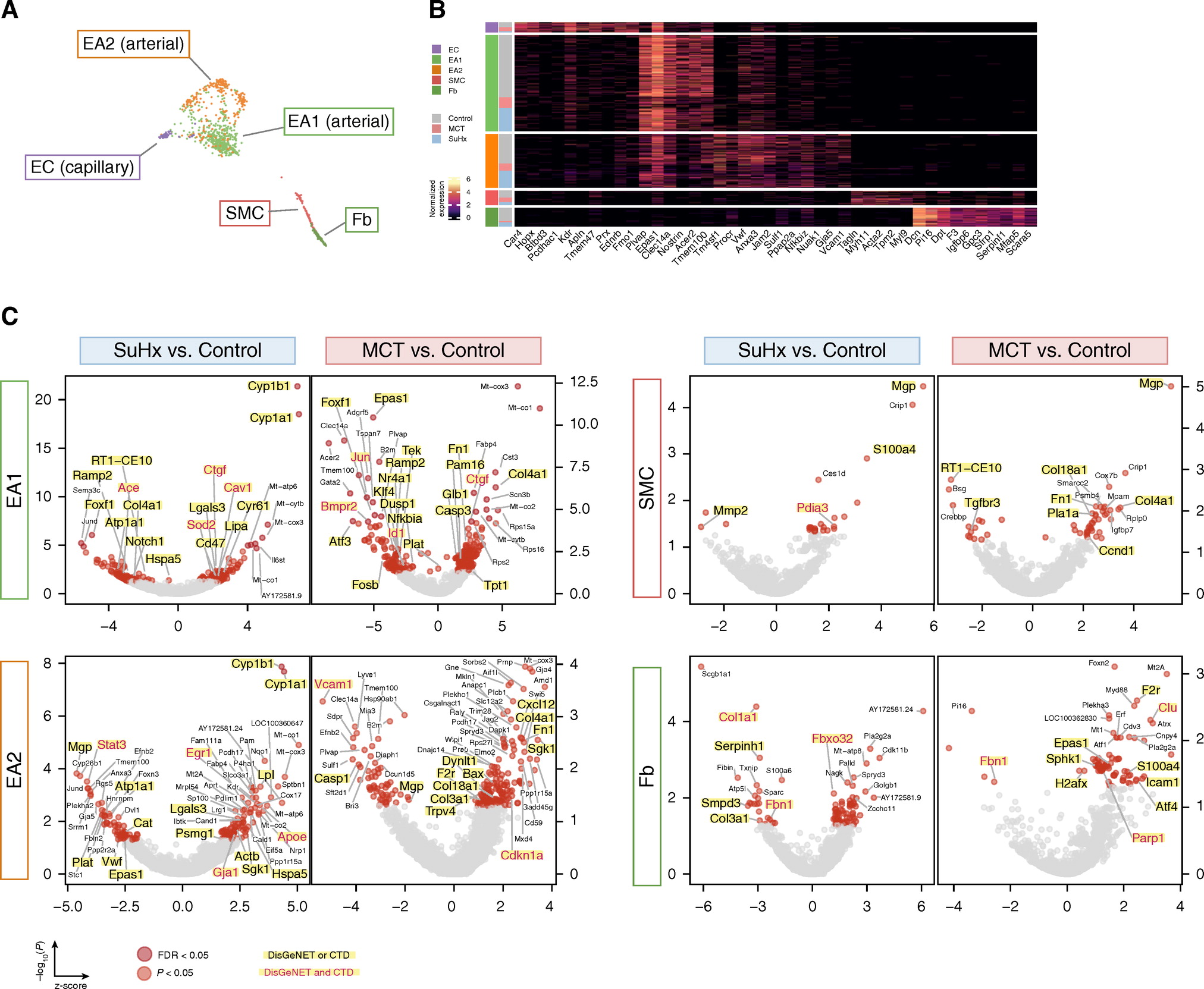
8. 将大鼠差异性基因表达与连接图相联系可以重新定位确定潜在的候选药物。例如,目前用于PAH患者的内皮素受体拮抗剂波生坦和已完成PAH的2期临床试验的他克莫司在细胞类型和疾病模型上的连通性非常相似,表明可能归因于多种途径类似于BMP信号的激活。
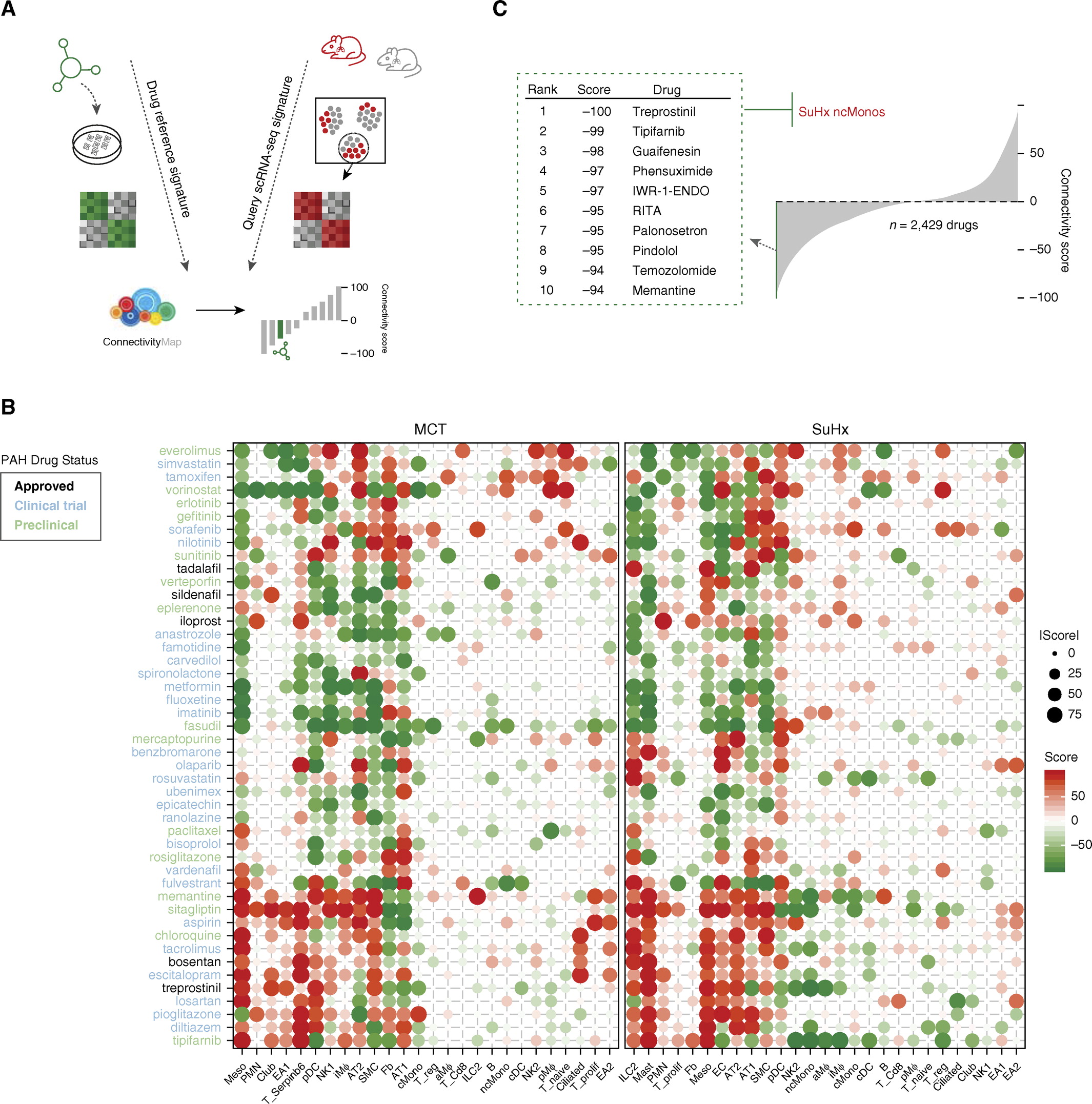
9.提供公开的sc-RNA数据库,以实现交互式浏览整个scRNA-seq数据集以及搜索和下载特定于细胞类型的标记基因,疾病特征以及药物预测。
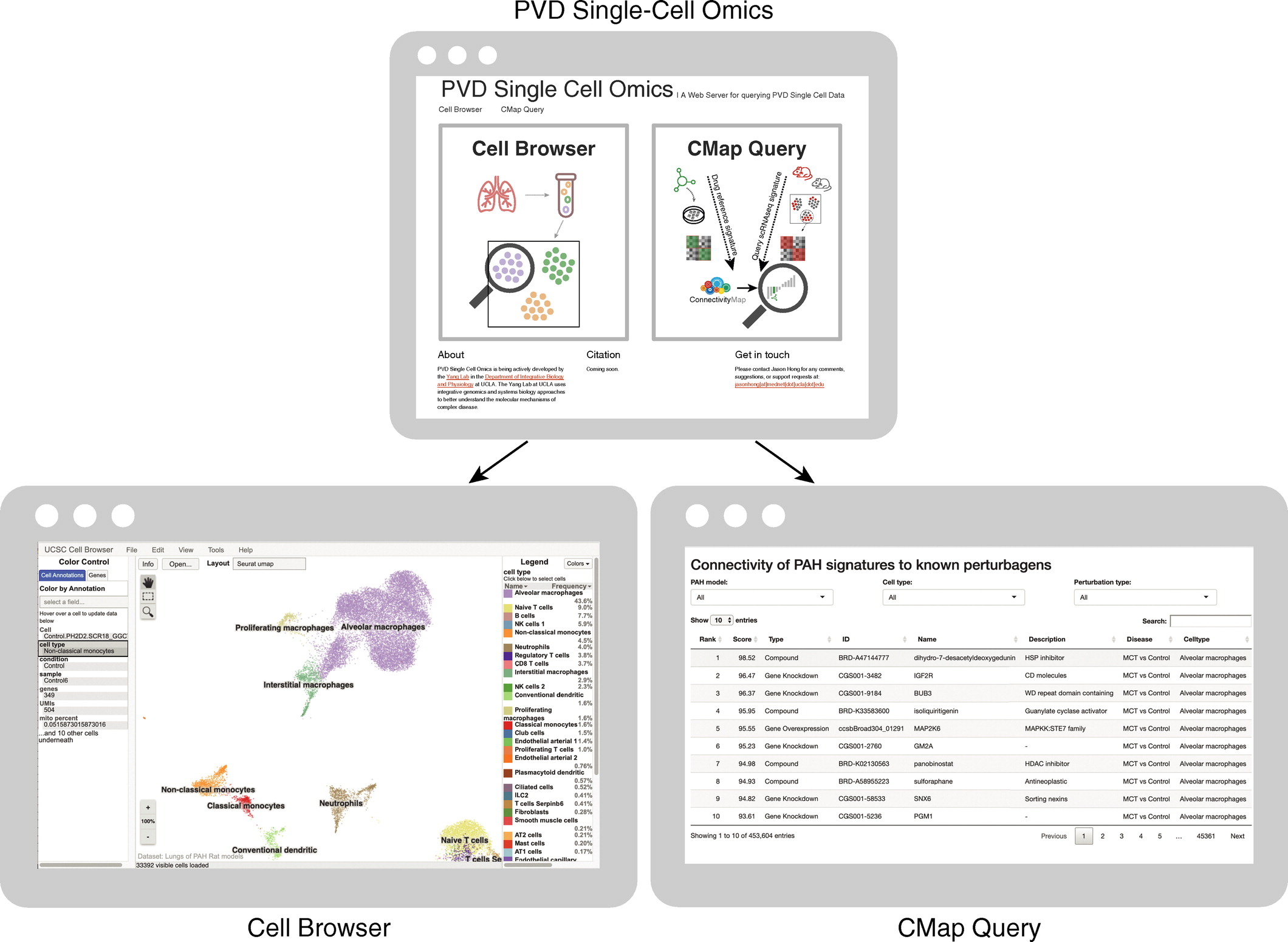
研究总结:
对Sugen-hypoxia和MCT大鼠模型的单细胞研究剖析了单个肺细胞群体中基因表达程序的独特和共同失调,阐明了它们与人PAH病理生物学的相关性,并预测了药物重新定位的可能性。这项研究将为PAH转化研究中临床前模型的合理使用提供指导。

Prof. Xia Yang早年毕业于山东大学,并在乔治亚州立大学分子遗传学/生物信息学博士,在UCLA接受了系统遗传学的博士后培训。在回到加州大学洛杉矶分校任教之前,她曾是Rosetta Inpharmatics / Merck&Co.的高级研究科学家和Sage Bionetworks的系统生物学总监。目前其在UCLA的实验室研究重点是开发和应用多组织多体组学系统生物学方法来剖析各种复杂疾病的分子网络,从心血管疾病到神经退行性疾病和神经系统疾病,并利用系统级网络来指导精准医学。通过整合人类和啮齿类动物种群的遗传,转录,表观基因组,蛋白质组学,肠道菌群和表型数据,我们研究了遗传和环境风险因素之间的复杂相互作用如何扰乱组织和细胞特异性基因网络,进而诱发疾病变异 易感性。随后,我们将疾病的因果分子网络用作治疗目标识别和生物标志物发现的基础。
文章出处:
Hong J, Arneson D, Umar S, Ruffenach G, Cunningham CM, Ahn IS, Diamante G, Bhetraratana M, Park JF, Said E, Huynh C, Le T, Medzikovic L, Humbert M, Soubrier F, Montani D, Girerd B, Trégouët DA, Channick R, Saggar R, Eghbali M, Yang X. Single-Cell Study of Two Rat Models of Pulmonary Arterial Hypertension Reveals Connections to Human Pathobiology and Drug Repositioning. Am J Respir Crit Care Med. 2021 Apr 15;203(8):1006-1022. doi: 10.1164/rccm.202006-2169OC. PMID: 33021809; PMCID: PMC8048757.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#动脉高压#
104
#肺动脉高压#模型的#单细胞测序#
200
您好!这篇文献可否发我看一下呢?我没有下载到。万分谢谢您! 406922468@qq.com
99
#新发现#
89
#RCC#
114
学习
121
学习
94
关注啦
147
认真学习了
120
好文章,谢谢分享。
123