华科薛宇/川大贾大教授团队《自然·通讯》:生酮饮食通过赖氨酸β-羟基丁基化重塑癌症代谢
2024-08-15 BioMed科技 BioMed科技 发表于上海
华中科技大学薛宇教授和四川大学贾大教授等人通过对小鼠肝脏的多组学分析表明,蛋白质Kbhb受到KD的强烈影响。
赖氨酸β-羟基丁酰化(Kbhb)是由生酮饮食(KD)诱导的翻译后修饰,而许多研究已经证明生酮饮食对多种人类疾病具有治疗作用。很少有人知道Kbhb是如何调节细胞过程的。在此,华中科技大学薛宇教授和四川大学贾大教授等人通过对小鼠肝脏的多组学分析表明,蛋白质Kbhb受到KD的强烈影响。使用具有已知功能的小型训练数据集,作者开发了一种生物信息学方法来预测功能重要的赖氨酸修饰位点(pFunK),该方法揭示了各种蛋白质上功能相关的Kbhb位点,包括醛缩酶B(ALDOB)Lys108。在肝细胞癌细胞中消耗KD或补充β-羟基丁酸酯会增加ALDOB Lys108bhb并抑制ALDOB的酶活性。Kbhb-minicking突变(p.Lys108Gln)减弱ALDOB活性及其与底物果糖-1,6-二磷酸的结合,抑制哺乳动物雷帕霉素信号传导和糖酵解的靶点,并显著抑制癌症细胞增殖。该研究揭示了Kbhb在调节癌症细胞代谢中的关键作用,并为预测功能上重要的赖氨酸修饰位点提供了一种普遍适用的算法。相关工作以“Ketogenic diet reshapes cancer metabolism through lysine β-hydroxybutyrylation”为题发表在Nature Metabolism。

【文章要点】
为了系统地研究KD的功能影响,作者对摄入或不摄入KD的小鼠肝脏进行了多组学分析,包括转录组学、蛋白质组学、代谢组学和β-羟基丁酰组学。有趣的是,研究发现,对肿瘤发生和进展至关重要的多种代谢途径,如糖酵解和三羧酸(TCA)循环,并且主要在β-羟基丁酰氨基水平上显著重塑。由于只有少数Kbhb位点被报道具有功能重要性,因此作者开发了一个分层学习框架,即预测功能重要的赖氨酸修饰位点(pFunK),以预测功能性Kbhb位点。作者选择了pFunK预测的六个Kbhb位点,并成功验证了其中五个,包括1,6-二磷酸果糖(FBP)ALDOB-Lys108(图1)。
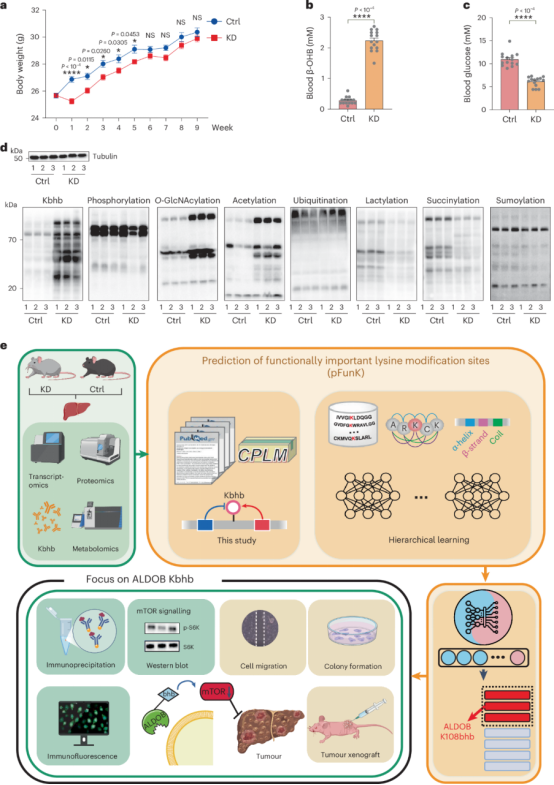
图1 本研究的主要步骤
进一步的实验表明,KD消耗或β-OHB添加有效增加了ALDOB-Lys108bhb,导致哺乳动物雷帕霉素靶点(mTOR)信号通路的抑制和癌症细胞增殖的抑制。至关重要的是,pFunK可以扩展到研究其他类型的赖氨酸酰化,如赖氨酸乙酰化(Kac)、赖氨酸丙酰化(Kla)和赖氨酸巴豆酰化(Kcr)。总之,作者不仅揭示了ALDOB-Lys108bhb在KD触发的癌症代谢重塑中的关键作用,而且还为预测功能上重要的赖氨酸修饰位点提供了一种普遍适用的算法(图2)。
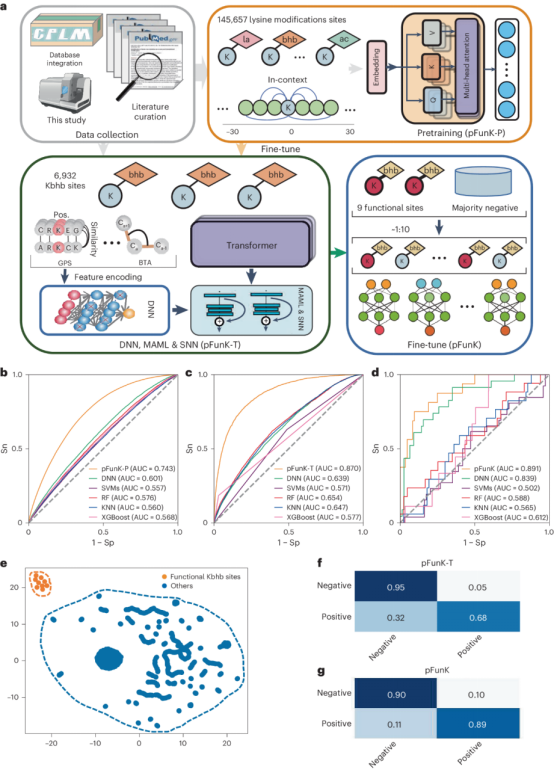
图2 pFunK的层次结构和性能
原文链接:
https://www.nature.com/articles/s42255-024-01093-w
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#生酮饮食# #癌症代谢# #赖氨酸β-羟基丁酰化#
256