Lancet Oncol:卡非佐米和来那度胺治疗原发性浆细胞白血病的EMN12/HOVON-129研究最终分析
2023-09-21 聊聊血液 聊聊血液 发表于上海
总的来说,尽管卡非佐米和来那度胺为基础的诱导、巩固和维持治疗在年轻和老年原发性浆细胞白血病患者中均产生了强效抗肿瘤活性,但无进展生存期和总生存期仍存在不足。
原发性浆细胞白血病
原发性浆细胞白血病(primary plasma cell leukaemia,pPCL)是一种侵袭性浆细胞恶性肿瘤,由于疾病相关和治疗相关并发症,预后差,早期死亡率高,约占多发性骨髓瘤患者的1-2%,传统化疗治疗后中位总生存期(OS)仅4-6个月。研究显示新药(硼替佐米和来那度胺)一线治疗仅能适度提高OS,大剂量美法仑 (HDM) 序贯自体造血干细胞移植 (HSCT) 或异基因HSCT 也可改善年轻患者的预后,此外双次自体HSCT较单次自体HSCT具有改善OS的趋势。然而即使采用这些新策略,pPCL的生存率仍不令人满意,早期死亡率较高(中位OS:老年、不适合移植患者为6-12个月,年轻、适合移植的患者为2-3年,年龄≤65岁的患者6个月死亡率高达25%,年龄>65岁的患者6个月死亡率高达49%)
前瞻性2期 EMN12/HOVON-129 研究纳入新诊断pPCL患者根据年龄将患者分配至两种不同治疗方案之一(年轻患者,年龄18-65岁;老年患者,≥66岁),所有患者均接受速效卡非佐米-来那度胺-地塞米松 (KRd) 三联方案诱导治疗以快速控制临床表现,并防止由于不可逆的疾病并发症导致的早期死亡。年轻患者接受4个周期的 KRd 诱导,随后自体 HSCT 串联减低强度异基因HSCT,或双次自体HSCT。诱导和移植后进行 KRd 巩固治疗和维持治疗,包括卡非佐米和来那度胺。老年患者接受8个周期的 KRd 诱导治疗,随后接受卡非佐米-来那度胺维持治疗。《The Lancet Oncology》近日报道了该研究最终分析结果。

研究方法
该非随机、II期、前瞻性、多中心研究入组欧洲19家中心既往未经治疗的症状性原发性浆细胞白血病患者(定义为循环单克隆浆细胞>2×109/L或白细胞分类计数的浆细胞增多>20%);18-65岁(年轻患者)和≥66岁(老年患者)患者在年龄特异性队列中接受治疗,并单独分析。
年轻患者接受4个28天/周期的KRd(第1、2、8、9、15和16天卡非佐米 [起始剂量,第1周期第1和2天20mg/m²静脉给药;目标剂量,此后36 mg/m²静脉给药];第1-21天来那度胺 25mg 口服给药;第1、2、8、9、15、16、22和23天地塞米松 20mg 口服给药)。然后患者接受环磷酰胺和粒细胞集落刺激因子的干细胞动员,以及美法仑200mg/m²(静脉)的标准自体HSCT。随后对具有HLA 全相合同胞或合适的无关供者患者进行2个疗程的 KRd 巩固治疗和减低强度预处理异基因HSCT。异基因HSCT 后2个月开始卡非佐米维持治疗,异基因 HSCT 后8个月在卡非佐米基础上加用低剂量来那度胺;维持治疗直至疾病进展或出现过度毒性。在无合适供者的情况下,在不适合接受异基因HSCT 的情况下,或如果患者不想接受异基因HSCT,如果患者达到至少部分缓解,则在第一个疗程自体HSCT后2-3个月之间进行第二个疗程的HDM和自体HSCT;随后4个周期的 KRd 巩固治疗,以及卡非佐米-来那度胺维持治疗直至疾病进展或过度毒性。
老年患者接受8个周期的 KRd 诱导治疗(第1、2、8、9、15和16天卡非佐米 [起始剂量,第1周期第1和2天20 mg/m²静脉给药;目标剂量,此后36 mg/m²静脉给药];第1-21天来那度胺 25mg 口服给药;第1、2、8、9、15、16、22和23天地塞米松 20mg 口服给药),随后卡非佐米-来那度胺维持治疗,直至进展或过度毒性。在维持治疗期间,在前12个28天/周期的第1、2、15和16天静脉给予27 mg/m²卡非佐米,然后在所有后续周期的第1天和第15天静脉给予56 mg/m²;在第1周期开始来那度胺治疗,剂量为10mg,第1-21天口服,28天为一个周期。
主要终点为无进展生存期(PFS),次要终点为总生存期(OS)、缓解率、安全性和毒性。
研究结果
患者
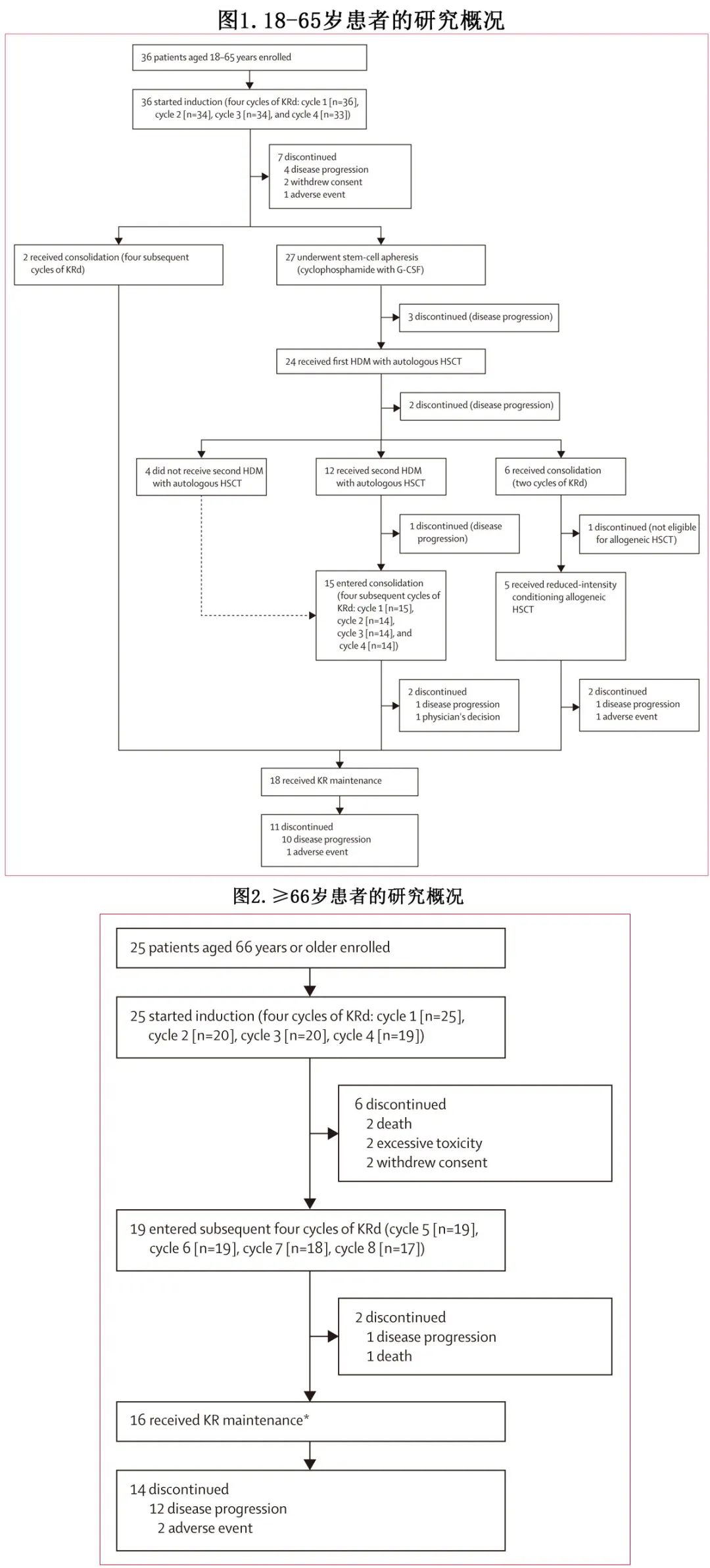
共纳入61例原发性浆细胞白血病患者(36例年龄18-65岁,25例年龄≥66岁;图1和图2)。
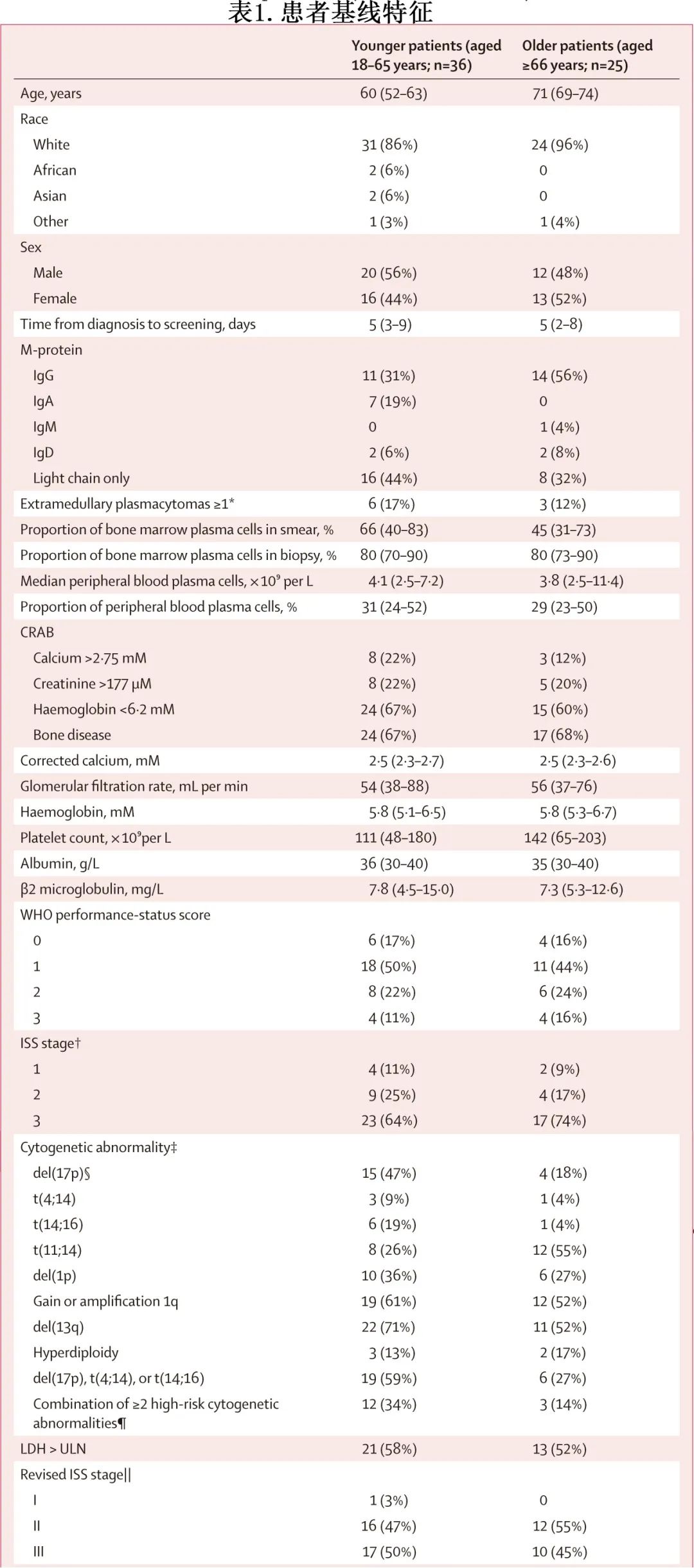
年轻患者队列中位年龄为60岁,20例患者 (56%) 为男性(表1)。老年患者队列中位年龄为71岁,12例患者 (48%) 为男性(表1),患者表现为高肿瘤负荷、晚期疾病分期(ISS和R-ISS)和高频率的高危特征(例如高危细胞遗传学异常或 LDH 升高)。
疗效
年轻患者队列
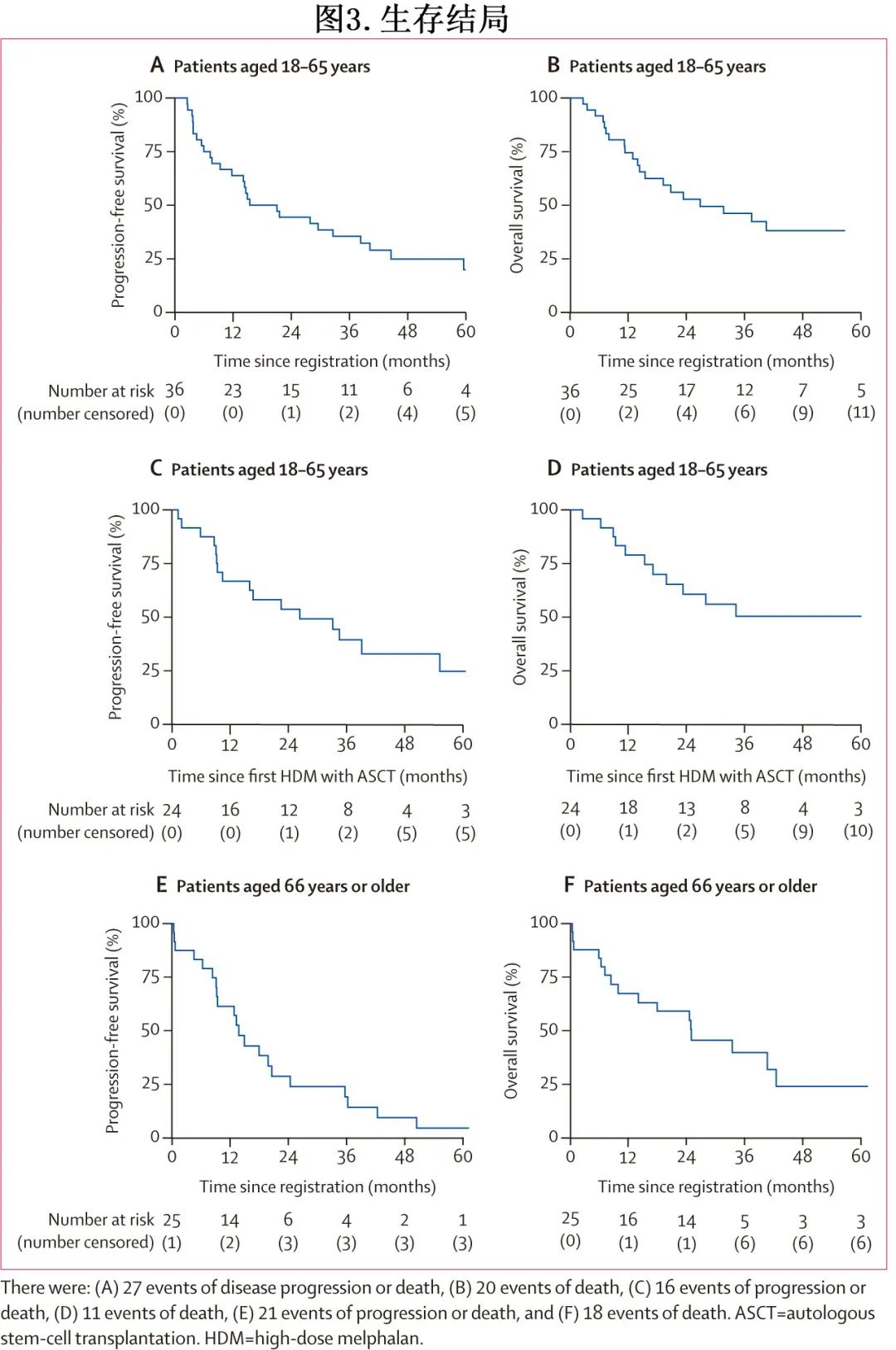
年轻患者队列中位随访43.5个月,报告了27例疾病进展或死亡事件,中位PFS为15.5个月(图3A),足以拒绝无效假设(中位无进展生存期为9个月)。
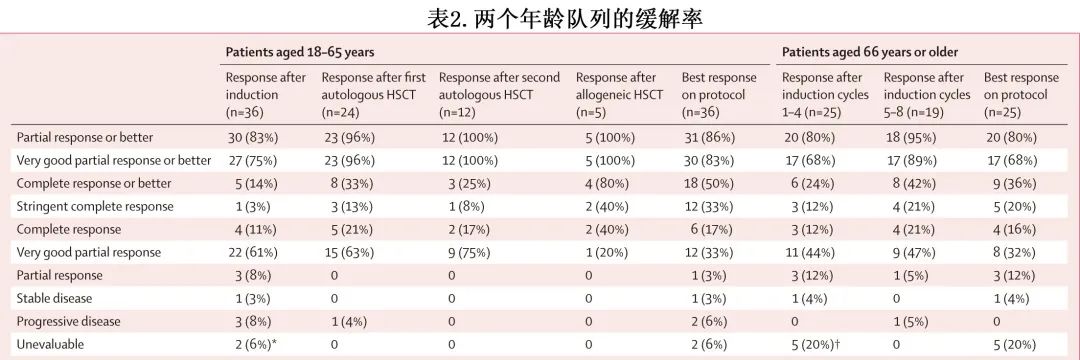
年轻患者队列整个研究期间获得的最佳缓解为:31例 (86%) 患者≥PR,30例 (83%) 患者≥VGPR,18例 (50%) 患者≥CR(表2)。在评价MRD的20例患者中,16例 (80%) 为MRD阴性(阈值为1个肿瘤细胞/105白细胞)。
年轻患者队列20例患者 (56%) 死亡(19例患者为复发相关死亡,1例为复发死亡 [退出方案治疗,异基因HSCT 后4个月人类偏肺病毒呼吸道感染])。中位总生存期为28.4个月(图3B),早期死亡率较低(6个月时8.3%)。
两队列不同时期的缓解率见表2。30例 (83%) 患者诱导后的缓解为≥PR,27例 (75%) 为≥VGPR,5例 (14%) 患者为≥CR。24例患者HDM自体HSCT后的≥PR为96%,24例患者中的8例 (33%)≥CR,23例 (96%) ≥VGPR。5例患者接受异基因HSCT,随后1例患者发生急性移植物抗宿主病(2级),另1例患者发生慢性移植物抗宿主病(重度);所有5例 (100%) 异基因 HSCT 后的缓解均为≥VGPR,4例 (80%) 患者为≥CR。12例接受了二次HDM序贯自体HSCT以及4周期KRd巩固,二次自体 HSCT 后的≥PR为100%,3例 (25%) 患者≥CR,12例 (100%) 患者≥VGPR。
年轻患者队列18例患者接受了维持治疗,其中16例为卡非佐米联合来那度胺,两药中位维持治疗时间为26.6个月。在开始维持治疗前,10例 (56%) 患者为VGPR,1例 (6%) CR,7例 (39%)sCR。
年轻患者队列接受首次HDM序贯自体HSCT的24例患者,从首次自体HSCT计算的的中位PFS为26.2个月、中位OS无法估计(图3C、D)。事后分析中计算了从二次移植开始的PFS,二次自体HSCT和异基因HSCT组的PFS无差异(31.2个月和49.2个月,2年PFS率58%和60%);从二次移植开始的OS也无差异(均为无法估计,2年OS率为82%和53%)。
老年患者队列
老年患者队列中位随访32.0个月,发生21起进展或死亡事件,中位PFS为13.8个月(图3E),足以拒绝无效假设(中位无进展生存期6.5个月)。20例(80%)患者的最佳缓解为≥PR,17例 (68%) 为≥VGPR,9例(36%;表2)为≥CR。≥CR 且可评价MRD的8例患者中的5例 (63%) 达到MRD阴性 (10-5)。
25例患者中的18例 (72%) 死亡(12例患者发生复发相关死亡,6例患者发生非复发死亡)。中位OS为24.8个月(图3F)。早期死亡率较低,6个月时为16%。
在前4个 KRd 诱导周期后,20例 (80%) 患者为≥PR,17例 (68%) ≥VGPR,6例(24%;表2)≥CR;4个额外诱导周期后缓解深度改善(19例患者中,18例 [95%] 为≥PR,17例 [89%] 为≥VGPR,8例 [42%] 为≥CR;表2)
16例患者开始维持治疗,其中81%为卡非佐米联合来那度胺,两药维持的中位时间为10.3个月。
安全性
研究期间发生的≥2级不良事件(移植相关不良事件除外)总结见表3和表4。
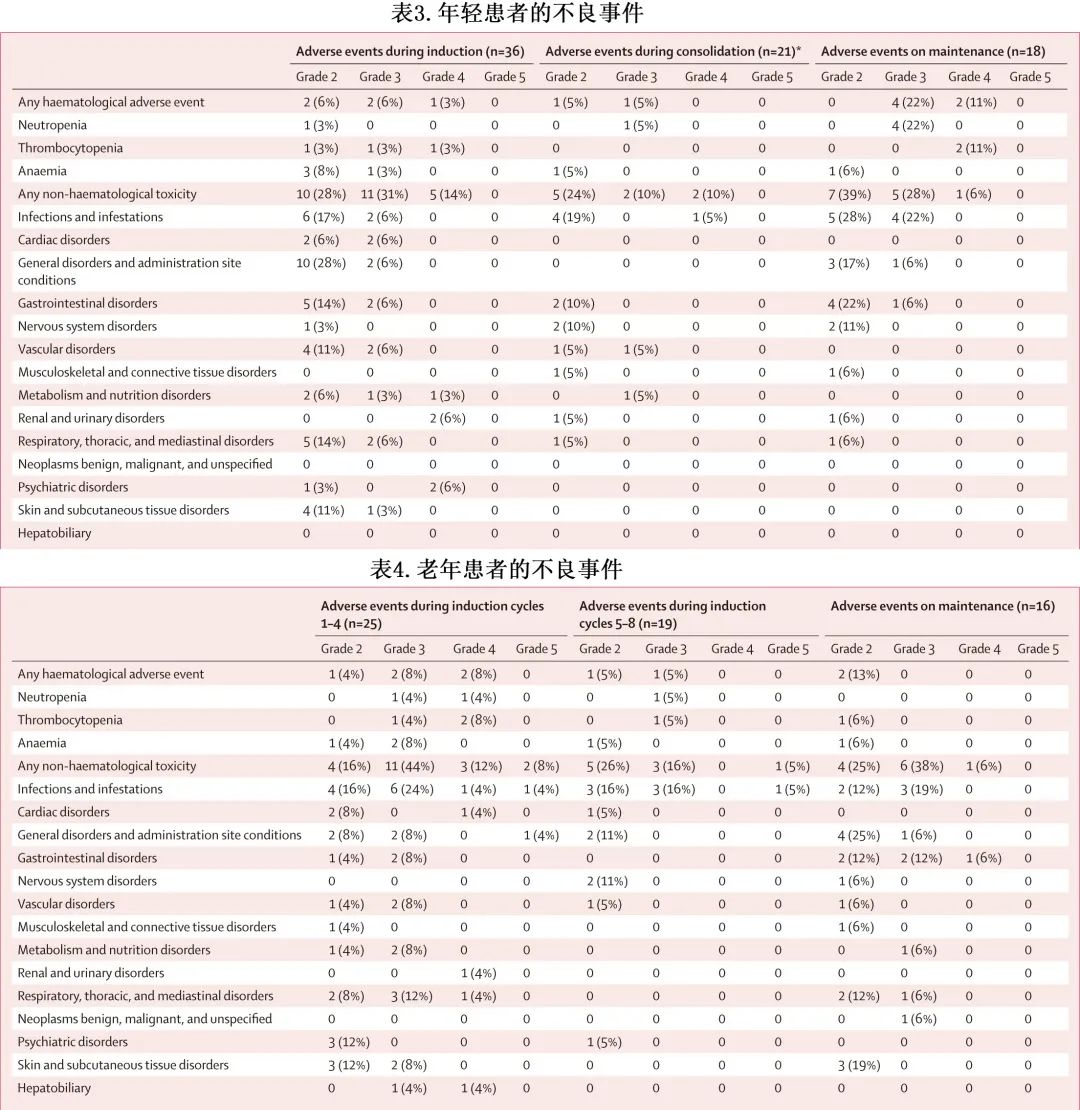
年轻患者队列
在年轻患者队列 (n=36) 中,分别有3例 (8%) 和16例 (44%) 患者在诱导期间报告了≥3级累积血液学和非血液学毒性(表3)。诱导治疗期间≥3级非血液学毒性包括心脏(2例 [6%] 患者)、胃肠道(2例 [6%] 患者)、呼吸系统(2例 [6%] 患者)、血管(2例 [6%] 患者)、肾脏(2例 [6%] 患者)和感染性(2例 [6%] 患者)不良事件。在巩固治疗期间,≥3级血液学(21例患者中的1例 [5%])和非血液学毒性(4例 [19%] 患者)的累积发生率低于诱导治疗期间(表3)。维持治疗期间的不良事件见表3。
2例患者因不良事件而中止治疗(1例患者在接受异基因HSCT 后因多重感染中止治疗,1例患者在住院期间因肺脓毒症和胆总管结石而发生心肌梗死,需要接受内镜下逆行胰胆管造影术联合胆道支架植入术和括约肌切开术)。1例患者在泊马度胺-环磷酰胺-地塞米松作为二线治疗期间(中止方案治疗后2.5年)发生骨髓增生异常综合征。36例患者中的26例 (72%) 共发生64起治疗相关严重不良事件,大约三分之一 (30%) 的严重不良事件发生在首个 KRd 诱导治疗周期内,44%发生在诱导治疗期间;最常见的治疗相关严重不良事件为感染。未观察到给药相关死亡。为管理诱导期间的不良事件,36例患者中的7例 (19%) 降低了卡非佐米的剂量(至少20%),18例 (50%) 降低了来那度胺的剂量,13例 (36%) 降低了地塞米松的剂量。移植后巩固治疗期间,3/21例 (14%) 患者的卡非佐米剂量降低,4例 (19%) 患者的来那度胺剂量降低,5例 (24%) 患者的地塞米松剂量降低。
老年患者队列
在老年患者队列 (n=25) 中,前4个 KRd 诱导周期内,≥3级血液学和非血液学毒性的累积发生率分别为16%(n=4) 和64%(n=16)(表4)。在前4个 KRd 周期内,≥3级非血液学毒性包括心脏(1例 [4%] 患者)、胃肠道(2例 [8%] 患者)、呼吸系统(4例 [16%] 患者)、血管(2例 [8%] 患者)、肾脏(1例 [4%] 患者)和感染(8例 [32%] 患者)不良事件。在 KRd 诱导治疗周期5-8,≥3级血液学和非血液学毒性的累积发生率低于前4个诱导治疗周期(分别为1/19例 [5%] 患者和4/19例 [21%] 患者;表4)。维持治疗期间的不良事件见表4
2例患者因不良事件而中止研究(1例患者在维持治疗期间因进行性神经功能下降,1例患者因维持治疗期间发生十二指肠腺癌,治疗开始后30个月)。25例患者中的19例 (76%) 共发生54起严重不良事件,大约三分之一 (35%) 的严重不良事件发生在首个 KRd 诱导治疗周期内,61%发生在诱导治疗的前4个周期内;最常见的治疗相关严重不良事件为感染。为管理不良事件,诱导治疗期间(第1-8周期)25例患者中的12例 (48%) 降低了卡非佐米的剂量(至少20%),16例 (64%) 降低了来那度胺的剂量,17例 (68%) 降低了地塞米松的剂量。报告了3例治疗相关死亡:2例感染和1例死因不明。
总结
该2起研究共有61例患者入组并接受 KRd 诱导治疗(36例患者年龄为18-65岁 [20例 (56%) 为男性,16例 (44%) 为女性];25例患者年龄≥66岁 [12例 (48%) 为男性,13例 (52%) 为女性])。中位随访43.5个月,年轻患者的中位无进展生存期为15.5个月,中位总生存期为28.4个月;对于老年患者,中位随访时间为32.0个月,中位无进展生存期为13.8个月,中位总生存期为24.8个月。不良事件最常见于治疗开始后,感染(年轻患者2/36例 [6%]和老年患者8/25例 [32%])和呼吸道事件(年轻患者2/36例 [6%]和老年患者4/25例 [16%])是前4个 KRd 周期内最常见的≥3级事件。36例年轻患者中的26例 (72%) 和25例老年患者中的19例 (76%) 报告了治疗相关严重不良事件,感染最常见。无年轻患者报告治疗相关死亡,老年患者报告3例 (12%,2例感染和1例死因不明)。
总的来说,尽管卡非佐米和来那度胺为基础的诱导、巩固和维持治疗在年轻和老年原发性浆细胞白血病患者中均产生了强效抗肿瘤活性,但无进展生存期和总生存期仍存在不足。新的试验应评估将新型免疫治疗纳入原发性浆细胞白血病患者的治疗中,从而有效的治疗迅速相互交替,以防止早期进展。此外,循环浆细胞比例较低的患者预后与循环浆细胞大于20%的患者相同,入组试验可能受益,或通过将原发性浆细胞白血病患者入组超高危多发性骨髓瘤患者的试验来获益。
参考文献
Niels W C J van de Donk ,et al. Treatment of primary plasma cell leukaemia with carfilzomib and lenalidomide-based therapy (EMN12/HOVON-129): final analysis of a non-randomised, multicentre, phase 2 study.Lancet Oncol . 2023 Sep 14;S1470-2045(23)00405-9. doi: 10.1016/S1470-2045(23)00405-9.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








啦咯啦咯啦咯
80