JAMA子刊:80%患者湿疹症状控制,重磅抗炎药5年持续安全有效
2024-09-25 医学新视点 医学新视点 发表于上海
这项研究支持了dupilumab治疗的长期安全性和有效性。
特应性皮炎是一种常见的湿疹,这是一种常见的慢性、复发性、炎症性皮肤病,发病通常始于儿童期,并可能持续到成年期,且患者还常合并过敏性鼻炎、哮喘等其他特应性疾病。全球范围内儿童患病率约10%~20%,成人患病率可高达10%。
重磅抗炎疗法dupilumab是首款获得美国FDA和欧洲药品管理局(EMA)批准用于局部治疗效果不佳的中重度湿疹的靶向生物药剂。自2017年获批以来,这款疗法在临床实践中的治疗数据也得到了进一步积累,对于特应性皮炎这样需要长期用药的慢性疾病而言,对药物长期应用效果的评估至关重要。
近期,《美国医学会杂志-皮肤病学》(JAMA Dermatology)发表一项长期随访研究,支持了dupilumab长期用药的安全有效性。在长达5年的临床实际应用中,dupilumab保持了较高的有效性,主要疗效指标控制良好的患者比例近80%或更高,且约2/3患者用药频率逐渐降低至每3-4周用药一次,不到1/4患者因不良事件和/或效果不佳等原因而停止治疗。

截图来源:JAMA Dermatology
Dupilumab是一款人源化的单克隆抗体,可特异性抑制白细胞介素-4(IL-4)和白细胞介素-13(IL-13)的过度信号传导,这两种关键蛋白分子是特应性皮炎病理中持续性炎症的主要驱动因素。Dupilumab需通过皮下注射给药。
这项前瞻性多中心队列研究旨在评估dupilumab在儿童、成人和老年特应性皮炎患者中的临床疗效及停药原因。研究数据来自荷兰14家医院,纳入了2017年10月至2022年12月期间接受dupilumab治疗的所有1286例特应性皮炎患者,患者中位年龄38岁(四分位数:26岁-54岁),其中儿童130例,成人1025例,老年人131例。整个随访期长达5年,所有患者的中位随访时间为87.5周(四分位数:32周~157周)。
研究采用的疗效评价指标主要为湿疹面积和严重程度指数评分(EASI)和瘙痒数值评定评分(NRS)。
湿疹面积和严重程度指数评分(EASI):评估头部/颈部、上肢、躯干、下肢这4个身体区域的湿疹面积和严重程度,总分范围0~72,分数越高越严重。≤7分为轻度,8~21分为中度,22~50分为重度,51-72分为极重度。
瘙痒数值评定评分(NRS):评分范围由0分(无瘙痒)至10分(严重瘙痒),临床以提问方式让患者通过数值口头表达主观瘙痒的严重程度。
患者在研究基线时平均EASI评分为17.8分,平均瘙痒NRS评分为6.8分。治疗数据显示,大多数患者能够维持对特应性皮炎的控制:
-
EASI评分≤7分(轻度)的患者比例在治疗28周时为78.6%,在治疗5年时为92.3%,治疗期间这一比例整体维持在约80%~90%;
-
治疗16周、2年和5年时,平均EASI评分分别为5.1、4.1和2.7分,均为轻度;
-
瘙痒NRS评分≤4分的患者比例在治疗28周时为72.2%,在治疗5年时为88.2%,治疗期间这一比例整体维持在约76%~84%;
-
治疗16周时,平均瘙痒NRS评分也显著降低至3.4分,此后一直保持在较低水平;治疗5年时,平均瘙痒NRS评分为3.5分。
-
两个指标同时达标(EASI评分≤7分且瘙痒NRS评分≤4分)则视为对治疗有应答,治疗16周时的应答率为63.6%,1年时应答率为68%,治疗3.5年~5年期间应答率在76%~78%在之间。治疗至开始应答的中位时间为17周。
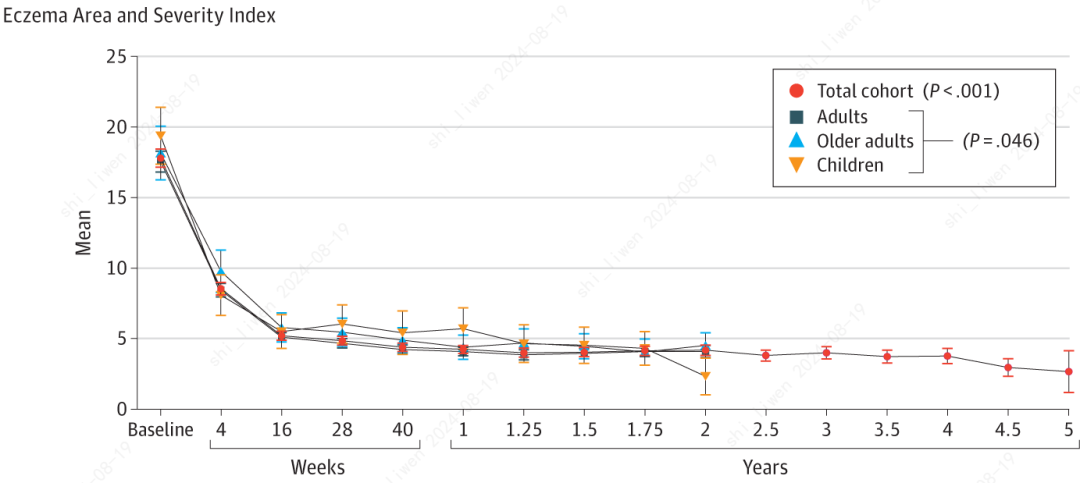
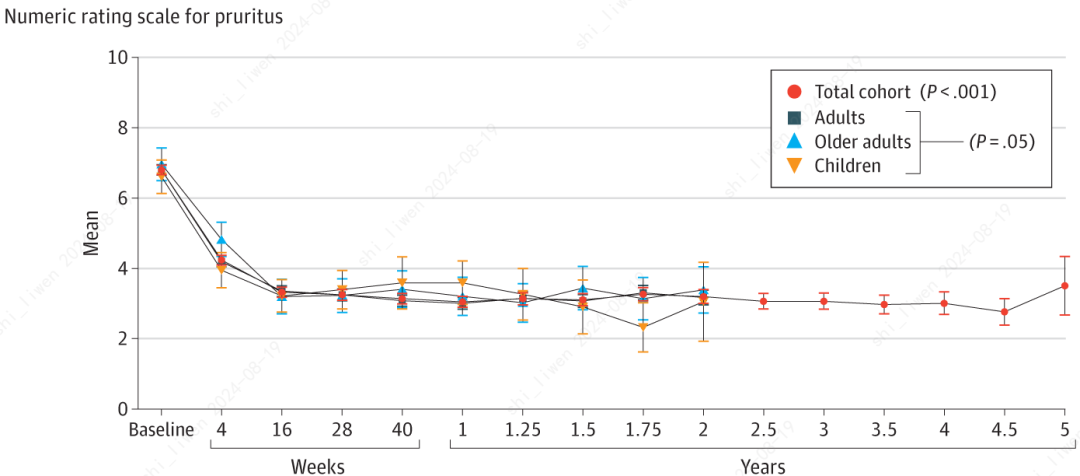
▲随着治疗时间延长,患者EASI评分和瘙痒NRS评分的变化情况。红圈-所有患者,深蓝方块-成人患者,浅蓝三角-老年患者,橙色倒三角-儿童患者(图片来源:参考资料[1])
同时,高达70.5%的患者在保持症状控制的情况下逐步减少了用药剂量,将用药间隔延长至每3-4周1次。
研究团队还进一步评估了不同年龄组之间的疗效差异。
-
在多个主要疗效评估指标上,成人患者和老年患者对dupilumab治疗的应答相似,而儿童患者在部分时间点的得分略高(症状更明显)。
-
从免疫和炎症相关生物标志物来看:成人患者、老年患者和儿童患者在治疗期间的TARC(胸腺和激活调节的趋化因子,与特应性皮炎的严重程度密切相关)水平下降趋势相似,治疗6个月后均已保持在较低水平;不同年龄组患者的嗜酸性粒细胞水平(反映2型炎症迹象)在治疗的4-28周略有升高,但在长期随访期间明显低于基线水平,并保持在正常范围内,各组长期趋势相似,整体水平始终为儿童患者>成人患者>老年患者。
此外,研究团队也关注了停药患者的情况。5年间共有306名患者(占所有患者的23.8%)停用dupilumab,这些患者的中位持续治疗时间为54周(四分位数:29周~110周),最常见的停药原因是不良事件和疗效不佳(211人,占所有停药人数69%,占所有患者的),其他停药原因包括妊娠、疾病得到控制等。此外还有41名患者重新开始dupilumab治疗,其中大多数患者恢复应答。
总体而言,这项研究支持了dupilumab治疗的长期安全性和有效性。
参考资料
[1] Boesjes CM, Kamphuis E, de Graaf M, et al., (2024). Long-Term Effectiveness and Reasons for Discontinuation of Dupilumab in Patients With Atopic Dermatitis. JAMA Dermatol, doi:10.1001/jamadermatol.2024.2517
[2] FDA approves new eczema drug Dupixent. US Food and Drug Administration. Retrieved August 15, 2024 from https://www.fda.gov/news-events/press-announcements/fda-approves-new-eczema-drug-dupixent
[3] Sanofi and Regeneron Announce FDA Approval of Dupixent® (dupilumab), the First Targeted Biologic Therapy for Adults with Moderate-to-Severe Atopic Dermatitis. Retrieved August 15, 2024 from https://www.sanofi.com/en/media-room/press-releases/2017/2017-09-28-05-00-00-1134127
[4] 中华医学会皮肤性病学分会免疫学组,特应性皮炎协作研究中心. 中国特应性皮炎诊疗指南(2020版). 中华皮肤科杂志, 2020,53(02) : 81-88. DOI: 10.35541/cjd.20191000
[5] 郝飞, 张建中. 特应性皮炎的研究现状与展望 [J] . 中华医学杂志, 2023, 103(32) : 2465-2469. DOI: 10.3760/cma.j.cn112137-20230302-00318.
[6] 宋璞, 付萌. 特应性皮炎瘙痒的临床评估及管理现状[J] . 中华医学杂志, 2023, 103(32) : 2531-2537. DOI: 10.3760/cma.j.cn112137-20230108-00042.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#湿疹# #Dupilumab#
51