MEK抑制剂单药治疗为BRAF V600E突变甲状腺乳头状癌伴肺转移患者带来长期缓解
2024-05-03 苏州绘真医学 苏州绘真医学 发表于上海
本文病例证实了MEK抑制剂单药治疗作为BRAF突变阳性甲状腺乳头状癌的替代治疗方法的潜力。
携带BRAF基因突变的实体瘤目前可通过BRAF/MEK抑制剂联合治疗,并且有大量有关缓解率的文献。但很少有研究描述BRAF突变阳性实体瘤对MEK抑制剂单药治疗的临床反应。本文报告一例 57 岁的女性,诊断为甲状腺乳头状癌(PTC)和进行性肺转移,最初接受甲状腺全切除术,随后接受了促甲状腺激素抑制治疗。NGS测序结果显示,该肿瘤存在BRAF V600E突变,该患者被纳入了MEK1/2口服抑制剂比美替尼(binimetinib)的临床研究。在开始治疗后不久,患者因肺转移迅速消退而出现气胸,比美替尼治疗 6 个月后的CT扫描显示部分持续缓解。一年后,由于出现痤疮样皮疹,减少了比美替尼剂量。经过 5 年的比美替尼治疗后,肺转移灶重新生长,治疗方案更改为口服多激酶抑制剂仑伐替尼(lenvatinib)。本文病例证实了MEK抑制剂单药治疗作为BRAF突变阳性甲状腺乳头状癌的替代治疗方法的潜力。
背 景
目前BRAF突变阳性实体瘤的标准治疗方法是BRAF/MEK抑制剂联合治疗,该策略比BRAF抑制剂单药治疗能更好地推迟耐药性的出现并缓解鳞状细胞癌。相似的是,MEK抑制剂单药治疗仅对BRAF突变阳性的黑色素瘤有中等疗效。然而,与大量关于BRAF/MEK抑制剂联合治疗的文献相比,关于MEK抑制剂单药治疗其它BRAF突变阳性癌症的报道很少。本文介绍了一例BRAF突变阳性的甲状腺乳头状癌(PTC),对MEK抑制剂单药治疗具有长期临床反应。
病 例
患者女,57 岁,五年前因诊断为PTC肺转移进展而转诊至名古屋大学临床肿瘤化疗科(图1a)。初步诊断后,患者行甲状腺全切除术,病理检查确定为pT3bN1bM1 IVB期的PTC(根据AJCC/TNM v7版标准)。当时研究人员使用 5 mCi的碘-131进行了诊断性闪烁扫描,在肺转移灶中未见碘-131累积,因此患者开始了促甲状腺激素抑制治疗。
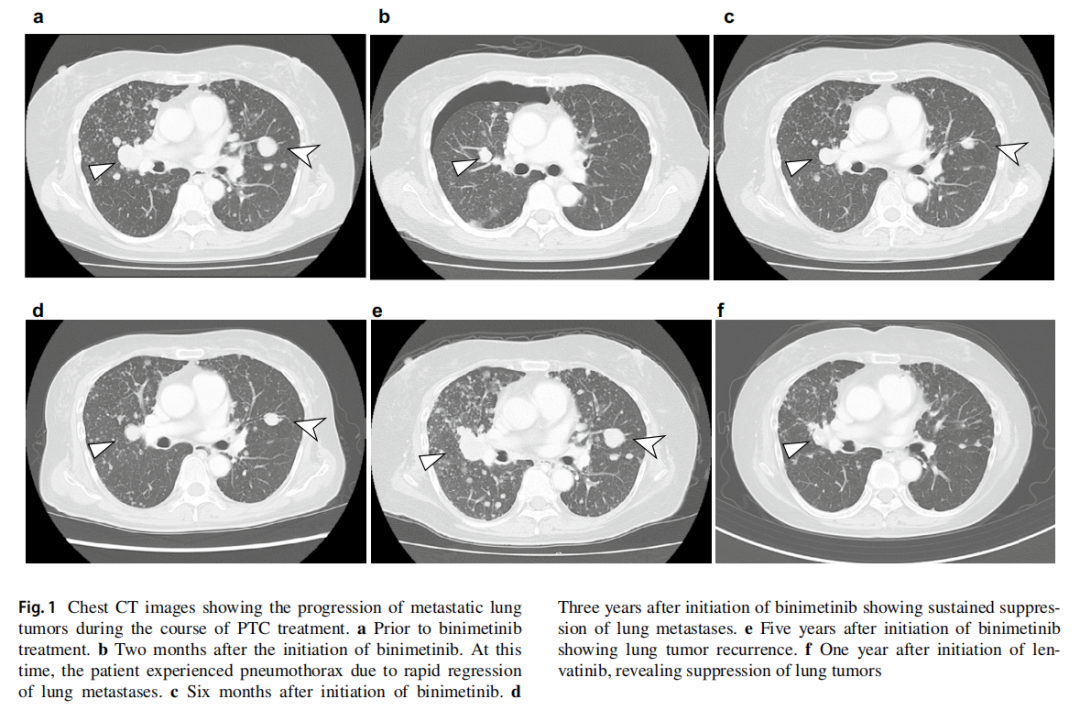
▲图1 胸部CT显示在PTC治疗中出现肺转移进展
患者身体健康状况良好(体力状态评分为 0),实验室检查未见异常。患者从不吸烟,且遗传性肿瘤家族史。对原发部位的福尔马林包埋手术标本进行了NGS检测,发现BRAF V600E突变,没有发现其它具有病理意义的突变。已知这种突变诱导BRAF激活,随后激活位于下游的MEK,所以患者参与一项I期口服MEK1/2抑制剂比美替尼(MEK162)的临床研究(NCT01469130),在一个连续 28 天的周期内每天口服两次 45 mg比美替尼。开始比美替尼治疗 2 个月后,患者因肺转移灶快速消退而发生气胸(图1b)。6 个月时,根据CT影像和RECIST v1.1标准,评估为部分缓解(图1c)。开始比美替尼治疗一年后,由于持续的痤疮样皮疹(2级,CTCAE v4.0)以及可能因类固醇软膏(用于皮疹治疗)引起的高血糖(3级),比美替尼剂量减少到每天 30 mg。此后几年未发现肺转移(图1d)。除痤疮样皮疹和高血糖外,未观察到严重不良事件。
比美替尼单药治疗 5 年后,CT显示肺转移灶的重新生长(图1e)。因此,治疗方案改为口服多激酶抑制剂仑伐替尼,标准剂量为 24 mg,每日一次。仑伐替尼使得肺转移灶迅速消失(图1f)。由于患者出现恶心(2级)、呕吐(1级)和高血压(3级),剂量调整为每日 14 mg,持续 5 天,间隔 2 天。在仑伐替尼治疗的过去 5 年中,CT影像显示肺转移灶仍保持收缩。
讨 论
本病例支持MEK抑制剂单药治疗作为BRAF突变阳性PTC的替代治疗方法。丝裂原活化蛋白激酶(MAPK)通路转导细胞外信号,调节多种生物学功能,包括细胞增殖。家族成员MEK1和MEK2被RAF介导的磷酸化激活,进而激活细胞外信号调节激酶(ERK)。因此,抑制RAF或MEK可以阻断BRAF V600E突变引起的RAS/RAF/MEK信号通路持久性(配体独立)激活(图2)。然而,与BRAF抑制剂单药治疗相比,同时抑制RAF和MEK在缓解BRAF突变阳性黑色素瘤方面显示出更好的长期疗效,这是通过推迟耐药性出现并降低发展为鳞状细胞癌的风险而实现的。基于这些信息,美国食品和药品监督管理局(FDA)已经批准BRAF/MEK抑制剂组合用于BRAF V600E突变泛实体瘤治疗。
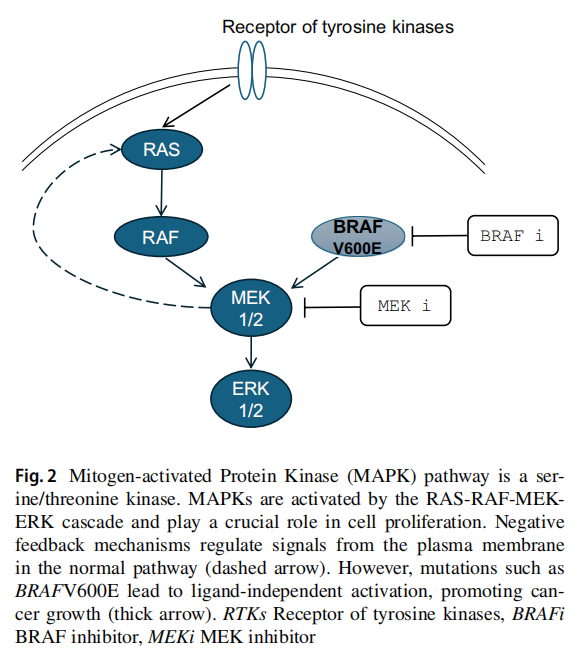
▲图2 丝裂原活化蛋白激酶(MAPK)通路是一种丝氨酸/苏氨酸激酶
与BRAF/MEK抑制剂联合治疗相比,有关MEK抑制剂单药治疗BRAF突变阳性癌症的报道很少。BRAF突变阳性转移性黑色素瘤的III期METRIC研究报道,与细胞毒性化疗相比,接受曲美替尼单药治疗的患者无进展生存期(PFS)得到改善(4.9 个月 vs. 1.5 个月)。然而,BRAF突变阳性黑色素瘤的III期COMBI-d研究发现,与达拉非尼单药相比,达拉非尼/曲美替尼联合治疗的PFS更长(11 个月 vs. 8.8 个月)。先前的临床研究也报道,在BRAF突变阳性结直肠癌和卵巢低级别浆液性癌中,MEK抑制剂单药治疗的有效性低于联合治疗。此外,曲美替尼的一项篮子试验结果显示,对于不表达BRAF V600E的实体瘤和淋巴瘤,临床获益率仅为 34%(11/32),中位PFS仅为 1.8 个月。此外,回顾类似的研究(表1),有一个静脉注射MEK抑制剂的黑色素瘤病例显示出长期肿瘤抑制(>8 年);另一个低级别神经胶质瘤病例对曲美替尼反应超过 12 个月,而其他病例没有表现出明显的反应或反应持续长达几个月。
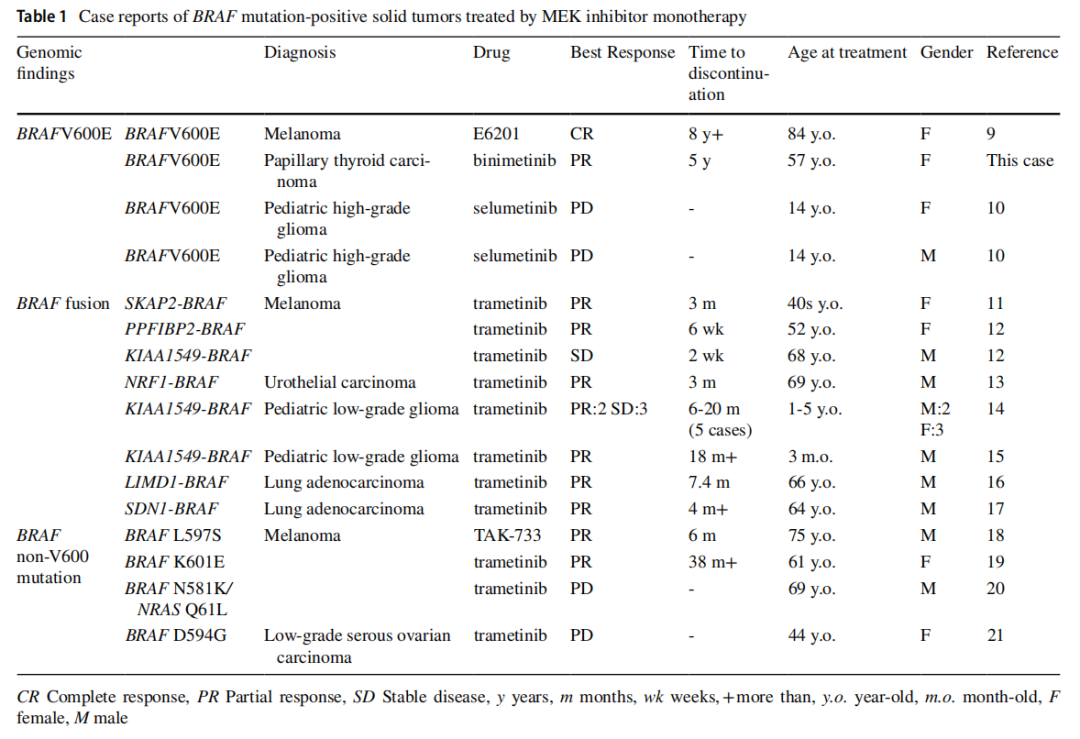
▲表1 MEK抑制剂单药治疗BRAF突变阳性实体瘤的病例报告
本病例提示BRAF突变阳性的PTC对MEK抑制剂单药治疗反应良好。虽然本文病例可能是个特例,但具有这种特征的实体瘤似乎也对其它MEK抑制剂单药治疗敏感。例如,一项研究口服MEK1/2抑制剂司美替尼(selumetinib)的II期试验发现,在携带BRAF V600E突变的碘难治性PTC患者的中位PFS比BRAF野生型PTC患者更长。然而,司美替尼不如联合治疗有效,对于BRAF V600E突变阳性实体瘤,BRAF/MEK抑制剂组合是标准治疗方案,因此MEK单药治疗可能是因不良事件或其他原因无法接受BRAF抑制剂治疗患者的选择。
最后,有趣的是,仑伐替尼在比美替尼治疗复发后表现出持续缓解,这表明选择性MEK抑制剂和多激酶抑制剂在BRAF突变阳性的PTC中不具有相同的耐药机制。
总之,本文报告了一例BRAF V600E阳性PTC对MEK抑制剂单药治疗有长期反应。减少药物的使用数量并避免那些非特异性药物的应用可能会降低治疗费用和不良事件的风险。因此,需要进行随机试验来测试MEK抑制剂单药治疗作为BRAF突变阳性甲状腺癌的替代治疗的有效性和安全性。
参考文献:
Takano, Y., Shimokata, T., Urakawa, H. et al. Long-term response to MEK inhibitor monotherapy in a patient with papillary thyroid carcinoma harboring BRAF V600E mutation. Int Canc Conf J (2024). https://doi.org/10.1007/s13691-024-00670-w

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















学习了
27
#甲状腺乳头状癌# #MEK抑制剂#
38