Am J Hematol:边缘区淋巴瘤的诊断和治疗(2023更新)
2023-08-26 聊聊血液 聊聊血液 发表于上海
《American Journal of Hematology》近日发表一篇综述,概述了MZL的生物学、流行病学、临床表现、当前管理策略和复发/难治性疾病管理中新药的新数据。
边缘区淋巴瘤
边缘区淋巴瘤 (MZL) 是第二常见的惰性淋巴瘤,占非霍奇金淋巴瘤 (NHL) 的7%,WHO将MZL分为三种亚型:粘膜相关淋巴组织 (MALT) 淋巴瘤(70%)、脾脏MZL(SMZL,20%) 和淋巴结MZL(NMZL,10%),但该比例存在地理差异。部分MZL 病例表现为晚期,无法确定明确的器官受累模式,通常称为播散性MZL。
MZL各亚型具有异质性临床病理学特征,最佳治疗路径仍存在显著不确定性。《American Journal of Hematology》近日发表一篇综述,概述了MZL的生物学、流行病学、临床表现、当前管理策略和复发/难治性疾病管理中新药的新数据。

MZL 的流行病学和自然史仍不完全清楚。淋巴瘤家族史是 MZL 的显著风险因素。结外 MZL 的遗传和环境风险因素包括感染因子和自身免疫性疾病,如干燥综合征、系统性红斑狼疮和桥本甲状腺炎。初步数据表明,淋巴结 MZL 的显著风险因素为金属工人职业(比值比3.6),而脾 MZL 的显著风险因素包括哮喘状态(比值比2.3)和使用某些类型的染发剂(比值比6.5)。
1.1 CD5-CD10表型的单克隆B细胞淋巴细胞增多症
表型与MZL(CD5-、CD10-) 一致的克隆性 B 细胞淋巴细胞增多症患者如果无淋巴瘤临床特征(如脾肿大或淋巴结肿大),可描述为具有 CD5- CD10-表型的单克隆 B 细胞淋巴细胞增多症(monoclonal B-cell lymphocytosis with a CD5- CD10- phenotype)。约15%随后会发生淋巴增生性疾病,最常见的为SMZL,但也可能进展为其他惰性 B 细胞淋巴瘤,例如淋巴浆细胞淋巴瘤;但与 CLL 型单克隆 B 细胞淋巴细胞增多症不同的是,其似乎没有明确的定量临界值,使得低于该临界值不会进展。在国际共识分类和世界卫生组织血液淋巴系统肿瘤分类第5版中,均曾将其归类为非 CLL 单克隆 B 细胞淋巴细胞增多症(non-CLL monoclonal B-cell lymphocytosis)。
1.1.1 结外边缘区淋巴瘤
结外边缘区淋巴瘤 (EMZL) 多为感染性病原体或自身免疫过程导致慢性抗原刺激并导致炎性淋巴细胞浸润,且可发生于广泛不同的部位,其中胃 EMZL 占病例的>30%,其他常见部位包括眼附属器、唾液腺、皮肤、结膜、肺、甲状腺和乳腺,具有不同的部位特异性病因。特定病因学病原体的最有力证据为,约三分之二的胃 MALT 病例与幽门螺杆菌诱导的慢性胃炎相关;自身免疫性疾病如干燥综合征和桥本甲状腺炎则分别与唾液腺和甲状腺 EMZL 风险增加相关。
根据受累部位不同,其临床表现差异很大,通常EMZL具有惰性行为和有利结局。在 EMZL 中,尤其是胃EMZL中,接触外来抗原和粘膜通透性极为重要。尽管大多数 EMZL 在诊断时为局限期,但约20%为 IV 期,在这种情况下结外播散为典型特征。与 MZL 相关的其他感染包括 SMZL 中的丙型肝炎病毒 (HCV)、结膜和眼附属器中的鹦鹉热衣原体、皮肤 EMZL 中的伯氏疏螺旋体、肠道 EMZL 中的空肠弯曲菌和支气管 EMZL 中的木糖氧化无色杆菌。
EMZL发生组织学转化的预后较差,可能由 TP53 突变、p16蛋白缺失或 MYC 重排所驱动。支持边缘区 B 细胞生长所需的关键信号包括BAFF、CD40、TLR、BCR和 NOTCH 受体信号传导。通过感染或自身免疫引起的慢性抗原刺激可驱动 BCR 介导的刺激、免疫球蛋白重链基因使用偏倚以及调节 NF-kB 通路的信号通路的基因异常,包括t(1;14)、t(11;18)、A20失活和 MYD88 突变。
1.2 诊断和分期
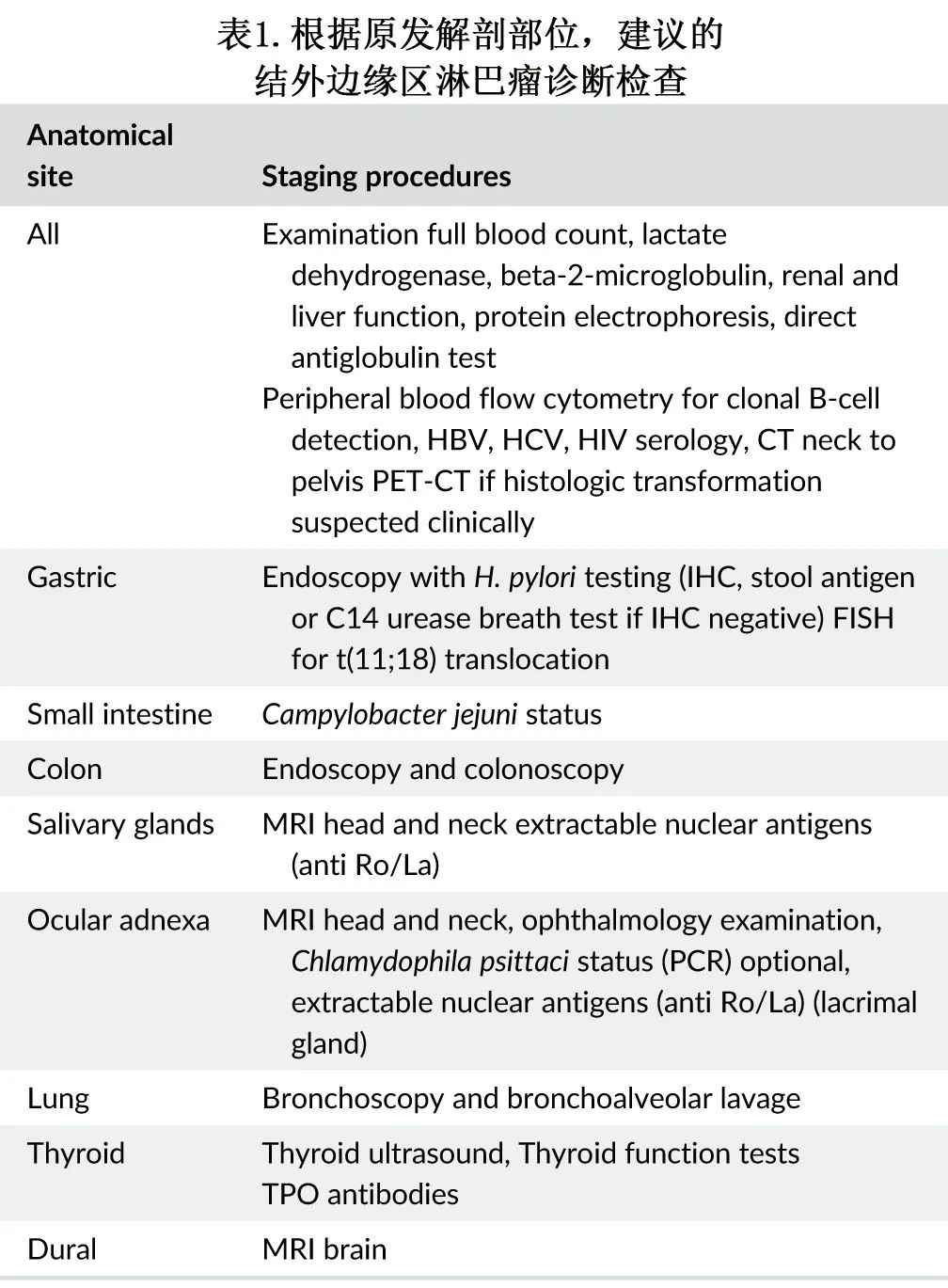
EMZL多为长期局限性,但也有高达25%的病例可发生多灶性单器官受累和全身播散(更多发生在非胃部位)。晚期患者的预后较差,可能需要与局部疾病患者不同的治疗策略。应根据受累部位和任何可能的潜在感染或自身免疫原因定制诊断检查。根据解剖位置进行分期的推荐方法见表1。
1.3 PET-CT
PET-CT在 MZL 分期中的作用不如滤泡性淋巴瘤明确,2014年 Lugano 分类中推荐使用 CT 扫描进行分期。在纳入376例患者的20项研究的荟萃分析中,18F FDG PET-CT 的检出率为71%,但该检出率因解剖部位而异,支气管 (94%) 和头颈部 (90%) 部位的检出率高于胃 (62%) 和眼部 (49%)。Alderuccio 等研究了接受 PET-CT 分期的152例患者,发现78.1%的患者有 FDG 显影病灶(定义为SUVmax > 2),建议在 MZL 研究中使用较低的 SUVmax 阈值。鉴于新数据证实大多数 MZL 为 FDG 显影,即将修订的 Lugano 分类可能推荐 PET-CT 作为分期模式。
与 CT 相比,PET-CT可使3%-42%的患者分期提高,但其对临床结局的影响尚不清楚。如果计划进行局部治疗(如放疗)或担心组织学转化为弥漫性大 B 细胞淋巴瘤,则应考虑 PET-CT 分期。
1.4 骨髓活检的作用
只有不足10%的显性局限性 MALT 淋巴瘤患者存在骨髓受累,无血细胞减少的患者可能免于骨髓活检,因为无论是否进行骨髓活检,影像学定义的IE 期患者均有极佳的淋巴瘤特异性结局。骨髓受累率因 MZL 亚型和评估手段(PET-CT或活检)而异。Alderuccio等描述活检显示EMZL、NMZL和 SMZL 的骨髓受累率分别为15.9%、50.8%和83.3%。与骨髓活检金标准相比,PET-CT在 MZL 亚型中具有较高的特异性 (98.9%-100%) 和阳性预测值 (86.7%-100%),但灵敏度较低 (31.4%-39.4%);EMZL 的阴性预测值最高 (89.6%),NMZL的阴性预测值中等 (61.2%),SMZL的阴性预测值最低 (22.6%)。重要的是,存在骨髓受累与任何亚型的早期治疗失败或较差结局均无关,从而反驳了其在临床实践中的强制性表现。
1.5 预后因素
MALT-IPI可确定可能有助于预后判断的三个因素(晚期疾病、年龄≥70岁和血清 LDH 升高)。在来自梅奥分子流行病学资源的一个队列中,国际预后指数对比滤泡性淋巴瘤国际预后指数后显示,MALT-IPI测量 PFS 和 OS 的能力最高(使用一致性统计)。此外基于PFS,专门为具有不同临床行为的 EMZL 设计了包含4个因素(年龄>60岁、血清 LDH 升高、III/IV期和多个粘膜部位)的修订MALT-IPI。与其他淋巴瘤亚型一样,早期疾病进展与较差的预后相关。在梅奥队列中,12个月时达到无事件生存期的患者的 OS 与一般年龄匹配人群相似,而在12个月或24个月内复发或进展的患者 OS 显著较差,标准化死亡率比分别为3.14和2.31。Conconi 等人在对IELSG-19 研究中接受免疫化疗的患者进行的分析报告了类似的观察结果。高 MALT-IPI 可预测早期疾病进展,在占比为18%的 POD24 患者中,10年 OS 为64%,而对照组为85%(风险比2.42)。在524例美国患者队列中,27%的患者在开始系统治疗后24个月内发生疾病进展(POD24),其组织学转化率较高,且在校正不良预后因素后OS较差。在观察性 NF10 研究中发现了相似的结果,18%(59/321) 的 MZL 患者发生 POD24 事件,导致3年 OS 为53%,而未发生 POD24 事件的患者为95%。
最近开发的适用于所有 MZL 亚型的预后指数为MZL-IPI。观察性 NF10 研究入组510例混合患者,包括NMZL(12%)、SMZL(33%)、EMZL(39%) 和播散性MZL(无法准确分型-16%),研究者多变量分析发现血清 LDH 升高、贫血、外周血淋巴细胞减少症、血小板减少症和亚型(NMZL或播散性MZL)是与结局较差独立相关的因素。使用这些要素得出了5因素风险评分,将患者分为3组之一,低、中和高危组的5年 PFS 率分别为85%、66%和37%。在训练集和验证集中,相对于IPI、FLIPI和MALT-IPI,MZL-IPI与更优的预测和辨别相关,也是 OS 的预后因素,该模型广泛适用于所有 MZL 亚型。
1.6 当前治疗
1.6.1 局限性疾病
胃MZL
大多数胃 MALT 淋巴瘤患者有幽门螺杆菌感染的证据,包括 C14 脲酶呼气试验活检和/或粪便抗原,阳性结果均应提示质子泵抑制剂联合二联或三联抗生素的根除治疗。单纯根除幽门螺杆菌可使75%的病例胃 MALT 淋巴瘤消退。患者应在根除后≥6周和停用质子泵抑制剂后≥2周重复进行幽门螺杆菌检测,以确保根除,并应在确认成功根除后不早于3个月进行重复内镜检查。患者通常会出现肉眼可见的改善,但组织学疾病持续存在,在这种情况下,许多患者最终会在稍后的时间点达到完全缓解。因此在大多数指南中,在定义为难治性疾病和转换为另一种治疗之前,建议进行至少12个月的内镜监测。
携带t(11;18) 易位和幽门螺杆菌阴性患者对幽门螺杆菌根除治疗的缓解率较低,放疗为标准治疗。经验性根除治疗可在希望避免辐射暴露的症状轻微患者中进行试验,但仅15%的病例缓解,携带t(11;18) 的患者甚至更少。在根除治疗未能达到疾病缓解的情况下,受累部位放疗是一种合理手段,使用中等剂量(3-4周20-30 Gy)可获得良好的结局。一项纳入局限性胃或非胃 MALT 淋巴瘤患者的研究中,10年总生存率和无复发生存率分别为87%和76%,原因特异性生存率为98%。其他治疗选择包括利妥昔单抗单药治疗和化学免疫治疗,如利妥昔单抗+苯丁酸氮芥或R-CVP,但治疗的毒性高于单独 CD20 治疗。胃切除术可导致显著的发病率,不再推荐。
眼附属器
眼附属器 EMZL 占 EMZL 的8%,且MZL是累及眼附属器的最常见淋巴瘤组织学亚型。大多数患者为 I/II 期,可省略广泛的分期检查,因为骨髓活检(1.7%阳性)和胃镜检查 (2.3%) 很少显示淋巴瘤受累,且无论疾病分期如何OS结局均极佳。一些研究者发现眼附属器 MALT 与鹦鹉热衣原体相关,但存在相当大的地理异质性。多西环素或克拉霉素的缓解率为45%-65%。IELSG39 研究对 IAE 期眼 EMZL 患者进行为期6个月的多西环素 100mg治疗,每日两次治疗4周然后停药4周,以使巨噬细胞内的非活性细菌被重新激活并对抗生素敏感,重复3次(共持续6个月)。在入组的44例患者中,PCR 检测到65%的患者携带鹦鹉热衣原体。中位随访83个月,2年和5年 PFS 率分别为75%和55%,表明长期脉冲式抗生素暴露可改善疾病控制。此外,部分鹦鹉热衣原体阴性病例中也报告了使用抗生素的疾病消退。因此,在患病率较高且对视力无直接威胁的地区,可考虑进行根除治疗的经验性试验。眼眶检查推荐头部MRI,全身CT 可用于寻找眼外受累。PET-CT 很少优于CT,因此不需要。虽然手术切除适用于容易到达的结膜或泪道部位,但累及球后位置应及时考虑累及野放疗。常规使用剂量为24-36 Gy,但大多数患者可发生晚期毒性(如白内障和干眼症),此外视网膜病变更令人关注但频率较低。使用较低剂量(例如4 Gy)可能是可行策略,可提供明确控制且减少眼部毒性,但仍需更长随访来证实真正持久的局部控制。
肺或支气管
支气管 EMZL 是最常见的肺实质淋巴瘤,占病例的70%~90%;此外仅次于胃、脾和眼,是最常见的结外受累部位。具有中心审查组织学的最大病例系列为 IELSG 研究,包括205例患者,中位年龄为62岁,女性略占优势,86%的患者就诊时为Ⅰ期或Ⅱ期;半数在就诊时有症状(咳嗽、呼吸困难、胸痛)而15%出现全身症状,半数无症状。纪念梅隆凯瑟琳癌症中心的系列研究纳入了200例患者,中位随访60个月以上,手术切除的 EFS 优于主动监测和系统治疗(6年EFS:分别为74% vs. 65% vs. 62%);但可能存在与疾病范围相关的选择偏倚,因为选择切除的患者中有90%仅有单个病灶。与慢性感染的相关性仍在研究中:木糖氧化无色杆菌是一种革兰氏阴性β-变形杆菌,毒力较低,但抗生素耐药性较高,在支气管 EMZL 57/124(46%) 的频率高于对照的15/82(18%),表明可能存在机制联系需要进一步证实。须获得足够的材料进行活检。手术切除的结局似乎有利,可能反映出切除病灶的尺寸通常较小。仅接受活检且存在残留淋巴瘤的患者可接受放疗。更晚期的患者如果肿瘤负荷高可以使用利妥昔单抗单药治疗,如果没有症状可以观察。
硬脑膜
硬脑膜淋巴瘤是一种不常见的 CNS 淋巴瘤,通常为EMZL,而非弥漫性大 B 细胞淋巴瘤。考虑到描述该疾病的文献均来自小病例系列,且确切发生率未知。其临床表现因肿瘤的大小和位置而异,可包括癫痫发作、头痛和颅神经麻痹,但也有部分患者可在因另一指征行神经影像学检查时偶然诊断。由于与脑膜瘤外观相似,可导致放射学误诊。女性占优势。大多数原发性硬脑膜 EMZL 患者接受手术切除,因为术前可能认为诊断为脑膜瘤。在活检后确认EMZL的患者中,单纯放疗似乎可实现极佳的疾病控制。系统治疗可保留用于脑实质受累或 CNS 外表现的患者。
结肠
结肠 EMZL 较为罕见,且仅限于小病例系列,估计占 EMZL 的2%,临床表现介于 GI 出血、肠套叠、肠梗阻和腹部 CT 肿块至结肠镜筛查期间的无症状检测。在一个系列中,9例患者中的3例也患有胃EMZL,尽管所有3例患者均存在幽门螺杆菌,但成功根除对结肠 EMZL 无影响。由于罕见性而不存在标准化治疗路径,观察、息肉切除术、手术切除放疗、免疫化疗和利妥昔单抗的使用数量太少,无法进行有意义的比较。息肉切除术时偶然切除病灶的IAE 期患者可以安全地观察,因此应根据患者特点和临床表现给予个体化治疗。总体结局似乎有利,淋巴瘤特异性死亡率相对较低(监测、流行病学和最终结果数据库分析中15年时为10.6%)。
甲状腺
原发性甲状腺 EMZL 罕见,估计自身免疫性甲状腺炎患者中0.5%发生。病例报告和系列的荟萃分析确定了34例患者,其中71%有自身免疫性甲状腺炎背景、7%有甲状腺癌背景。治疗方法各不相同,包括手术切除联合或不联合免疫化疗,患者结局良好,仅报告了2例复发。
唾液腺
唾液腺 EMZL 具有明显的女性优势 (1:3),可能归因于与自身免疫性疾病密切相关,约三分之一的病例有既往史(最常见的是干燥综合征)。GPR34 易位和突变导致恶性 B 细胞的旁分泌刺激和唾液 EMZL 的淋巴瘤形成,但其总体突变负荷似乎低于非干燥综合征相关EMZL,且依赖于刺激微环境。无论采用何种主要治疗预后均良好。根据 NCCN 指南,某些研究中心可以考虑手术,特定无症状患者也可观察。由于口干恶化和长期牙齿并发症的风险较高,放疗不太受支持。
其他部位
关于其他亚型对抗生素应答率的数据有限,病例系列显示,在接受疏螺旋体抗生素治疗(头孢曲松)的11例病例中,6例的皮肤 EMZL 消退,大多数患者为肠道EMZL。放疗是非胃I期结外 MZL 的合理标准治疗。II期研究确定累及野放疗是局限性非胃 MALT 淋巴瘤的合理手段,5年无进展生存期 (PFS) 和总生存期 (OS) 分别为79%和95%。
1.7 原发性皮肤边缘区淋巴增生性疾病
最近发现的一个独立临床病理实体,原发性皮肤边缘区淋巴增生性疾病(Primary cutaneous marginal zone lymphoproliferative disorder)具有高度有利的预后和100%的疾病特异性生存率。约占原发性皮肤 B 细胞淋巴增生性疾病的1/3,很容易通过局部 RT 治疗,但约半数患者发生皮肤复发,且多灶性表现的患者风险较高。
1.7.1 晚期疾病
晚期 EMZL 与晚期 FL 一样,均无法治愈,应推迟治疗直至出现症状。惰性行为意味着初始观察适用于大多数患者,对于需要治疗的患者,免疫化疗是标准治疗。基于几项前瞻性研究和一些大型观察性系列研究,苯达莫司汀和利妥昔单抗 (BR) 得到广泛使用。比较 BR 与 R-CHOP 的大型随机 StiL 研究中纳入了67例 MZL 患者,两方案之间未观察到差异。同样,BRIGHT研究者发现在46例 MZL 患者中,BR组和 R-CHOP/R-CVP 组的 CR 率无差异。一项2期研究纳入60例年龄<85岁、任何部位发生的初治 EMZL 患者,旨在探索BR(无利妥昔单抗维持治疗),还纳入了幽门螺杆菌根除治疗失败的胃 EMZL 患者和局部治疗难治的皮肤 EMZL 患者。该研究对缓解进行了调整:3个周期后进行中期CT,CR/CRu患者仅再接受1个周期(共4个周期),其他患者均接受6个周期的治疗。结果大多数患者 (75%) 只需要4个周期的治疗,4例患者 (7%) 因毒性提前终止苯达莫司汀治疗;该研究符合其主要终点,2年 EFS 率为93%,中位随访43个月,4年 EFS 和 OS 率分别为93%和96%。一项BR治疗患者 (n=237) 的大型观察系列显示相似结果,ORR为92%(CR 81%),估计的3年 PFS 和 OS 分别为80.5%和89.6%。德国前瞻性登记研究数据中也发现了类似的结果,值得注意的是20%的患者接受利妥昔单抗维持治疗,与 PFS 延长相关,但与 OS 无关。IELSG19 研究者将454例患者随机分配至苯丁酸氮芥单药治疗组或苯丁酸氮芥+利妥昔单抗组,方案修正案增加了第三组利妥昔单抗单药治疗。中位随访7.4年,联合治疗组的5年 EFS 率为68%,苯丁酸氮芥单药组为51%,利妥昔单抗单药组为50%(p=0.009),因此该非强化且耐受性良好的治疗方案是这种情况下的合理标准治疗。
1.7.2 利妥昔单抗维持治疗
有研究阐述了免疫化疗后利妥昔单抗维持治疗在 MZL 中的作用。在 III 期 StiLNHL72008 MAINTAIN 研究入组了119例初治 EMZL 和 SMZL 患者,采用 BR 治疗,随后随机接受利妥昔单抗维持治疗2年或观察。随访76个月后,利妥昔单抗维持治疗的 PFS 更优(中位未达到vs.观察92.2个月(风险比 [HR]=0.35%,p=0.008));6年后利妥昔单抗维持治疗组的 OS 率为92%,观察组为86%,无显著差异。II 期研究给予苯丁酸氮芥+利妥昔单抗诱导后皮下利妥昔单抗维持治疗,5年 EFS 为87%,与 IELSG19 研究的苯丁酸氮芥+利妥昔单抗组相比更佳,但该比较为非随机对比。COVID 大流行改变了利妥昔单抗维持治疗的感知获益与风险。综上所述,免疫化疗后利妥昔单抗维持治疗似乎可能导致 PFS 延长,而毒性未显著增加,但对总生存期无影响,因此不推荐常规使用。
1.8 淋巴结边缘区淋巴瘤
淋巴结 MZL(NMZL) 约占 MZL 的10%,占所有 NHL 的<2%。由于其罕见性,对该疾病的了解极具挑战性,且 NMZL 历史上在临床试验中常与滤泡性和小淋巴细胞淋巴瘤合并。NMZL 多为惰性,通常在就诊时呈播散性。与丙型肝炎感染相关,但自身免疫比其他 MZL 亚型更少见。就诊时常见膈上淋巴结肿大,特别是累及头颈部,分别有1/3和1/2的患者为肿瘤直径>5cm和Ⅲ/Ⅳ期。约10%的病例中可检测到 IgM 异常蛋白,可能导致诊断与华氏巨球蛋白血症混淆,而检测 MYD88 L265P 突变可能有帮助,因为其存在于95%的华氏巨球蛋白血症中,但NMZL中<10%。PTPRD突变存在于20%的 NMZL 中,并且似乎对该疾病具有特异性。
淋巴结 MZL 的病理学特征与脾脏和结外 MZL 相似,可能导致诊断困难,尤其是累及脾脏或结外部位时。尽管 FLIPI 的使用结果各不相同,但尚无专门针对淋巴结 MZL 开发的预后系统。年龄增长和晚期具有不良预后影响。
一般而言,滤泡性淋巴瘤的免疫化疗方案适用于有症状的 NMZL 患者。局限性疾病采用放疗治疗,而无症状、低肿瘤负荷、晚期疾病可以安全地观察。在与丙型肝炎感染相关的 NMZL 中,感染根除治疗可使大多数患者的淋巴瘤消退,无需紧急淋巴瘤缓解,应将其用作初始治疗策略。尽管缺乏前瞻性研究,但利妥昔单抗的免疫化疗通常是症状性晚期患者的标准治疗。一项倾向匹配分析比较利妥昔单抗单药治疗与免疫化疗,免疫化疗无 OS 优势,表明利妥昔单抗单药治疗是一种合理的选择,尤其是在低危患者中。已经探索用于其他惰性 B 细胞淋巴瘤亚型(如滤泡性淋巴瘤)的多种方案,包括R-CVP、R-CHOP和BR。此外由于毒性,氟达拉滨方案不常规使用。
1.9 脾边缘区淋巴瘤
脾 MZL(SMZL) 占所有淋巴恶性肿瘤的2%,MZL的20%。中位生存期为8-10年,但5%-10%发生组织学转化为弥漫性大 B 细胞淋巴瘤。1/3无症状患者可安全观察。
NOTCH 通路和其他边缘区分化相关基因经常发生突变,高达60%的 SMZL 患者;KLF2 转录因子的突变可导致 NF-kB 信号的激活,是另一个常见的遗传事件。虽然明确诊断最好采用脾脏组织学,但在临床实践中通常结合外周血淋巴细胞形态(双极细胞质绒毛突起和圆形细胞核)、免疫表型和临床表现(脾肿大、淋巴细胞增多和血细胞减少)亦可作出诊断。25%的 SMZL 发生脾门淋巴结肿大,但外周淋巴结肿大罕见,可发生自身免疫性溶血性贫血等自身免疫现象。CT 扫描足以进行分期,而PET-CT可保留用于怀疑组织学转化的患者。
与其他 MZL 亚型一样,无症状患者可观察管理。症状性脾肿大、血细胞减少或全身症状是治疗指征。一线治疗选择包括脾切除术、利妥昔单抗单药治疗和免疫化疗,虽然这三种方法尚未直接比较,但通常首选利妥昔单抗单药治疗或免疫化疗。
1.9.1 脾切除术
利妥昔单抗单药治疗之前脾切除术是主要的治疗方法,尽管也有确诊的益处,但其在当代管理中已经失去优势。在大多数病例中,脾芯针活检也可以安全地得出诊断,同时避免脾切除术。尽管如此,脾切除术仍可控制疾病并改善血细胞减少,也可能是特定患者的有用方案,例如利妥昔单抗、BTK抑制剂难治性疾病。通过腹腔镜方法和静脉血栓栓塞预防可减少围手术期短期并发症。在择期脾切除术(或脾切除术后)前至少2周接种疫苗和预防性抗生素,可将包裹性细菌感染的晚期风险降至最低。
1.9.2 免疫化疗
免疫化疗适用于伴有播散性疾病、全身症状和/或高级别转化的fit患者。R-CVP 和 R-CHOP 均常用于滤泡性淋巴瘤,可给予SMZL 患者;但在一项前瞻性 II 期研究中,R-COMP(利妥昔单抗联合环磷酰胺、长春新碱、非聚乙二醇化脂质体多柔比星和泼尼松)的客观缓解率 (ORR) 仅有84%,6年 PFS 为54%。在 II 期 BRISMA/ELISG36 研究中,56例 SMZL 患者接受了 BR 治疗,ORR和 CR 率分别为91%和73%,3年 PFS 和 OS 分别为90%和96%,且未观察到非预期毒性;因此BR是其积极且可耐受的治疗方案选择。
与不维持治疗相比,在淋巴结和 SMZL 患者中初始 BR 治疗后使用利妥昔单抗维持治疗2年可延长PFS(但未延长OS)(HR=0.35,p=0.008)。观察性研究也证实这一结论。
1.9.3利妥昔单抗单药
一项大型回顾性系列研究中利妥昔单抗单药治疗的 ORR 为92%,10年无进展率为64%。RESORT 研究用 375 mg/m2 每周4次治疗患者,然后患者随机分配到观察组和利妥昔单抗维持组,维持治疗组的至治疗失败时间和 PFS 显著改善。单药利妥昔单抗(短期或长期给药)已成为大多数患者的首选方法,单药策略无应答的患者可使用脾切除术或免疫化疗。最近的单机构数据报告,CD5表达(虽然在 MZL 中罕见)与利妥昔单抗单药治疗后较低的 ORR 相关,但与 BR 无关,表明如果需要全身治疗,可能首选BR。CD5 表达的部分不利影响可能是由于其与复杂核型和/或 TP53 缺失相关,但未对这些因素进行单独分析。
1.9.4 组织学转化
组织学转化为弥漫性大 B 细胞淋巴瘤与预后不良和总生存期较差相关。组织学转化的年发生率约为每年1%。初始治疗未达CR、血清乳酸脱氢酶水平升高、诊断时淋巴结部位>4个、累及多个粘膜部位、CD5表达和脾脏 MZL 以及复杂核型与组织学转化风险增加相关。组织学转化的 SMZL 患者的基因组复杂性、TNAIFP3、TP53改变、CDKN2A/B丢失和 6p 增加更高。
1.10 MZL的新药
1.10.1 BTK抑制剂
一项伊布替尼研究中63例患者中位年龄为66岁,中位既往治疗线数为2;MALT 淋巴瘤 (51%) 是最常见的 MZL 亚型,其次为淋巴结 (27%) 和脾 (22%)。贫血 (14%)、感染性肺炎 (8%) 和疲乏 (6%) 是最常见的≥3级治疗中出现的不良事件 (TEAE);59%的患者发生出血事件,除1例达肝素治疗性抗凝患者发生5级脑出血外,其余均为1-2级;房颤4例 (6%)。中位随访33.1个月,ORR为58%,中位 DOR 为27.6个月,中位 PFS 为15.7个月,未达到中位OS。结外、淋巴结和脾 MZL 的 ORR 分别为63%、47%和62%。KMT2D 和 CARD11 突变与 DOR 较差相关。
维奈克拉在复发性/难治性细胞淋巴瘤(包括MZL)患者的 I 期研究中显示出活性。尚未进一步探索其单药治疗 MZL 的情况,但在一项小型 II 期研究中研究了伊布替尼与 BCL2抑制剂联合治疗,期中分析显示第16周的 ORR 为 84%(CR 42%)。
在单臂 II 期 MAGNOLIA 研究中评估泽布替尼,既往接受过≥1线治疗的MZL 患者接受泽布替尼 160mg 治疗每日2次。68例患者中常见亚型为MALT(38%)、淋巴结 (38%) 和脾 (18%),6%不确定。患者既往接受过中位2线治疗,ORR为68%(CR 26%),MZL亚型之间的 ORR 率相似;估计15个月 PFS 率为82.5%。最常见的 TEAE 为腹泻 (22%)、青肿 (21%) 和便秘 (15%),最常见的≥3级 TEAE 为中性粒细胞减少症 (10%);房颤和高血压各有3%的患者发生。MYD88 和 TNFAIP 突变与有利 PFS 相关 (HR=0.09),KMT2D与较差 PFS 相关 (HR=6.5)。此外在疾病进展的2例患者中发现了 BTK 和 PLCG2 的获得性突变。
在43例 MZL 患者中探索了阿可替尼。中位随访13.3个月,ORR为53%(CR 13%),估计中位 PFS 为27.4个月。
伊布替尼+利妥昔单抗联合治疗初治 MZL 患者的IELSG47/MALIBU研究对 SMZL 和 NMZL 患者进行初步分析,在45例患者(SMZL组30例,NMZL组15例)中ORR为91%(CR 49%),整个队列的2年 PFS 率为77%(SMZL组86%,NMZL组59%)。最常见的≥3级不良事件为中性粒细胞减少症 (20%) 和皮疹 (9%);3级房颤 (2%) 和高血压 (4%) 不常见。III 期随机 SELENE 研究考察了复发性/难治性 FL 或 MZL 患者(占13.9%)在免疫化疗(R-CHOP或BR)基础上加用伊布替尼的影响。大多数 (90%) 患者接受BR,研究未达到主要终点PFS(总体或 MZL 队列);伊布替尼组腹泻、恶心、疲乏、皮疹、发热、呕吐、咳嗽、贫血和血小板减少症的发生率更高。由于 III 期研究结果为阴性,伊布替尼的 MZL 适应症已自愿退出。虽然可以超说明书使用,但由于泽布替尼或阿可替尼的安全性特征相对更佳,因此是首选。
1.10.2 新型CD20单抗
III 期随机对照 GALLIUM 研究对比奥妥珠单抗或利妥昔单抗联合化疗(苯达莫司汀、CVP或CHOP),主要纳入初治滤泡性淋巴瘤患者,但分别入组了195例 MZL 患者并进行随机分组;研究没有足够的效力专门显示两组间 MZL 的 PFS 差异,中位随访59.3个月后奥妥珠单抗组和利妥昔单抗组的 PFS 无显著差异(4年 PFS 率分别为72.6%和64.1%),风险比为0.79,且队列之间的 OS 相似。奥妥珠单抗组3-5级不良事件的发生率更高 (86.1 vs. 77.4%),5级事件的发生率更高 (14.9% vs. 9.7%),但全因死亡更少 (19.2% vs. 22.9%)。因此无法得出结论,奥妥珠单抗与利妥昔单抗相比是否可改善初治 MZL 患者。
1.10.3 PI3K抑制剂
PI3Kδ抑制剂 idelalisib 是首创药物,在一系列惰性 B 细胞恶性肿瘤(包括MZL)中具有显著活性。虽然惰性淋巴瘤的 III 期研究已经开始,但idelalisib 与化学免疫治疗和其他新药联合使用时毒性相当大,进一步的临床开发已停止。其他 PI3K 抑制剂包括copanlisib、umbralisib、parsaclisib和zandelisib,但由于担心 III 期研究的毒性和 OS 结果,所有先前获批的 PI3K 抑制剂均已撤市,因此此类药物在淋巴瘤中不太可能发生进一步的临床开发。
1.10.4 CAR-T治疗
CAR-T研究的重点是侵袭性组织学亚型,但少数研究集中于惰性淋巴瘤患者。ZUMA-5 是一项正在复发性/难治性惰性 B 细胞淋巴瘤患者中进行的 axicabtagene ciloleucel (axi-cel)II 期研究,纳入22例既往接受过≥2线治疗(包括 CD20 单克隆抗体联合烷化剂)的 MZL 患者,MZL 患者的中位年龄为66岁,中位既往治疗线数为3,52%的患者在接受 CD20 和基于烷化剂的治疗后发生过 POD24 事件。MZL 患者的 ORR 为85%(60%CR),中位随访12.1个月中位 PFS 为11.8个月,估计的12个月 OS 率为92.9%。所有22例 (100%) 患者均发生细胞因子释放综合征,其中2例 (9%) 发生≥3级事件,15例 (68%) 需要托珠单抗治疗。神经毒性的发生率很高:17例 (77%) 发生任何神经系统事件,其中9例 (41%)≥3级。14例 (64%) 患者需要使用类固醇。值得注意的是,MZL患者中≥3级神经毒性的发生率高于同一研究的 FL 队列 (15%),且 MZL 患者中与 axi-cel 毒性相关的分析指标的中位增幅高于 FL 患者。
1.10.5 其他新药
来那度胺和利妥昔单抗广泛用于FL,联合治疗对 MZL 也有效。AUGMENT 研究纳入了63例复发性/难治性 MZL 患者(占研究人群的18%),并将其随机分配至利妥昔单抗组或利妥昔单抗联合来那度胺组。研究表明联合来那度胺可改善PFS (HR=0.46),但在 MZL 子集中无显著性。在初治患者中进行的 II 期研究得出的 ORR 为93%(70%CR),MZL 子集的长期随访报告中,中位 PFS 为59.8个月,5年 OS 为96%。IELSG40 研究中来那度胺联合克拉霉素,研究纳入了44例复发性/难治性 EMZL 患者;ORR为44%,2年 PFS 率为53%,毒性特征相对有利,但明显低于其他基于来那度胺的联合治疗,与克拉霉素单药治疗相似。
CD20XCD3 双特异性抗体正在一系列 B 细胞淋巴瘤中迅速发展,尽管mosunetuzumab、epcoritamab和 glofitamab的 I 期剂量递增研究中纳入了少数 MZL 患者,但尚未报告 MZL 的专门 II 期队列。考虑到在 DLBCL 和 FL 中观察到的有利疗效和毒性,这些药物可能对 MZL 也有效。
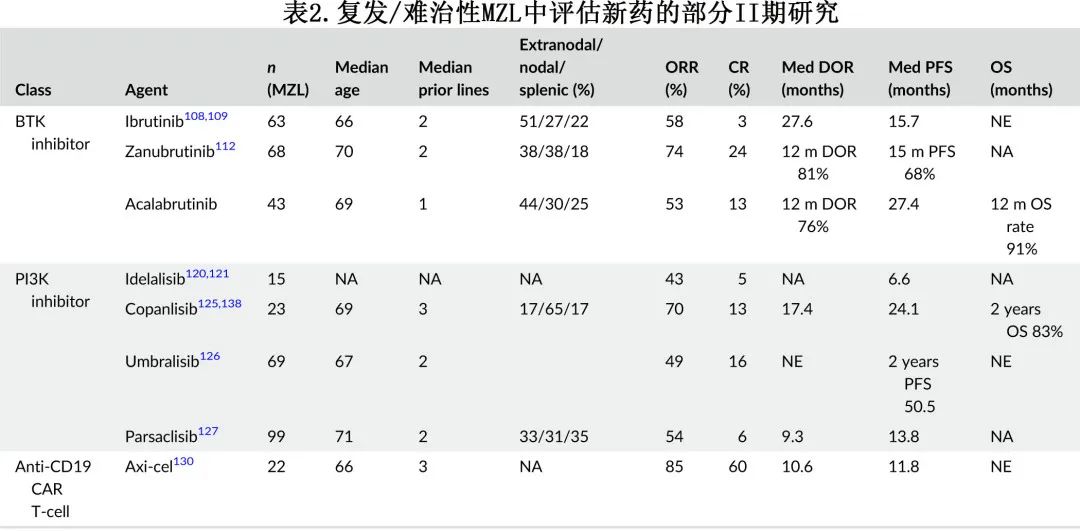
MZL 中评估的新药总结见表2。
总结
MZL 是一种惰性 B 细胞淋巴瘤,临床表现、生物学、病因学和治疗具有相当大的异质性。大多数局限期 MALT 淋巴瘤患者采用抗生素(幽门螺杆菌相关胃MALT)或放疗(胃和非胃部位)预后极佳。在无症状的情况下脾MZL可观察,而有症状的患者可在需要时接受利妥昔单抗单药治疗或免疫化疗。NMZL 患者可以使用与滤泡性淋巴瘤相似的原则和免疫化疗方案进行管理。MZL-IPI可用于所有 MZL 亚型的预测。组织学转化罕见,但与较差的结局相关,应使用以蒽环类药物为基础的免疫化疗进行管理。BTK 抑制剂、免疫调节剂等新型靶向药物对复发/难治性疾病患者有效。目前,CAR-T细胞治疗在 MZL 中的作用仍在多项试验中进行研究。未来的研究将定义更活跃的新型组合。
参考文献
Cheah CY, et al.Marginal zone lymphoma: 2023 update on diagnosis and management.Am J Hematol . 2023 Aug 21. doi: 10.1002/ajh.27058.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言