“不可成药”逆袭治疗多种适应症,一文盘点在研实力KRAS G12C抑制剂
2023-05-08 找药宝典 网络 发表于上海
一文盘点在研实力KRAS G12C抑制剂。
在过去40年里,KRAS由于结构特点等原因被认为不可成药。直到2021年5月28日,第一个针对KRAS G12C的抑制剂Sotorasib(AMG510)被美国FDA加速批准上市,打破了KRAS突变无靶向药的僵局。
除了AMG510被批准之外,Adagrasib(MRTX849)是第二款被FDA批准上市的KRAS G12C抑制剂,它于2022年12月12日被美国FDA批准用于治疗转移性非小细胞肺癌患者。此外,来自KRYSTAL-1的CRC队列的数据支持Adagrasib加西妥昔单抗(爱必妥)在KRAS G12C突变的晚期 CRC患者中的突破性治疗指定,这些患者的癌症在先前接受化疗和抗 VEGF治疗后出现进展。
KRAS G12C在实体瘤中普遍存在
KRAS G12C 变体在几种实体瘤中普遍存在,并且作为致癌驱动因素在 NSCLC 中约占 14%,在 CRC 中约占 3% 至 4%,在阑尾癌中约占 3% 至 4%,在卵巢癌中约占 0.4%,在卵巢癌中约占 1% 至 3 %在 PDAC 中,小肠癌为 1% 至 3%,胆道癌为 1%,子宫内膜癌为 1.5%。
Adagrasib 挑战晚期实体瘤
2023年4月ASCO全体会议介绍了KRYSTAL-1Ⅱ期研究 (NCT03785249) 的最新发现,Adagrasib单药在KRAS G12C 突变实体瘤患者中表现出可控的安全性和有意义的临床活性。
在 1/2 期研究中接受共价 KRAS 抑制剂治疗的实体瘤患者(不包括结直肠癌 (CRC) 和非小细胞肺癌(NSCLC;n = 57))的客观缓解率 (ORR) 为 35.1。在 2022 年 10 月 1 日的数据截止日期,中位随访时间为 16.8 个月,中位无进展生存期 (PFS) 为 7.4 个月(95% CI,5.3-8.6)。6 个月和 12 个月的 PFS 率分别为 56.5% 和 17.7%。中位总生存期 (OS) 为 14.0 个月(95% CI,8.5-18.6),6 个月和 12 个月的 OS 率分别为 84.0% 和 53.5%。
中位治疗持续时间为 5.3 个月,中位反应时间为 1.4 个月,8.8% 的患者出现疾病进展。疾病控制率 (DCR) 为 86.0%,其中 50.9% 的患者病情稳定。
adagrasib在胰腺导管腺癌(PDAC)和胆道癌(BTC)患者中的临床活性值得注意,因为化疗在二线环境中对这些患者人群的临床活性有限。
PDAC 患者 (n = 21) 经证实的 ORR 为 33.3%,DCR 为 81.0%,中位 PFS 为 5.4 个月(95% CI,3.9-8.2),中位 OS 为 8.0 个月(95% CI,5.2 -11.8)。PDAC 患者的 6 个月 PFS 率为 49.3%。该人群的 6 个月和 12 个月 OS 率分别为 69.7% 和 14.0%。
相比之下,BTC 患者(n = 12)的确认 ORR 为 41.7%,DCR 为 91.7%。中位 PFS 为 8.6 个月(95% CI,2.7-11.3),6 个月和 12 个月的 PFS 率分别为 58.3% 和 14.6%。中位 OS 为 15.1 个月(95% CI,8.6-不可估计),6 个月 OS 率为 100%,12 个月 OS 率为 87.5%。
没有阑尾癌患者 (n = 7) 有反应;然而,这些患者的 DCR 为 85.7%。两名小肠癌患者疾病得到控制,其中一名患者获得部分缓解。在胃食管连接部 (GEJ)/食管癌患者 (n = 3) 中,1 名患者达到了 ORR。该人群的 DCR 为 66.7%。
7例妇科肿瘤患者的ORR和DCR分别为57.1%和85.7%。在 2 名卵巢癌 (n = 4) 和子宫内膜癌 (n = 3) 患者中观察到 4 种反应。卵巢癌患者的 DCR 为 75%,子宫内膜癌患者为 100%。
最后,在合并了未知原发癌 (n = 4) 或乳腺癌 (n = 1) 患者的队列中,ORR 为 40%,DCR 为 100%。除了 1 名原发肿瘤不明的患者外,唯一的乳腺癌患者也获得了部分缓解。
63 名患者的治疗相关不良事件 (TRAE) 是可评估的。最常见的任何级别事件包括恶心 (49.2%)、腹泻 (47.6%)、疲劳 (41.3%)、呕吐 (39.7%) 和血肌酸增加 (15.9%)。大多数 TRAE 为 1 级或 2 级,其中 1 名患者出现 4 级发热性中性粒细胞减少症。
目前临床在研的KRAS G12C抑制剂不止AMG510和adagrasib,还有更多药物值得关注。
1. IBI-351(GFH925)
IBI-351是劲方医药研发的一款KRAS G12C抑制剂,信达生物通过合作获得了在中国(包括中国大陆、香港、澳门及台湾)的开发和商业化权利。它是一种新型、具有口服活性的强效 KRAS G12C 抑制剂,旨在通过共价和不可逆地修饰 KRAS G12C 蛋白的半胱氨酸残基来有效靶向 GTP/GDP 交换。临床前半胱氨酸选择性研究显示IBI351对 KRAS G12C 具有高选择性,IBI351 有效抑制下游信号通路,诱导肿瘤细胞凋亡和细胞周期停滞。
2023年5月4日,中国国家药品监督管理局药品审评中心(CDE)官网最新公示,GFH925片拟纳入突破性治疗品种,拟用于至少接受过两种系统性治疗的KRAS G12C突变型晚期结直肠癌患者。
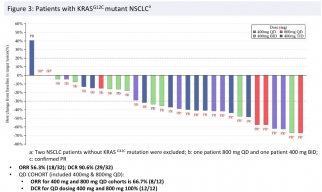
在2023年的AACR年会上,IBI351单药治疗晚期实体瘤患者的I期研究结果表明,在晚期KRAS G12C突变的NSCLC患者中,使用II期推荐剂量的IBI351单药治疗具有良好的安全性和令人鼓舞的疗效。
到数据截止日期(2022年11月30日),共有74名受试者参加了该研究,其中包括67名非小细胞肺癌(NSCLC)患者、6名结直肠癌(CRC)患者和1名胰腺癌患者。大约38.8%的NSCLC患者在基线时有脑转移。67名可评估的NSCLC患者中,41名达到部分缓解 (PR),研究者评估的ORR为 61.2%,DCR为92.5%。值得注意的是,在600mg BID(推荐的 2 期剂量)治疗的 30名NSCLC患者中,观察到更好的疗效信号,研究者评估的ORR为 66.7%(确认的ORR为53.3%)和 DCR为96.7%。


基于此,该产品治疗至少接受过一种系统性治疗的KRAS G12C突变型的晚期非小细胞肺癌(NSCLC)患者的适应症已被CDE纳入突破性治疗品种。
2. JDQ443
JDQ443是由诺华研发的一种高选择性和高生物活性的KRAS G12C抑制剂,在 2022 年 AACR 年会上公布的Ib/II期KontRASt-01(NCT04699188) 试验的剂量递增部分的初始数据中显示了早期疗效信号和可耐受的安全性。
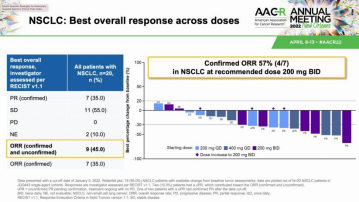
研究结果显示在20 名 NSCLC 患者亚组中,ORR 为 45%,对于接受200mg BID的7例NSCLC患者来说,ORR高达57%。研究人员观察到 55% 的患者疾病稳定,没有疾病进展的报告。对于接受4种不同剂量JDQ443治疗的39例患者,大多数TRAE为1-2级,无4级和5级AE发生;对于接受JDQ443 200mg BID治疗的11例患者来说,无3级及以上AE发生。
3.Divarasib(GDC-6036)
Divarasib(GDC-6036)是由罗氏开发的一种新型KRAS G12C抑制剂,它的作用是不可逆地将KRAS G12C癌蛋白锁定在非活性状态,阻止肿瘤细胞生长。
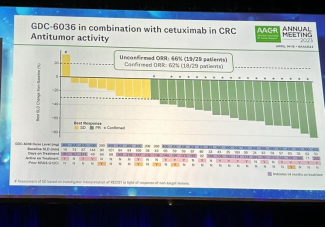
2023年AACR年会上数据显示,Divarasib和西妥昔单抗(爱必妥)在CRC患者联合治疗中表现出有希望的临床活性。divarasib 加西妥昔单抗获得了 62% 的确认客观缓解率 (ORR)。值得注意的是,总体人群中29名患者有5名之前接受过KRAS G12C抑制剂治疗,这5名患者中有3名确认对基于divarasib的组合有部分反应。
此前2022年ESMO大会上提交数据表明,divarasib 单一疗法具有良好的安全性,并且在大多数患者中得到了很好的管理。在CRC 队列(n = 39)中每天接受400mg全剂量治疗的患者的ORR为31%,所有剂量水平的ORR为24%。并且到目前为止,接受400mg治疗的患者的确认ORR已上升至36%。
4.JAB-21822
JAB-21822是加科思自主研发的KRAS G12C抑制剂。临床前研究数据表明,可单药治疗KRAS G12C突变的实体瘤,同时在KRAS G12C抑制剂治疗发生耐药后,联合SHP2抑制剂有望有效克服和逆转KRAS抑制剂的耐药问题。
2022年ASCO大会公布的I期临床试验显示,截至2022年4月1日,共入组72例晚期实体瘤患者,其中有32例KRAS G12C突变NSCLC患者进行疗效评估。总缓解率(ORR)为56.3%(18/32),疾病控制率(DCR)为90.6%(29/32)。
2022年12月,国家药品监督管理局药品审评中心(CDE)公示,JAB-21822 获得突破性疗法认定,用于二线及以上治疗晚期KRAS G12C突变的转移性非小细胞肺癌(NSCLC)患者。

5.D-1553
D-1553是由益方生物自主开发的一款新型,高效口服的KRAS G12C抑制剂。

近期,在《Journal of Thoracic Oncology》(JTO)上报告了D-1553最新的I期临床研究的数据,在74名可评估疗效分析的患者中,30名患者部分缓解,38 名患者疾病稳定,ORR为40.5%,疾病控制率(DCR)高达91.9%。中位无进展生存期为8.2个月,中位缓解持续时间为7.1个月。在推荐的Ⅱ期剂量下可评估反应的62名患者中,24名患者出现部分反应(ORR,38.7%),32名患者出现疾病稳定(DCR,90.3%)。中位无进展生存期和反应持续时间分别为7.6个月和6.9个月。值得注意的是,在脑转移患者中,ORR为17%,DCR高达100%。

6.LY3537982
LY3537982是由礼来开发的一种新型、有效、口服、高选择性KRAS G12C抑制剂。
在2023年AACR大会上, 公布了I 期 LOXO-RAS-20001 研究 (NCT04956640) 的数据,旨在评估口服 LY3537982 在KRAS G12C 突变的非小细胞肺癌 (NSCLC)、结直肠癌 (CRC)、子宫内膜癌、卵巢癌和胰腺癌患者中的初步疗效和安全性。
初治(未接受过KRAS抑制剂治疗)的NSCLC患者ORR为38%;经治NSCLC患者ORR为7%;可评估的KRAS G12C突变CRC和胰腺癌患者的ORR分别为10%和42%。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言