Nat Med:血源性肿瘤突变负担作为非小细胞肺癌阿特珠单抗治疗的生物标志物
2022-04-19 MedSci原创 MedSci原创
将bTMB开发为一种预测性的、独立的免疫治疗生物标志物或与其他生物标志物联合使用,还需要进一步的研究和优化分析。
阿特珠单抗单药治疗在EGFR/ALK野生型鳞状或非鳞状局部晚期或转移性非小细胞肺癌(NSCLC)患者的一线治疗中具有较好疗效,这些患者的肿瘤高表达程序性死亡配体1 (PD-L1)。在回顾性研究中,循环肿瘤DNA (ctDNA)中的肿瘤突变负担(TMB)在预测PD-L1/PD-1抑制剂的疗效方面具有较好的前景。

近日,顶级医学期刊Nature Medicine上发表了一篇研究文章,该研究旨在前瞻性地评估了血液TMB (bTMB),研究人员开展了B-F1RST 试验(NCT02848651),这是一项开放标签的2期临床试验,评估了bTMB作为一线阿特珠单抗单药治疗局部晚期或转移期IIIB-IVB非小细胞肺癌的预测生物标志物(n=152)。

该研究共同的主要终点是研究人员评估的RECIST版本1.1的客观缓解率(ORR),以及研究人员评估的无进展生存期(PFS);在预先定义的bTMB≥16的临界值时,较高和较低bTMB亚组之间的无进展生存期(PFS)。该研究的次要终点包括研究人员评估的PFS、总生存期(OS)、不同bTMB临界值的缓解持续时间以及安全性。
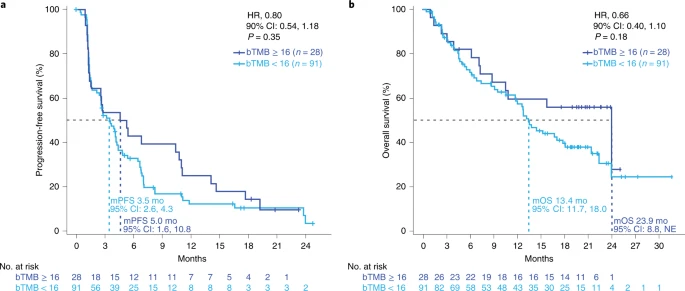
研究者评估的bTMB≥16组与bTMB<16组的PFS无统计学意义。然而,bTMB≥16与较高的ORR相关,ORR随着bTMB临界值的增加而改善。研究人员没有观察新的安全信号。在探索性分析中,最大体细胞等位基因频率(MSAF)<1%的患者ORR高于MSAF≥1%的患者。然而,进一步的分析表明,这种效果是由更好的基线预后而不是MSAF本身所驱动的。在36.5个月的随访中,对OS的探索性分析发现,与bTMB<16相比,bTMB≥16与更长的OS相关。
由此可见,将bTMB开发为一种预测性的、独立的免疫治疗生物标志物或与其他生物标志物联合使用,还需要进一步的研究和优化分析。
原始出处:
Edward S. Kim,et al.Blood-based tumor mutational burden as a biomarker for atezolizumab in non-small cell lung cancer: the phase 2 B-F1RST trial.Nature Medicine.2022.https://www.nature.com/articles/s41591-022-01754-x.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#突变负担#
77
#肿瘤突变#
92
#标志物#
77
#Nat#
77
#非小细胞#
73
认真学习了
74
#生物标志#
62
#生物标志#
69
#Med#
71