J Hepatol:帕比司他联合化疗显著提高难治性肝母细胞瘤生存率
2024-02-28 儿童肿瘤前沿 儿童肿瘤前沿 发表于上海
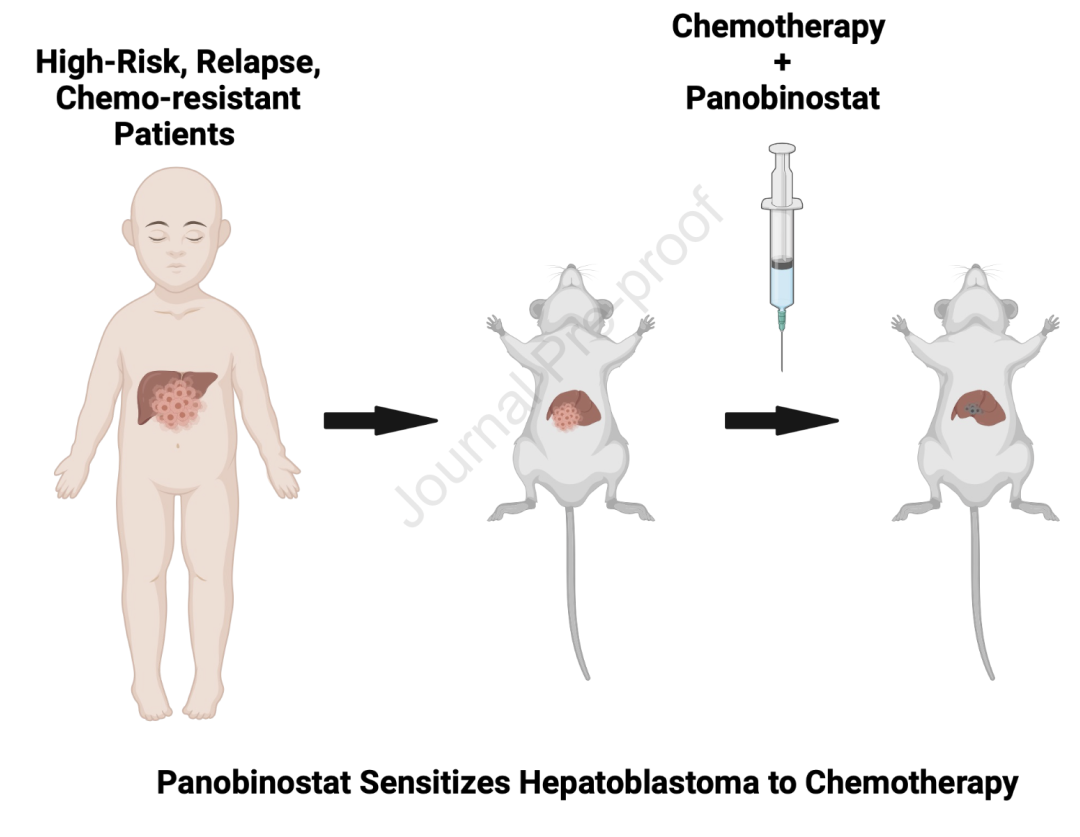
该研究证明了使用长春新碱、伊立替康和帕比司他的联合疗法可以减少高风险、复发和治疗难治性肿瘤的肿瘤大小,并为未来临床试验中利用这种联合疗法提供了临床前证据。
肝母细胞瘤(HB)是儿童最常见的肝脏癌症,占所有儿童恶性肿瘤的1%。尽管低风险疾病对围手术期化疗和手术的反应良好,但高风险疾病仍然导致高复发率和死亡率。现已提出长春新碱和伊立替康(vincristine and irinotecan:VI)的联合治疗作为这些情况的挽救疗法。尽管有证据表明VI策略初始反应良好,但许多患者对这种治疗无反应,最终因疾病进展而死亡。此外,当前的标准化疗存在终身耳聋和心脏功能障碍的风险。因此,需要针对复发难治性和高风险HB开发新的疗法。
HDACi(组蛋白去乙酰化酶抑制剂)作为癌症治疗的药物引起了关注,其在血液恶性肿瘤的治疗中已取得了显著进展。帕比司他是一种广谱HDAC类抑制剂,在多个临床试验中用于治疗患有实体和血液恶性肿瘤的儿童,并显示出良好的药物耐受性且毒性低。尽管先前的研究暗示HDACi可能为HB提供治疗选择,但在HB的临床前测试平台中尚未有关于帕比司他联合疗法的发表数据。
近日,由 Sanjeev A. Vasudevan团队发表于 Journal of Hepatology 题为 A Novel Treatment Strategy Utilizing Panobinostat for High-Risk and Treatment- Refractory Hepatoblastoma 的文章, 证明了使用长春新碱、伊立替康和帕比司他的联合疗法可以减少高风险、复发和治疗难治性肿瘤的肿瘤大小,并为未来临床试验中利用这种联合疗法提供了临床前证据。

文章分析了患者HB样本的RNA测序、微阵列、NanoString和免疫组化数据,以确定HDAC分类表达。使用PDSp筛选与帕比司他的联合化疗。开发了HB患者来源的异种移植(PDX)小鼠模型,并用在PDSp药物筛选中显示出最高疗效的联合疗法进行治疗。
首先,为了研究HDACi在治疗HB中可能发挥的作用,研究人员重新分析了51个HB肿瘤样本的微阵列数据,并将其与6个匹配的正常肝脏样本进行了标准化。除了HDAC1, HDAC2、HDAC3、HDAC4、SIRT1和HDAC11在HB样本中也表达过高。所有其他HDAC基因在HB样本中没有统计学上的过表达。为了进一步验证这些结果,研究人员评估儿童肿瘤学组(COG)库中的HB样本,重新分析了NanoString NCounter检测中所有未治疗HB肿瘤样本的已发表基因表达数据集,并与7个非癌症匹配的儿童肝脏样本进行了比较。与匹配的肝脏样本相比,肿瘤中的HDAC2、HDAC4和HDAC11表达升高。
为了进一步验证HB中HDAC的高表达,研究人员对五个患者肿瘤样本进行了RNA测序,这些样本被用来开发了六个PDX。与正常肝脏相比,HDAC1、HDAC2、HDAC4、HDAC7、SIRT1和HDAC11的表达有统计学上的增高。值得注意的是,PDX肿瘤也有这些相同HDAC亚型的类似升高表达。之后,研究人员对用于创建PDX的患者肿瘤的RNA测序中发现表达倍数变化较高的相同HDAC亚型。与配对的正常肝脏相比,HB肿瘤的平均免疫组化评分在HDAC1、HDAC2、HDAC4、HDAC7和HDAC11染色时更高。
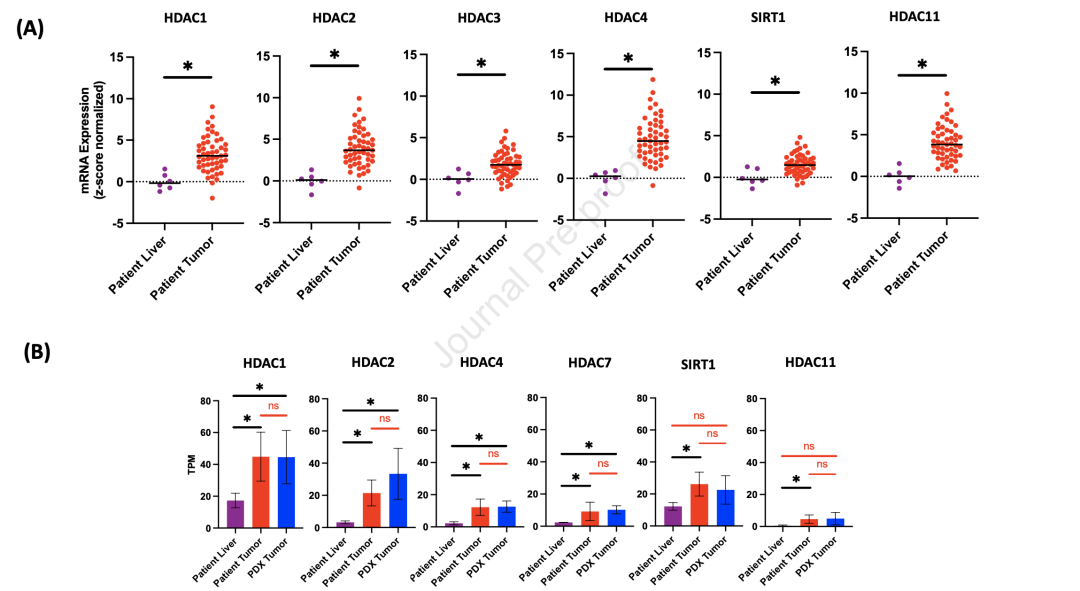
HDAC基因和蛋白质表达在HB中升高
其次,为了评估泛HDAC抑制的疗效,研究人员使用了八种HB细胞系进行了大规模药物筛选。在所有八种细胞系中,一致发现最低细胞活力的是帕比司他。鉴于这次药物筛选以及在多个HB样本队列中发现I-IV类HDACs过表达的事实,研究人员决定使用包括帕比司他在内的几种HDACi进行体外细胞毒性实验。在测试的四种HDAC抑制剂中,帕比司他在三种商业获取的细胞系(HuH-6、HepG2、HepT1)以及该研究建立的治疗难治性患者来源细胞系(HB17)中,在最低纳摩尔剂量下引起了显著的细胞死亡。
由于帕博尼司他具有最强的细胞毒性效应,研究人员决定在后续研究中使用帕比司他。在蛋白质水平上,帕比司他加药开始4小时后,H3/H4的乙酰化强度显著增强;从加药24小时后,乙酰化H3/H4的比率总体上升,这表明帕比司他通过其预期的机制发挥作用。
鉴于帕博尼司他引起的高度细胞死亡,研究人员决定在PDXs模型中测试帕比司他作为单一疗法以及与标准和治疗难治性化疗的联合疗法。从四种高风险和复发/难治性HB PDXs(HB52、HB66、HB106、HB113)培养出PDSps,并进行了广泛的药物筛选,使用了高风险化疗方案,包括顺铂/阿霉素、顺铂/阿霉素/5-氟尿嘧啶/长春新碱,以及长春新碱/伊立替康(VI)。然后将帕博尼司他添加到这些方案中,以测试联合策略的疗效。通过这种筛选策略,发现肿瘤细胞杀伤效果最好的治疗是帕比司他/长春新碱/伊立替康(VIP)。
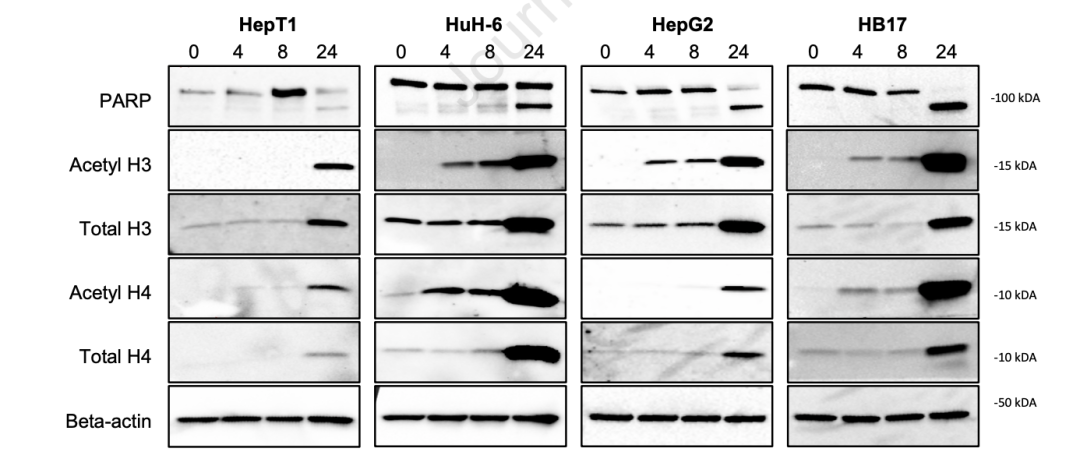
帕比司他在体外对HB有效
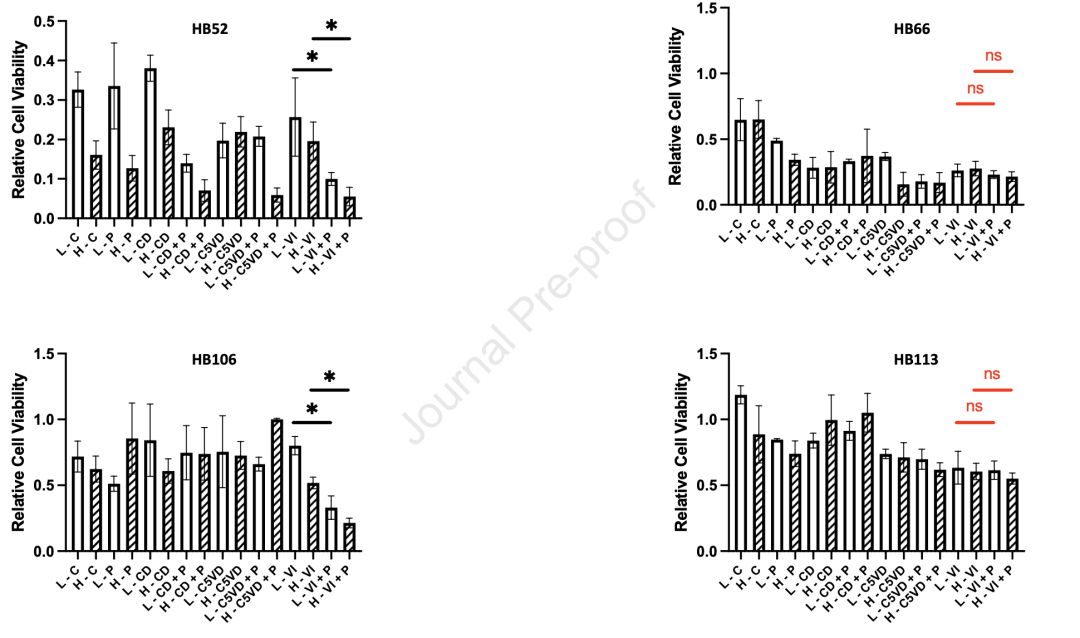
VIP在HB PDSp中最为有效
在单药研究中,研究人员选择了HB52 PDX来测试帕比司他单药治疗。与安慰剂组相比,肿瘤生长速度相同,1-2周内达到直径1.5厘米,并且在安乐死时的肿瘤大小与安慰剂组相似。因此,帕比司他单药治疗在剩余模型中可能无效。鉴于在四个PDSp模型中VIP疗法的杀伤效果最好,研究人员决定探究这个方案对高风险、治疗难治性和复发性HB PDXs的作用。
最初研究人员测试了HB52。接受安慰剂组的小鼠在1周内达到1.5厘米直径。接受VI治疗的小鼠在6周内肿瘤体积总体增加。接受VIP治疗的小鼠在治疗1周后显著减少肿瘤,研究结束时平均体积减少了2.4倍。VIP组的甲胎蛋白(AFP)水平在6周时下降了400倍(p=0.05)。接受VI治疗的组在3周和6周时AFP水平有所下降,但与安慰剂小鼠相比没有统计学显著差异。
当在HB106上重复这些实验时,研究人员发现肿瘤显著减少,4周时MRI显示肿瘤完全消失,且这一状态持续到6周,而VI组在研究结束时平均体积增加了1.2倍。
在HB66和HB113中,与安慰剂和VI治疗相比,肿瘤生长显著减缓。但这两个PDX模型在VI和VIP治疗组中AFP都没有下降。值得注意的是,在所有四项研究中,所有三种治疗组的小鼠体重稳定,没有观察到显著的不适。在HB52和HB106模型的最终MRI中,VIP组的肿瘤负担较小。在所有四个模型中, VIP治疗组与VI治疗组相比表达显著下降。
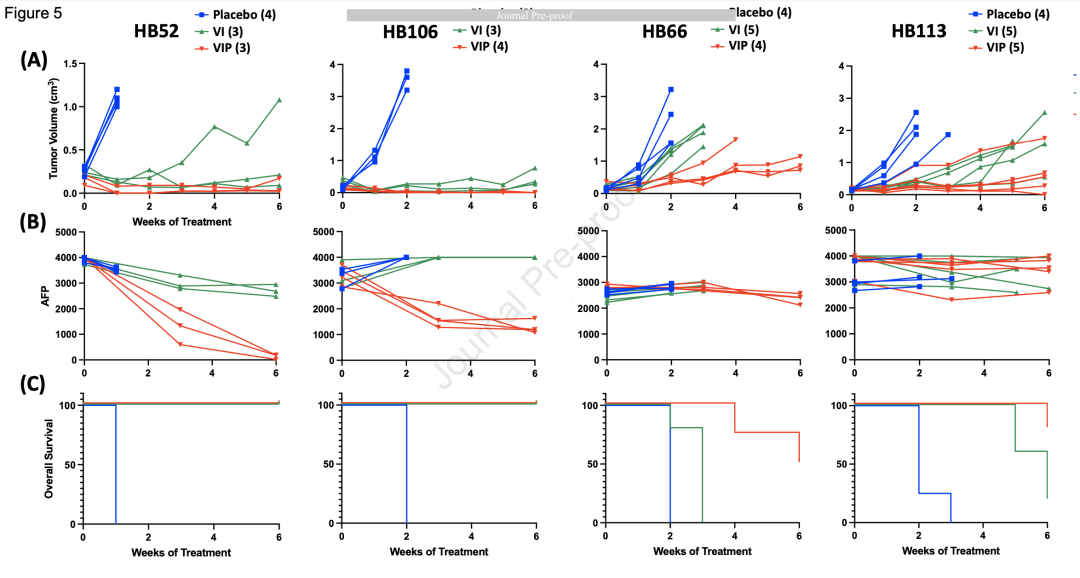
VIP治疗导致肿瘤缩小或生长速度减缓
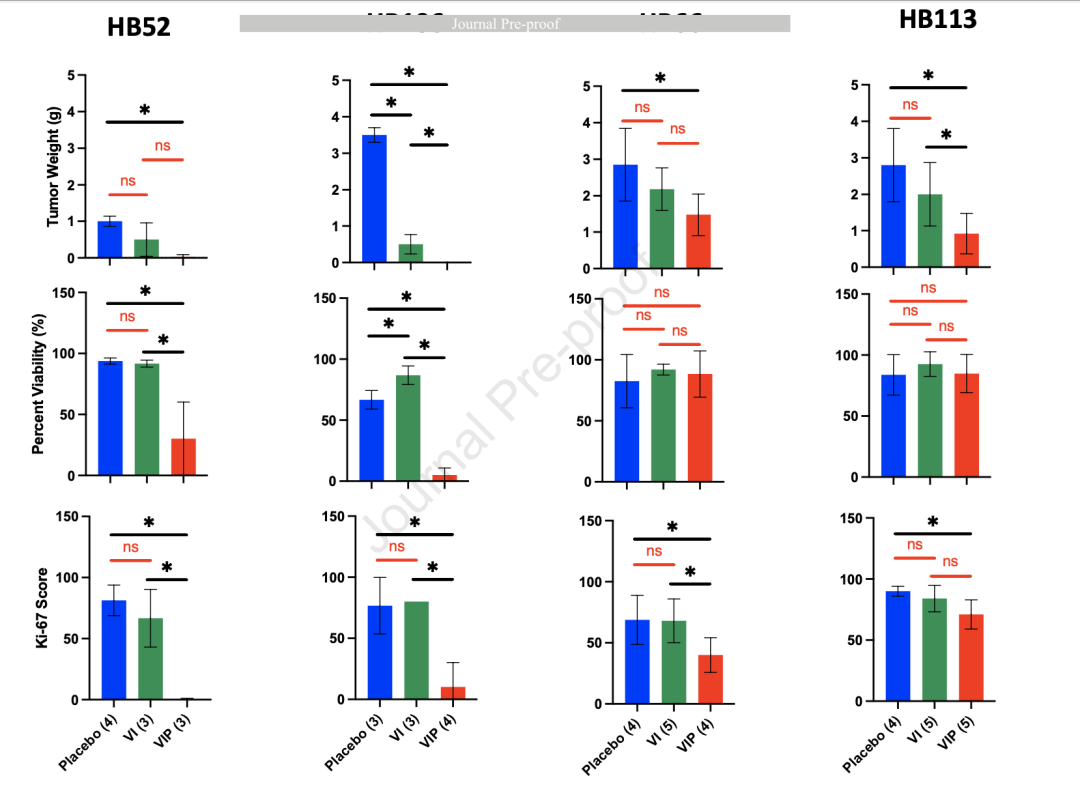
VIP导致HB肿瘤坏死(被遮挡细胞系分别为:左二-HB106;左三-HB66)
然而,为了进一步开发针对高风险HB的疗法,评估这种联合疗法的全部机制是必要的。研究人员已经证明,将帕比司他添加到VI治疗中显著降低了HDAC通路基因,特别是Bcl-2抗凋亡家族的BCL2和BCL2L1的表达。虽然在所有四个模型中,添加帕比司他后BCL2和BCL2L1的遗传表达显著下降,但HB66和HB113接受VI治疗的肿瘤仍具有最高的BCL2和BCL2L1表达。虽然需要进一步验证,但数据表明Bcl-2表达升高可能与对VI的耐药性相关,类似于它与对顺铂、阿霉素和5-FU化疗耐药性的相关性。此外,在此研究中,帕比司他在体外诱导HB凋亡,以及VIP治疗后T2加权成像中肿瘤强度的增加,说明有坏死的发生。但值得注意的是,VI增强抗癌效果的机制尚未完全清楚。长春新碱在与伊立替康和帕比司他的关系中的作用仍需要进一步研究。
总之,在这项研究中,研究人员开发了一个有效且高效的HB临床前工作流程,并且证明了VIP疗法是一种有效的治疗策略,已在四种独特的化疗耐药临床前模型中得到验证,并值得在未来的临床试验中考虑。此外,这种临床前测试流程不仅可以用来筛选针对高风险HB肿瘤的新疗法,还可以用来筛选那些具有独特突变和特征、对当前标准治疗方案无反应的肿瘤。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














肝母细胞瘤(HB)是儿童最常见的肝脏癌症
42
认真学习了
42
很不错
72
#化疗# #帕比司他# #肝母细胞瘤#
85