Lancet:罗特西普对比重组人促红素治疗输血依赖的较低危MDS的3期研究期中分析结果(COMMANDS研究)
2023-06-22 聊聊血液 聊聊血液 发表于上海
COMMANDS研究在26个国家的142家研究中心开展,计划进行两次期中分析,第一次是无效分析,第二次是疗效分析,本次报告的是第二次中期分析的结果,即在约300例患者完成24周治疗或在达到24周治疗前
对于较低危骨髓增生异常综合征(MDS)患者(根据2012年修订的IPSS-R 定义为极低危、低危或中危),治疗的主要目标是治疗贫血和改善生活质量,因为较低危MDS引起的慢性贫血治疗通常需要定期输注红细胞,与发病率增加、铁超载和总生存期缩短相关。
红细胞生成刺激剂 (ESA) 如重组人促红素(Epoetin Alfa)是较低危MDS患者的标准治疗,可用于输血依赖性贫血,特别是低血清促红细胞生成素 (< 500U/L) 和红细胞输血需求低于每月2个红细胞单位的患者。ESA的治疗的反应率可高达70%,但如果血清促红细胞生成素高于500U/L,预期反应率(定义为不依赖浓缩红细胞输注或血红蛋白升高≥1.5 g/L,或两者,持续至少8-16周)则不足10%。
罗特西普是一种红细胞成熟剂,在其双盲、安慰剂对照、3期 MEDALIST 研究中纳入输血依赖的较低危MDS,证实其可降低输血依赖性较低危MDS伴环形铁粒幼红细胞患者的贫血严重程度。但尚无研究比较罗特西普与ESA用于治疗未经ESA治疗、较低危MDS患者的贫血的疗效和安全性。
COMMANDS研究是一项全球、III期、开放性、随机对照研究,旨在比较罗特西普与重组人促红素治疗需要红细胞输注的 ESA 初治、较低危MDS患者所致贫血的疗效和安全性。近日《The Lancet》报告了COMMANDS研究预先规定的期中分析数据,发现对于未接受过红细胞生成刺激剂治疗的较低危MDS患者,相比重组人促红素,罗特西普在改善红细胞输注依赖性、提升血红蛋白水平、增进治疗反应的持久性等方面具有显著统计学意义,所有亚组均取得相同或更好的治疗效果,此外安全性和耐受性可接受。
COMMANDS研究在26个国家的142家研究中心开展,计划进行两次期中分析,第一次是无效分析,第二次是疗效分析,本次报告的是第二次中期分析的结果,即在约300例患者完成24周治疗或在达到24周治疗前停药时检验主要终点的优效性。
研究纳入标准包括年龄≥18岁,未接受过 ESA治疗,诊断为MDS(WHO 2016 标准)且符合极低危、低危或中危IPSS-R分类,骨髓中原始细胞<5%,筛选时经中心病理学实验室确认,需要输注红细胞(随机前每8周输注2-6个单位浓缩红细胞,持续至少8周),筛选时内源性血清促红细胞生成素浓度低于500 U/L。
入组患者1:1随机接受罗特西普或重组人促红素治疗。罗特西普皮下给药,每3周1次,起始剂量为1.0 mg/kg体重,可增加至1.33 mg/kg,然后最大剂量为1.75 mg/kg。重组人促红素皮下给药,每周一次,起始剂量为 450 IU/kg 体重,可增加至787.5 IU/kg,然后最大剂量为1050 IU/kg(最大允许总剂量为80000 IU),持续治疗时间≥24 周。
主要终点为摆脱红细胞输注12周(RBC-TI)且平均血红蛋白(Hb)水平增加≥1.5g/dL。关键次要终点包括1-24周期间有至少8周的血液学红系反应 (haematological improvement–erythroid,HI-E,IMWG标准),RBC-TI ≥ 12周及24周。
患者
356例患者随机分配接受治疗:178例患者接受罗特西普治疗,178例患者接受重组人促红素治疗(图1)。
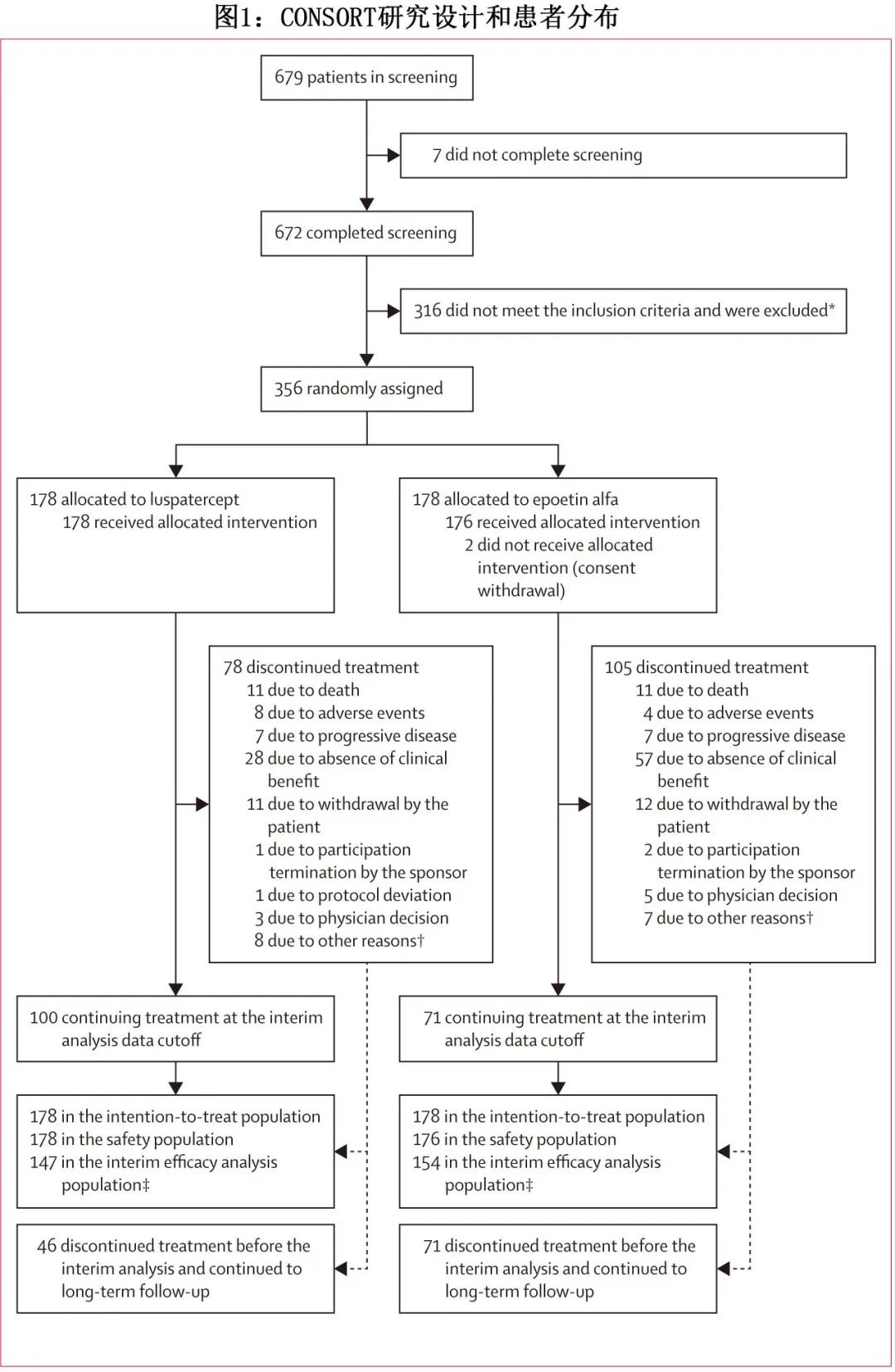
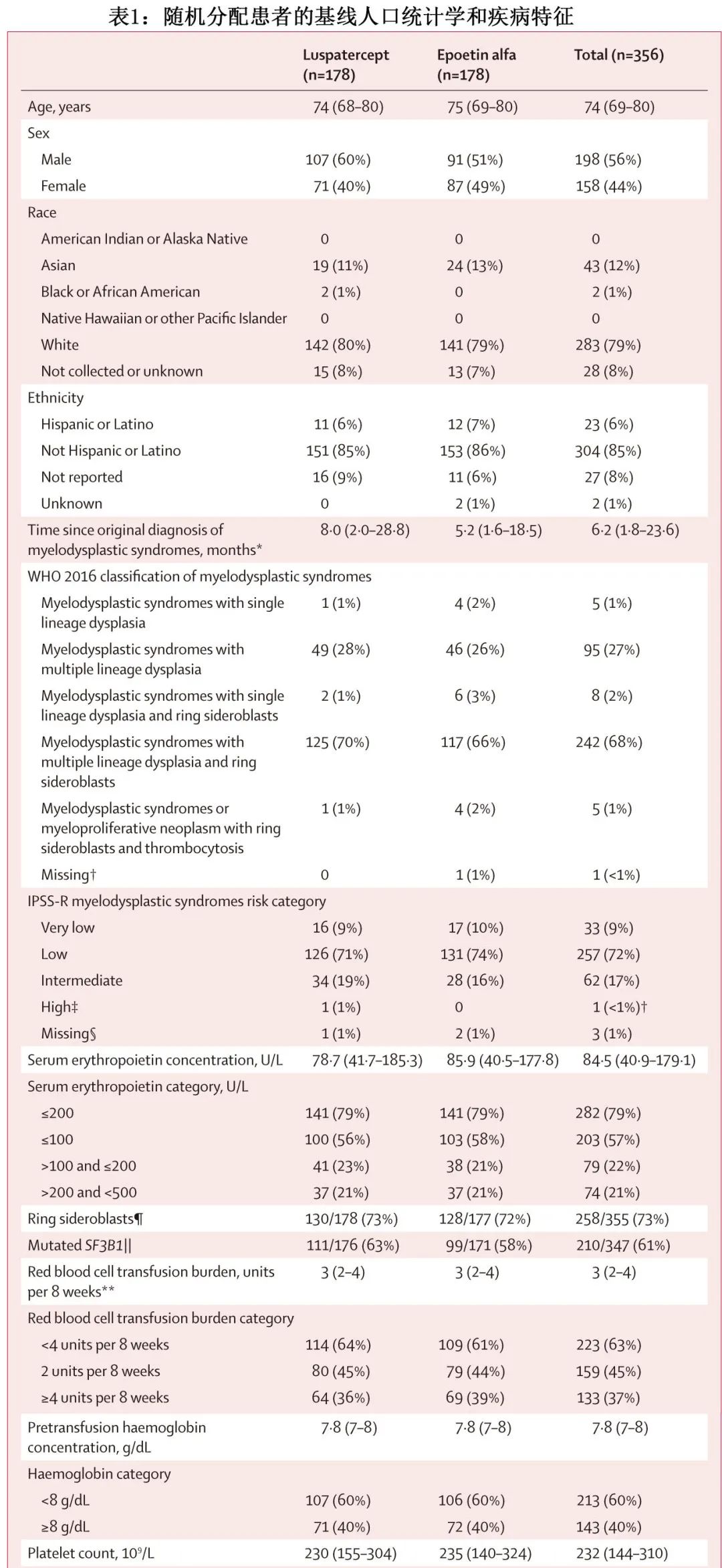
随机分配患者的基线特征在治疗组间平衡(表1)。患者的中位年龄为74岁;198例 (56%) 患者为男性,158例 (44%) 为女性。基线前8周内的中位输血负荷为 3U/8 周。中位基线内源性血清促红细胞生成素为84.5 U/L,中位基线血红蛋白浓度(输血前)为7.8 g/dL。在可获得环形铁粒幼红细胞数据的患者中,355例中258例 (73%) 存在环形铁粒幼红细胞。罗特西普组的中位治疗持续时间为42周,重组人促红素组为27周。罗特西普组147例患者和重组人促红素组154例患者接受了至少24周的治疗或提前停药,并被纳入中期疗效分析。
疗效
罗特西普组147例患者中的86例 (59%) 和重组人促红素组154例患者中的48例 (31%) 达到了主要终点,即摆脱红细胞输注12周(RBC-TI)且平均血红蛋白(Hb)水平增加≥1.5g/dL(第1-24周)(缓解率的共同风险差异为26.6;p<0.0001;比值比 [OR]=3.1)。此外,第1-24周期间,罗特西普组中98例 (67%) 患者和重组人促红素组中71例 (46%) 患者实现了至少12周的摆脱红细胞输注(缓解率的常见风险差异为19.;标称p=0.0002;OR=2.4;图2);分别有70例 (48%)和45例 (29%) 患者实现了24周的摆脱红细胞输注(缓解率的常见风险差异为17.0;标称p=0.0006;OR=2.3;图2)。罗特西普组109例 (74%) 患者和重组人促红素组79例 (51%) 患者达到至少8周的HI-E反应(反应率的共同风险差异为22.3;标称p<0.0001;OR=2.8;图2)。第1-48周期间,罗特西普组128例患者中有74例 (58%) 达到摆脱红细胞输注至少24周,重组人促红素组136例患者中有47例 (35%) 达到摆脱红细胞输注至少24周(缓解率的常见风险差异为21.8;标称p<0.0001)。

所有达到摆脱红细胞输注至少12周(第1-24周)的患者至治疗结束摆脱红细胞输注的中位持续时间:罗特西普组患者的中位持续时间为127周,重组人促红素组患者为77周(标称p=0.0050)。在HI–E反应患者中,罗特西普组患者至HI–E的平均时间为17.1天,重组人促红素组为27.0天。
在 ITT 人群中,罗特西普组178例患者中的4例 (2%) 和重组人促红素组178例患者中的5例 (3%) 进展为急性髓性白血病(风险比 [HR]=0.821;标称p值=0.77);发生率分别为1.76/100人年和2.31/100人年。
在纳入疗效分析的301例患者中,295例有82个分析基因的基线突变数据,报道了36个基因的体细胞突变。大多数突变的变异等位基因频率为3-50%,最常见的突变基因为SF3B1、TET2、ASXL1、DNMT3A、U2AF1和SRSF2。罗特西普和重组人促红素组之间的基线突变频率无显著差异。常见突变基因的风险差异估计值表明,与重组人促红素相比,ASXL1、TET2、SF3B1和SF3B1α(定义为同时携带 DNMT3A 或 ASXL1 和/或 TET2 突变的 SF3B1 突变)突变患者更有可能获得罗特西普的主要终点缓解(图3)。
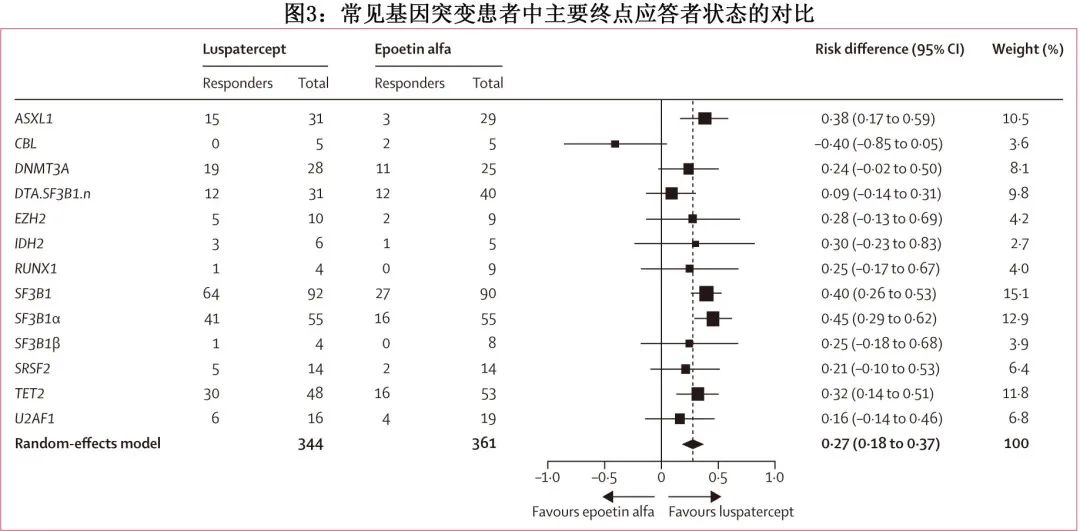
按亚组评估了罗特西普应答者与重组人促红素应答者在主要终点方面的比例,具体如下:环形铁粒幼细胞阳性亚组(罗特西普组70/108例[65%]应答vs 重组人促红素组29/112例[26%])和环形铁粒幼细胞阴性亚组(16/39例[41%] vs 19/41例 [46%]);突变 SF3B1亚组(64/92例[70%] vs 27/88例[31%])和非突变 SF3B1 亚组(22/53例[42%] vs 20/62例[32%]);内源性血清促红细胞生成素浓度 (≤200U/L) 亚组 (74/118例[63%]vs 44/121例[36%]) 和内源性血清促红细胞生成素浓度(>200至<500 U/L)亚组 (12/29例[41%] vs 4/33例[12%]);以及基线输血负荷低于每8周4个红细胞单位(61/92例[66%] vs 35/90例[39%]),基线输血负荷至少为每8周4个红细胞单位(25/55例[45%] vs 13/64例[20%])。对于所有分析的亚组,罗特西普组患者摆脱红细胞输血中位持续时间(持续至少12周)均长于重组人促红素组。
安全性
所有178例随机分配至罗特西普组的患者均接受治疗,而178例随机分配至重组人促红素组的患者中有176例接受重组人促红素治疗(2例患者在随机化后立即中止研究;图1),最终354例患者纳入安全性人群。罗特西普组的中位治疗持续时间长于依泊汀α组(42周 vs 27 周)。总体而言,罗特西普组164/178例 (92%) 患者和重组人促红素组150/176例 (85%)患者发生了至少1起治疗后出现的不良事件,最常报告的治疗后出现的不良事件(所有等级,任一组中≥10%的患者发生)为腹泻、疲乏、外周水肿、高血压、无力、恶心、呼吸困难和新冠肺炎,除无力外,罗特西普组的发生率均高于依泊汀α组(表2)。
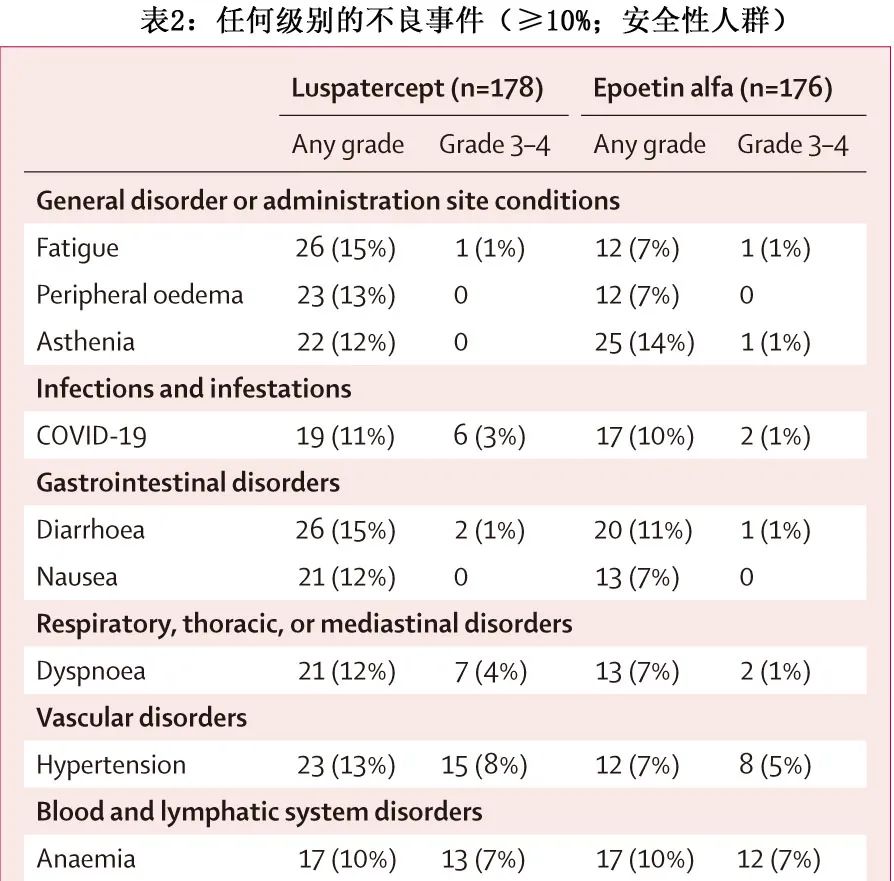
罗特西普组54例 (30%)患者和重组人促红素组31例 (18%)患者报告了疑似治疗相关不良事件。罗特西普组中最常见的疑似治疗相关不良事件(≥3%的患者,最常见的事件发生于5%的患者)为疲乏(7例患者发生9起事件)、乏力(5例患者发生7起事件)、恶心(9例患者发生11起事件)、呼吸困难(6例患者发生6起事件),头痛(5例患者的6起事件)和高血压(6例患者的9起事件),均为1级或2级,但7例高血压事件的严重程度为3级;重组人促红素组中未报告≥3%的疑似治疗相关不良事件。罗特西普组97例 (54%)患者和重组人促红素组75例 (43%)患者发生至少1起3级或4级治疗后出现的不良事件;最常报告的罗特西普治疗期间出现的3级或4级不良事件(≥3%的患者)为高血压、贫血、呼吸困难、中性粒细胞减少、血小板减少、感染性肺炎、COVID-19、MDS和晕厥;重组人促红素治疗期间出现的3级或4级不良事件为贫血、感染性肺炎、中性粒细胞减少、高血压、铁超载、COVID-19感染性肺炎和MDS。校正暴露量后,3级或4级不良事件无显著差异(罗特西普vs重组人促红素:85/100患者-年 vs 73/100 患者-年)。
罗特西普组68例 (38%)患者和重组人促红素组60例 (34%)患者报告了治疗后出现的严重不良事件。在两个治疗组中,最常见的严重治疗后出现的不良事件均属于感染及侵染类疾病;主要为COVID-19(各9例 [5%] 患者)和感染性肺炎(罗特西普组6例 [3%],重组人促红素组9例 [5%])。治疗组间严重 TEAE 的总体发生率和暴露校正的发生率相似。罗特西普组1例患者(急性髓系白血病)和重组人促红素组3例患者(急性冠脉综合征、急性发热性中性粒细胞增多性皮肤病伴发热和肝炎伴无力)报告了疑似治疗相关严重不良事件。罗特西普组8例 (4%)患者和重组人促红素组4例 (2%)患者因治疗后出现的不良事件而中止治疗,其中2起事件被认为是疑似治疗相关不良事件:1起非严重3级劳力性呼吸困难事件,1起严重4级转化为急性髓系白血病事件,罗特西普组各1例患者发生。
特别关注的治疗中出现的不良事件和其他相关安全性事件包括恶性肿瘤、癌前疾病、血栓栓塞事件、肾损伤、高血压、肝毒性、髓外造血肿块、免疫原性反应(局部和超敏反应)和乏力,这些事件的严重程度大多为1级或2级。两个治疗组中恶性肿瘤、癌前病变、肝毒性和免疫原性超敏反应的发生率相似;而罗特西普组乏力、肾损伤、免疫原性局部反应、高血压和血栓栓塞事件的发生率更高。治疗前24周内的结果与之相似;但按暴露量校正后,治疗组间无力、肾损伤和血栓栓塞事件的发生率相似,然而罗特西普组高血压和免疫原性局部反应的频率仍较高。此外研究中未检测到髓外造血肿块病例。总体而言,罗特西普的安全性特征可接受,与既往观察结果一致。
罗特西普组178例患者中的5例 (3%) 和重组人促红素组176例患者中的7例 (4%) 进展为高危MDS(根据 IPSS-R 标准)。试验期间,罗特西普组和重组人促红素组分别有32例 (18%) 和32例 (18%) 患者死亡。在罗特西普组,导致死亡的治疗后出现的不良事件(总计n=8[5%])为多器官功能障碍(1例患者)、感染和侵染(2例患者)、神经系统疾病(2例患者)、冠状动脉供血不足(1例患者)、肠缺血(1例患者)和急性髓性白血病(1例患者);1例导致死亡的急性髓系白血病(接受1.0 mg/kg 罗特西普3次给药后确诊)发生于1例78岁患者,研究者认为与研究治疗相关,该患者接受罗特西普治疗44天。重组人促红素组导致死亡的治疗后出现的不良事件(总计n=12[7%])为发热(1例患者)、感染和侵染(5例患者)、心脏疾病(5例患者)和营养不良(1例患者)。
COMMANDS研究对完成24周治疗或提前停药的301例患者(罗特西普组147例,重组人促红素组154例)进行了中期疗效分析。罗特西普组147例患者中的86例 (59%) 和重组人促红素组154例患者中的48例 (31%) 达到了主要终点(常见风险缓解率差异为26.6;95%CI 15.8-37.4;p<0.0001)。接受罗特西普(42周)的患者的中位治疗暴露时间长于重组人促红素(27周)。最常报告的罗特西普治疗期间出现的3级或4级不良事件(≥3%的患者)为高血压、贫血、呼吸困难、中性粒细胞减少、血小板减少、感染性肺炎、COVID-19、MDS和晕厥;重组人促红素治疗期间出现的3级或4级不良事件为贫血、感染性肺炎、中性粒细胞减少、高血压、铁超负荷、COVID-19感染性肺炎和MDS。罗特西普组中最常见的疑似治疗相关不良事件(≥3%的患者,最常见的事件发生于5%的患者)为疲乏、无力、恶心、呼吸困难、高血压和头痛;而重组人促红素组中无≥3%的患者。校正暴露量后,3级或4级不良事件无显著差异(罗特西普vs重组人促红素:85/100患者-年 vs 73/100 患者-年)。1例急性髓系白血病确诊后死亡被认为与罗特西普治疗相关(治疗44天)。
在该中期分析中,对于未经ESA治疗的较低危MDS患者,与重组人促红素相比,罗特西普可改善摆脱红细胞输注和血红蛋白增加的发生率。对于需要红细胞输注的较低危MDS伴或不伴环形铁粒幼细胞患者,罗特西普可为贫血的当前标准治疗提供替代疗法。但也需要长期随访和额外的数据来证实本研究结果,并进一步完善较低危MDS患者的其他亚组的结果,包括 SF3B1 未突变和环形铁母细胞阴性亚组。
克利夫兰诊所Hetty E Carraway教授同期对此研究发表点评“Are we ready to ring in a new upfront therapy in lower-risk myelodysplastic syndromes?”。他认为,该研究存在一定局限性,但证实了ESA初治的较低危MDS患者可从基于罗特西普的一线治疗中获益,尤其是环形铁母细胞阳性状态和SF3B1 突变患者。罗特西普作为输血依赖患者的替代一线有效疗法是可取的,但也仍有几个尚未回答的问题。首先,是否需要确定一线罗特西普与 ESA相比对哪些患者最有益,如果是,如何确定(即通过血清促红细胞生成素浓度、SF3B1突变状态、环形铁粒幼红细胞状态或其他因素)?其次,对于一线罗特西普治疗无临床反应的患者,是否应给予 ESA 治疗,如果是,反应的可能性如何?第三,突变谱分析是否有助于指导选择哪种药物是最佳一线治疗或可缓解对克隆进化的担忧(即出现导致疾病进展的耐药克隆)?第四,研究结果是否适用于非裔美国人(仅占研究队列的1%)和本研究中可能代表不足的其他患者?第五,与重组人促红素相比,罗特西普需要更少的门诊访视,这对健康相关生活质量有什么影响,指导下一步的药物经济学数据是否会直接节约成本(或节省时间)?
Carraway教授热切期待 COMMANDS 研究的全面结果;然而在较低危MDS患者的一线中,罗特西普能否以及如何改变当前的治疗前景仍待观察。不管怎么说,较低危MDS患者治疗中有多种选择也是非常有价值的。
参考文献
1.Platzbecker U,et al.Efficacy and safety of luspatercept versus epoetin alfa in erythropoiesis-stimulating agent-naive, transfusion-dependent, lower-risk myelodysplastic syndromes (COMMANDS): interim analysis of a phase 3, open-label, randomised controlled trial.Efficacy and safety of luspatercept versus epoetin alfa in erythropoiesis-stimulating agent-naive, transfusion-dependent, lower-risk myelodysplastic syndromes (COMMANDS): interim analysis of a phase 3, open-label, randomised controlled trial.Lancet . 2023 Jun 9;S0140-6736(23)00874-7. doi: 10.1016/S0140-6736(23)00874-7.
2.Carraway HE.Are we ready to ring in a new upfront therapy in lower-risk myelodysplastic syndromes?Lancet . 2023 Jun 12;S0140-6736(23)01130-3. doi: 10.1016/S0140-6736(23)01130-3.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言