【JCO】FLT3-ITD AML移植后基于MRD的吉瑞替尼维持治疗,助力整体治疗策略
2024-03-23 聊聊血液 聊聊血液 发表于上海
学者使用 FLT3 抑制剂吉瑞替尼开展一项 HCT 后维持治疗的随机研究,以确定所有此类患者是否均获益,以及MRD是否可以确定哪些患者获益。
FLT3-ITD AML移植后维持
FLT3内部串联重复突变 (FLT3-ITD) 在急性髓系白血病 (AML)中很常见,可增加复发风险。异基因造血细胞移植 (HCT) 可改善携带FLT3-ITD的AML患者的结局,患者在HCT 后常规接受 FLT3 抑制剂维持治疗,但支持证据的相关研究质量不高,且这些研究中并未在HCT前应用FLT3抑制剂(目前HCT前应用FLT3抑制剂较为普遍)。此外,至少半数CR1期接受移植的FLT3-ITD AML患者可不给予进一步治疗而治愈,因此很多HCT后接受FLT3抑制剂的患者面临不必要的毒性。
HCT 前后存在可测量残留病灶 (MRD) 可高度预测结局,但由于 FLT3-ITD 突变在疾病过程中明显不稳定,历史上未将其视为 MRD 的有用标志物,但近期数据表明,使用序贯聚合酶链反应 (PCR) 和二代测序 (NGS) 的高灵敏度检测方法可检测缓解期患者的低水平 FLT3-ITD 突变,且突变与复发相关。
因此学者使用 FLT3 抑制剂吉瑞替尼开展一项 HCT 后维持治疗的随机研究,以确定所有此类患者是否均获益,以及MRD是否可以确定哪些患者获益。研究结果近日发表于《Journal of Clinical Oncology》,同期附专家评述“Moving Toward Total Therapy in AML: Personalized Treatments Improve Post-Transplant Outcome”。

研究方法
该随机、双盲、安慰剂对照的血液和骨髓移植临床试验网(BMT CTN) 1506 (MORPHO)研究旨在确定:(1)对于接受HCT的CR1期FLT3-ITD AML患者,HCT后使用吉瑞替尼维持治疗是否有益,(2) FLT3-ITD MRD检测可否用于确定哪些患者获益。
研究纳入首次缓解期接受HCT的 FLT3-ITD AML 成人患者,并在 HCT 后随机接受安慰剂或吉瑞替尼 120mg 每日一次治疗24个月。主要终点为无复发生存期 (RFS),次要终点包括总生存期 (OS) 以及 HCT 前/后 MRD(PCR) 对 RFS 和 OS 的影响。
研究结果
患者
该研究有16个国家的122个中心参与,共筛选620例患者,移植前注册488例并最终随机356例患者,每组均为178例(图1)。
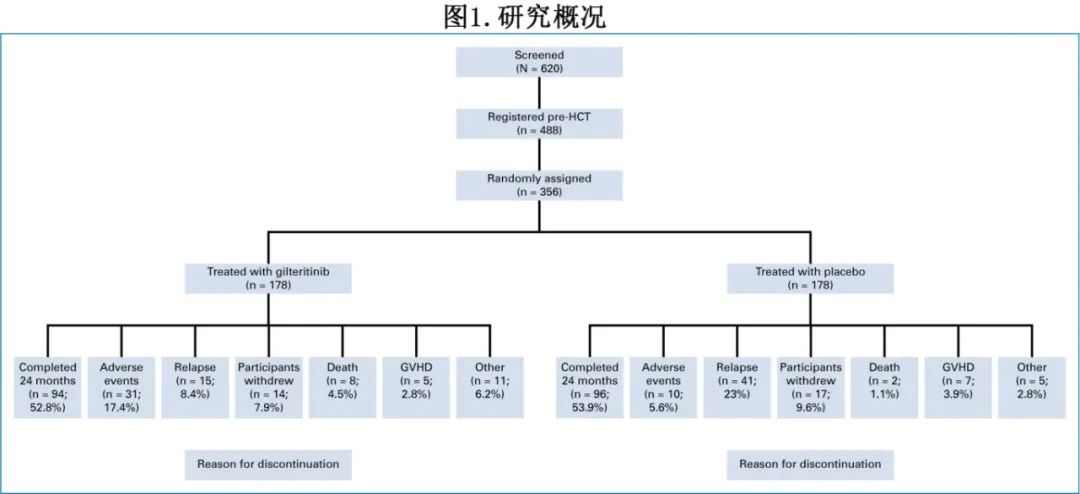
初步分析是基于最后一例患者随机分配2.5年作为数据截止日期。安全性分析集(SAF)包括服用至少1剂研究药物的355例患者(吉瑞替尼组178例和安慰剂组177例)。早期停药的最常见原因包括吉瑞替尼组的AE(17.4%)和安慰剂组的复发(23%)(图1)。
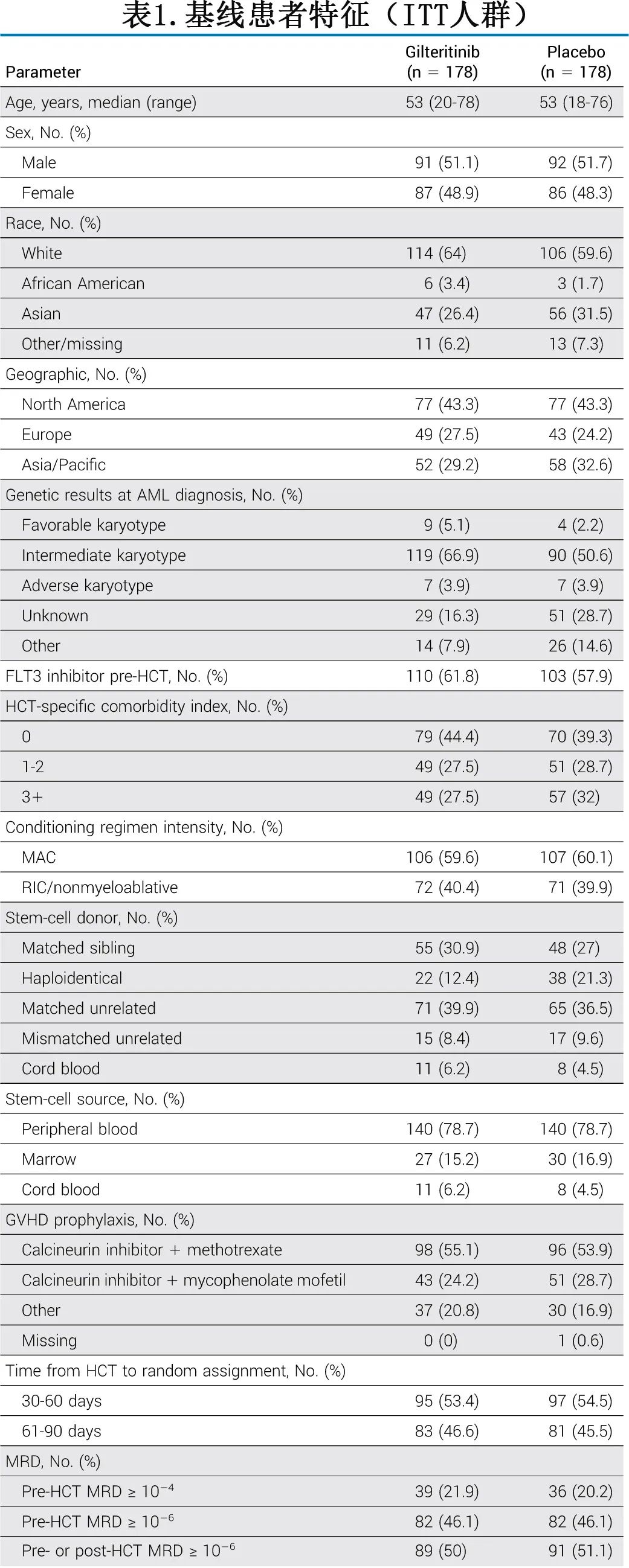
患者特征见表1。34.6%的患者携带NPM1突变。由于未获得其他突变或FLT3-ITD等位基因比例的信息,因此无法根据ELN 2022系统分类。HCT前356例中350例(98%)和HCT后(随机分组前)356例中347例(97.5%)获得用于MRD分析的骨髓穿刺。HCT前,在分层水平(≥1X10-4) 有75/356例(21.1%)为MRD阳性,而在≥1X10-6水平有164/356例 (46.1%)为MRD阳性。HCT后,≥1X10-6MRD水平上有71/356例(19.9%),包括16例(4.5%)在HCT后MRD阳性但HCT前MRD阴性。因此,共180 ([164+16 /356];50.6%)的患者在围HCT期为MRD阳性。
疗效
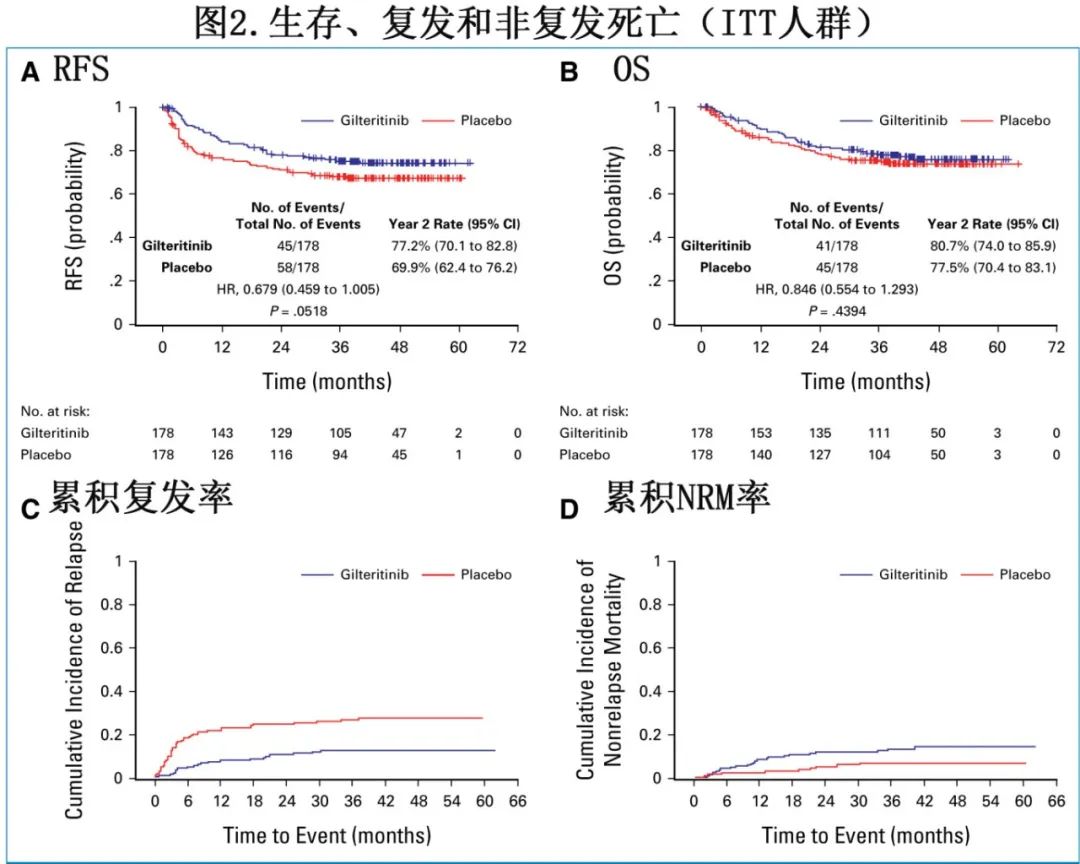
在数据截止时存活的270例患者中,中位随访时间为43.8个月。在初步分析中共观察到103起RFS事件,这使统计学功效从85.0%降至78.6%;更长时间的随访不会显著增加事件数量,因为HCT后2年以后的事件发生率非常低。
尽管吉瑞替尼组的RFS优于安慰剂组(图2A),但无统计学差异(2年RFS率分别为77.2%和69.9%,HR=0.679,P=0.0518);86例死亡,OS无统计学差异(图2B) (HR=0.846,吉瑞替尼组稍优,p=0.4394)。吉瑞替尼组组的复发率低于安慰剂组、NRM高于安慰剂组(图2C和图2D)。
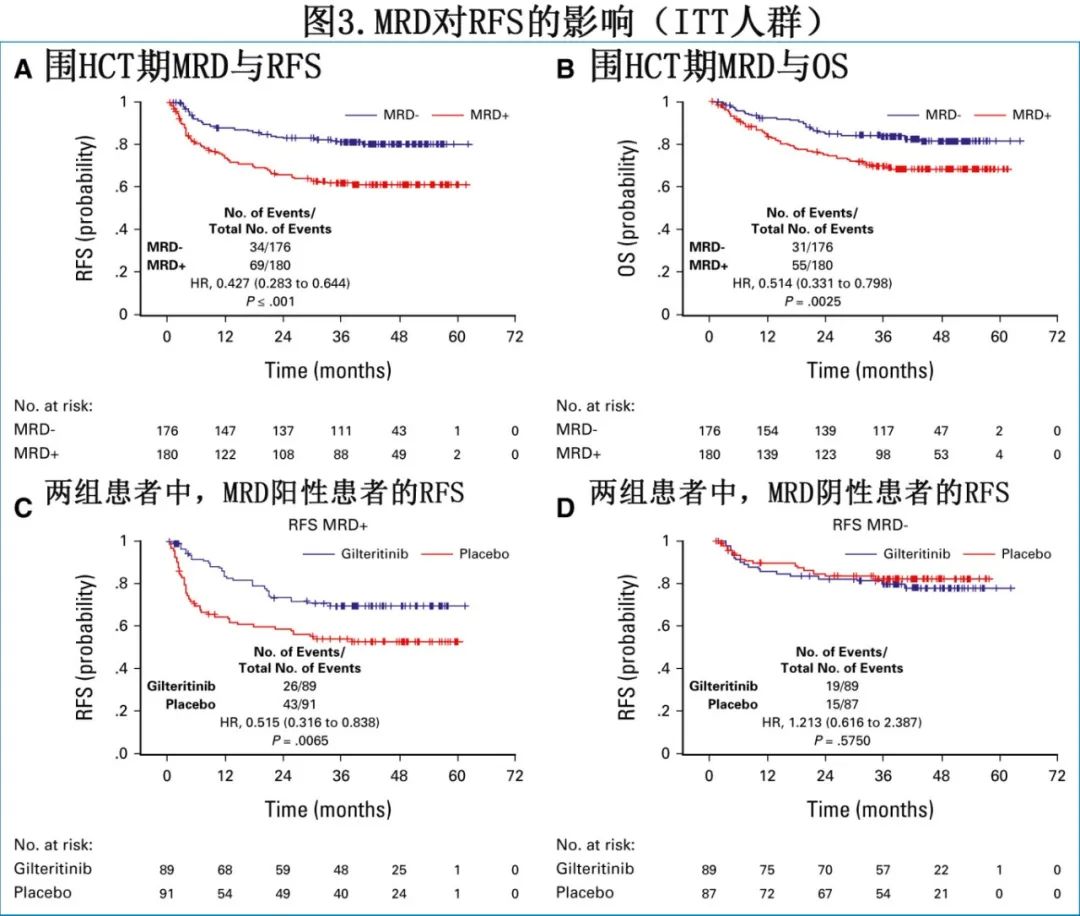
对于两组,≥1X10-6水平的MRD阳性均与RFS和OS降低相关(图3A和3B)。在HCT前或HCT后MRD阳性患者中,如果接受吉瑞替尼治疗,则RFS显著改善,而MRD阴性患者的RFS相似(图3C和3D);对于HCT前(p=0.0105)、HCT后(P=0.0143)或HCT前+后(P=0.0065)为MRD阳性的患者,情况也是如此。同样,HCT前或HCT后MRD水平≥1X10-6的患者接受吉瑞替尼治疗后OS改善,但未达到统计学差异(p=0.0731)。
对于HCT前接受过FLT3抑制剂治疗的患者(60%),吉瑞替尼与安慰剂组相比有RFS获益(HR=0.598;p=0.0436),但接受和未接受HCT前FLT3抑制治疗的患者之间的HCT前MRD阳性率没有差异(48.3% vs 52.1%)。与接受减低强度预处理(RIC)的患者相比,接受MAC的患者的OS改善(HR=0.529;P=0.0027),且与MRD状态无关。
亚组分析显示,不同地区的结局存在差异。吉瑞替尼在北美有获益,在亚洲/世界其他地区(ROW)获益很小,而欧洲有轻度负面影响(图4)。但需要注意的是,研究人群和临床实践模式存在明显的地理差异,例如从诊断至HCT的时间、诱导和巩固疗程的数量、HCT前FLT3抑制剂用药、预处理方案和合并使用唑类药物。

安全性
安全性分析集(SAF)包括吉瑞替尼组178例和安慰组177例,吉瑞替尼组178例中的94例(52.8%)和安慰剂组178例中的96例(53.9%)完成24个月维持治疗。吉瑞替尼组18.5%和安慰剂组20.3%发生治疗期间发生的III~IV级aGVHD (p=0.6157),分别有93例(52.2%)和75例(42.4%)发生治疗期间发生的cGVHD (p=0.181)。
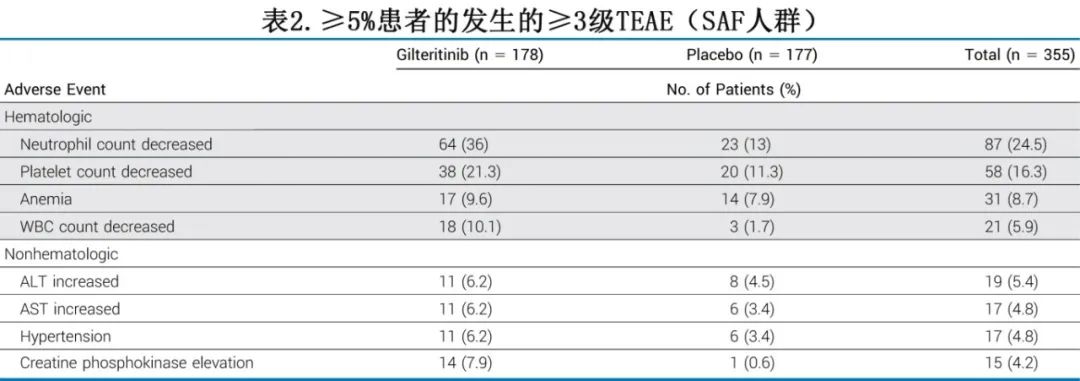
吉瑞替尼组82%和安慰剂组53.1%发生≥3级治疗期间出现的不良事件(TEAE)。与安慰剂组相比,吉瑞替尼组治疗期间出现的骨髓抑制和感染均更为常见,且骨髓抑制是患者早期退出研究治疗的最常见原因。表2列出了发生于≥5%患者的≥3级TEAE。
总结
该研究是支持基于MRD的HCT后维持治疗的首批研究之一。研究纳入356例患者,在HCT后随机分配接受吉瑞替尼或安慰剂维持治疗。尽管吉瑞替尼组的RFS较高,但无统计学差异(HR=0.679,P=0.0518)。50.5%的患者在HCT前或后为MRD阳性(这是一个非常大的群体),并且在预设的亚组分析中,吉瑞替尼对这一人群有益(HR=0.515,P=0.0065);而MRD阴性患者无获益(HR=1.213,p=0.575)。
该研究的目的是挑战以下假设:全球所有FLT3-ITD AML患者均应在HCT后接受FLT3抑制剂维持治疗,而结果证明该假设无效。HCT后使用吉瑞替尼维持治疗确实对FLT3-ITD AML患者有益,但仅对围HCT期FLT3-ITD MRD阳性的患者有益。研究还验证了FLT3-ITD突变作为MRD有用标志物的效用,且对干预具有明确意义。该研究的发现改变了临床实践,对数据的进一步研究可能有助于进一步了解该病的生物学和治疗。
专家评述
JCO杂志同期发表Naval G Daver和Charles Craddock两位专家的Editorial文章,认为MORPHO研究非常重要,因为它不仅证实了靶向治疗改善移植后结局的能力,还因为它强调应将allo-SCT视为 AML 综合性整体治疗路径的关键组成部分,包括诱导/巩固化疗、移植和移植后干预。
MORPHO研究提供了令人信服的证据,证明吉瑞替尼维持治疗可改善接受异基因移植且有移植前或围移植期MRD证据的FLT3突变AML患者的结局,而MRD阴性患者从吉瑞替尼维持治疗中无获益,反而可能暴露于不必要的毒性,包括药物毒性和经济毒性。
该数据对AML治疗过程中移植的最佳利用也具有更普遍的意义。首先,对于适合的FLT31 AML成人患者,无论移植前的MRD状态如何,应首选清髓性预处理方案,而非减低强度方案。其次,该研究首次确定使用移植前和围移植期MRD评估来指导移植后预防性干预的重要性。因此可以提出一种新的模式,即对于具有高复发风险的患者应定期进行MRD评估(包括移植前和移植后早期开始定期评估),而非按照目前的做法在移植后100日评估缓解状态。
对于有移植前或围移植期 MRD 证据的 FLT3+ AML 异基因移植患者,吉瑞替尼维持治疗是一种新的标准治疗;而对于因高危接受移植的非FLT3 AML患者,可能需要旨在增强 GVL 效应的干预措施,如快速免疫抑制减量或供者淋巴细胞输注。该研究也支持更广泛的基于药理学的维持研究作为缺乏 FLT3 突变的 AML 患者的减少复发策略,正在进行的 AMADEUS 研究评估使用口服阿扎胞苷 (CC486) 进行移植后维持治疗,其结果值得期待。
随着更多靶向治疗药物进入 AML 治疗模式,也可能为评估在 NPM1 或 KMT2A 突变患者中使用IDH抑制剂(如艾伏尼布、olutasidenib和enasidenib)或 menin 抑制剂进行移植后维持治疗的获益提供新的机会,或可通过移植前和围移植期 MRD 评估进行指导。更广泛地说,虽然多项回顾性和前瞻性研究证实MRD 对 AML 预后的重要性,但该研究首次将MRD确定为预测生物标志物,可用于指导AML 成人患者的治疗决策。
最后,该研究证实了既往化疗对移植结局的影响,并支持检查创新的诱导策略,其可能通过降低移植前 MRD 负荷或替代降低移植后复发或死亡率来改善移植结局。
许多因 AML 而接受异基因移植的患者仍死于疾病复发,因此迫切需要改善移植结局的创新策略,而MORPHO研究的结果提示可从精心设计的前瞻性随机移植研究中获得治疗红利。目前的许多移植实践仍基于回顾性登记数据集,存在伴随的偏倚,而嵌入基因组学和 MRD 分析(正如MORPHO研究)的前瞻性移植研究因其罕见性而值得注意。MORPHO研究中有40种不同的预处理方案(许多是在缺乏前瞻性随机数据的情况下使用的),而精心设计的MORPHO研究可适应这些方案,而这正是指导非移植实践的必要条件。BMT CTN在过去十年中提供了一系列影响临床实践的前瞻性移植研究,这值得赞扬。
参考文献
1.Levis MJ, et al.Gilteritinib as Post-Transplant Maintenance for Acute Myeloid Leukemia With Internal Tandem Duplication Mutation of FLT3.J Clin Oncol . 2024 Mar 12:JCO2302474. doi: 10.1200/JCO.23.02474.
2.Daver NG, Craddock C.Moving Toward Total Therapy in AML: Personalized Treatments Improve Post-Transplant Outcome.J Clin Oncol . 2024 Mar 12:JCO2400006. doi: 10.1200/JCO.24.00006.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#FLT3-ITD# #急性髓系白血病# #吉瑞替尼# #MRD#
45