Sci Transl Med:KRAS突变型肺癌或喜迎MEK抑制剂联合用药
2019-03-25 Michael 转化医学网
大约30%的癌症存在KRAS的活化突变,其通过称为MAPK的信号传导途径触发肿瘤发生与进展。虽然目前还没有直接针对KRAS的药物成功,但已经开发出针对MEK的靶向治疗。
导读
大约30%的癌症存在KRAS的活化突变,其通过称为MAPK的信号传导途径触发肿瘤发生与进展。虽然目前还没有直接针对KRAS的药物成功,但已经开发出针对MEK的靶向治疗。已知MEK是KRAS在癌症中促进MAPK级联反应的下游蛋白之一,因此针对MEK的靶向治疗理论上可抑制KRAS突变型肺癌,但实际效果一般。目前来自德克萨斯大学MD安德森癌症中心的研究人员发现ZEB1抑制剂可增强MEK的靶向治疗的效果,其最新的研究成果发表于《Science Translational Medicine》杂志。
通过肺癌细胞系和小鼠模型实验,肿瘤学副教授Don Gibbons领导的研究小组阐明了KRAS驱动的肺癌细胞是如何将肿瘤细胞从稳定、静止的细胞转化为一种与胚胎发育相关的可移动抗性细胞,进而躲避抗癌治疗的。该团队还发现一种联合用药,可以逆转这种细胞转化,恢复肿瘤细胞对靶向治疗的敏感性。
Gibbons表示,“在包括肺癌在内的多种临床肿瘤中尝试过MEK抑制剂对肿瘤的疗效,但其治疗结果并不乐观。这些药物并没有一直持续杀灭KRAS突变患者体内的肿瘤细胞,目前尚不清楚其原因”。
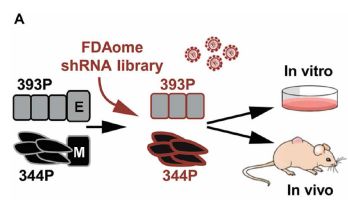
此次发现的这种间充质细胞在胚胎发育过程中极其活跃。由于胚胎干细胞可产生发育中胚胎发育所需的所有细胞类型,因此此时上皮细胞呈现间充质形式,一旦细胞正确“归位”,间充质细胞恢复到上皮形式并促进器官的形成。由于间充质细胞在胚胎发育过程中奇特的特性,因此其具有很高的迁移和侵袭能力,而这种上皮与间质的转化被称为上皮至间充质转换(EMT),这一转化目前已被明确广泛存在于肿瘤的发生和进展过程。
正常的机体均具有功能正常且分化良好的上皮细胞。这些上皮细胞分遍于全身各处。当肿瘤发生时,EMT基因被各种因素激活,具有正常功能的上皮细胞向间充质细胞转化,失去其原有的稳定功能,肿瘤组织因此得以发生发展,最终扩散于全身各处。
当用MEK抑制剂治疗具有上皮-间充质类型的KRAS突变肺癌肿瘤的小鼠模型时,间充质细胞从一开始就具有对MEK抑制剂的抗性,上皮细胞最初反应良好,但超过80%的肿瘤会随着时间的推移变得对MEK抑制剂耐药。
反转EMT,恢复MAPK
以前的研究表明,一种叫做组蛋白去乙酰化酶(HDAC)抑制剂的药物可以逆转EMT,使间充质细胞恢复到正常上皮细胞。在此次研究中,用HDAC抑制剂处理细胞可抑制ZEB1,逆转其EMT并恢复MAPK活性,使肿瘤细胞易受MEK抑制剂的控制。
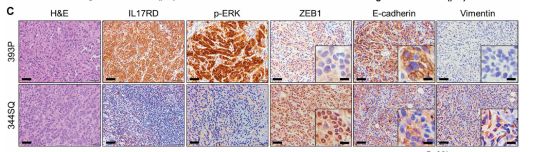
HDAC抑制剂和MEK抑制剂联合治疗缩小小鼠肿瘤
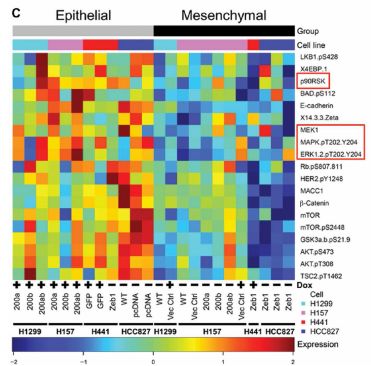
对人类肿瘤的几个大数据集的分析表明ZEB1与MAPK途径的激活之间存在负相关。用miR-200表达或HDAC抑制剂mocetinostat抑制ZEB1功能使敏感的癌细胞对MEK抑制敏感并显着降低体内肿瘤生长,显示出KRAS突变癌症极具潜力的联合用药策略。在人肺肿瘤样品中,高ZEB1和低IL17RD表达与低MAPK信号传导相关,提供预测患者对MEK抑制剂反应的潜在标志物。
此研究还侧重于将MEK抑制剂与免疫检查点抑制剂相结合,从而释放对肿瘤的免疫攻击。
原始出处:Peng DH1,2, Kundu ST1, Fradette JJ1, et al. ZEB1 suppression sensitizes KRAS mutant cancers to MEK inhibition by an IL17RD-dependent mechanism. Sci Transl Med. 2019 Mar 13;11(483).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#抑制剂#
52
#TRA#
47
#MEK#
57
#突变型#
53
#RAS突变型#
61
#Transl#
47
#KRAS突变#
65
#KRAS#
57
#MEK抑制剂#
51
#联合用药#
61