广西医科大学宁峙彭/新加坡国立大学陈小元ACS Nano:冷暴露疗法联合NO气体疗法介导乳腺癌放疗增敏及免疫治疗
2024-10-17 iNature iNature 发表于上海
本研究为CE与RT联合抗肿瘤治疗提供了坚实的理论基础和科学依据。
冷暴露疗法(CE)是一种低成本、无创治疗恶性肿瘤的新方法。当机体暴露在寒冷环境中,激活棕色脂肪组织(BAT)的产热代谢,快速诱导肿瘤饥饿,抑制肿瘤生长。CE引起的微环境改变可以进一步配合常规治疗(如放疗、化疗),提高传统治疗的效果。目前尚未有CE联合治疗的研究报道,因此科研人员迫切需要探索CE与传统疗法(如放疗)的联合抗肿瘤机制。2024年10月14日,广西医科大学宁峙彭教授、新加坡国立大学陈小元院士共同通讯在国际顶级期刊ACS Nano上以“Cold Exposure Therapy Sensitizes Nanodrug-mediated Radioimmunotherapy for Breast Cancer”为题发表了相关研究论文。

该研究构建了一种载有谷胱甘肽(GSH)反应性一氧化氮(NO)前药S-Nitroso-N-acetyl-DL-penicillamine(SNAP)的脂质体(SL)。肿瘤微环境内(TME)的GSH促进SL释放NO,随后,放疗产生的超氧阴离子(O2•-)与NO反应生成强氧化性的过氧亚硝酸盐(ONOO-),诱导肿瘤细胞死亡。CE对肿瘤组织有一系列影响,包括ATP水平和髓源性抑制细胞(MDSCs)的降低,以及GSH水平的下降,均有助于改善放疗(RT)的疗效。这项工作研究了CE联合NO气体疗法对肿瘤放疗增敏和促进肿瘤放射免疫治疗的影响,并突出了CE新疗法具有巨大临床应用前景。
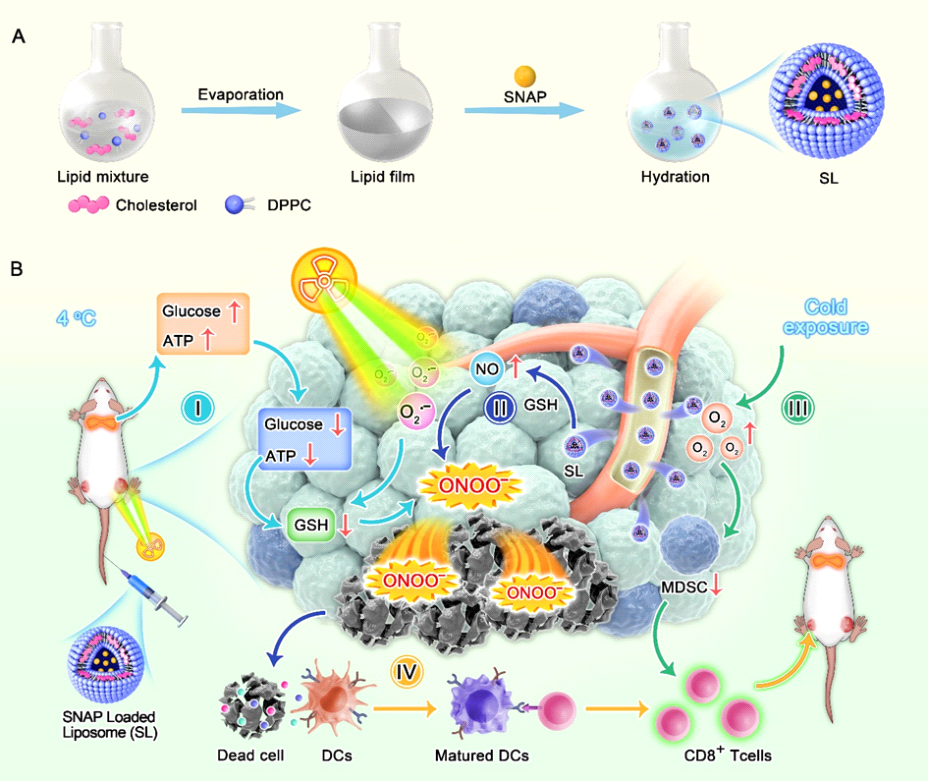
图1 SL介导的乳腺癌放射免疫治疗示意图
该工作对成功制备的具有GSH响应性释放NO和细胞内化能力的SL纳米平台进行了详细表征。结果显示,所制备的SL尺寸均一、成功负载SNAP、GSH响应性释放NO、并具有良好胶体稳定性。此外,DIO标记的SL与4T1细胞共孵育后,细胞的DIO荧光逐渐增强,并在4h后观察到最明显的DiO荧光,表明SL可以被癌细胞内化。
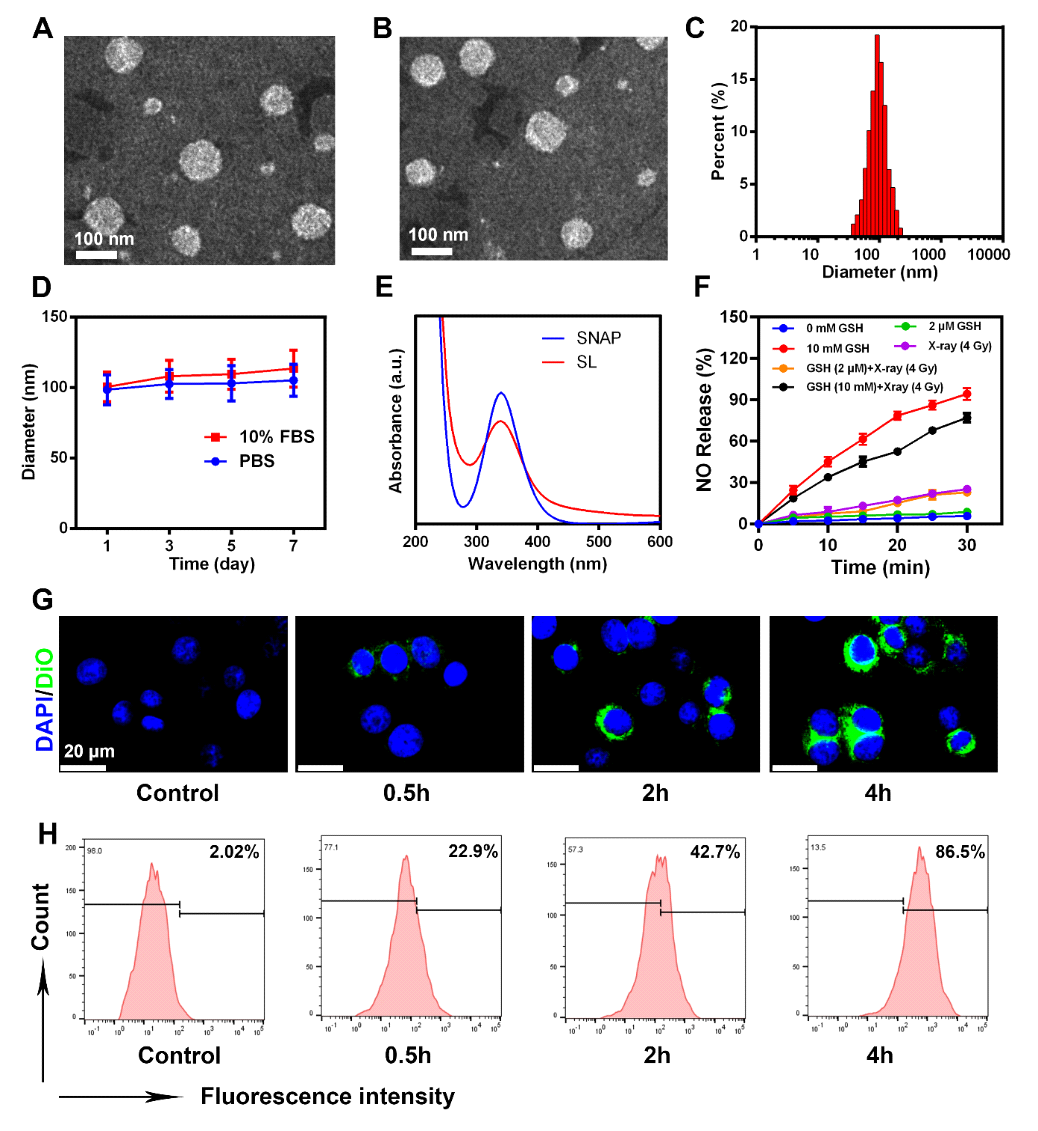
图2 SL的制备与表征
随后采用体外低糖(LG)培养肿瘤细胞模拟CE治疗诱导肿瘤组织中葡萄糖的减少,探索了SL在细胞水平抗肿瘤效果的评价。SL处理细胞后,肿瘤区域内的GSH促进SNAP中NO的释放。随后,RT产生的O2•-与NO反应生成具有强氧化性的ONOO-,诱导细胞死亡,抑制了细胞集落形成。对DNA双链断裂标记物γ-H2AX进行免疫荧光染色,结果表明SL+RT+LG组的γ-H2AX数量最多,说明SL+LG处理引起的RT致敏性最大。同时,研究了不同组4T1细胞在不同辐射剂量下的存活分数,LG、SL和SL+LG均有放射致敏作用,其中SL+LG作用最强。LG治疗诱导肿瘤中ATP和GSH含量降低,其中SL+LG+RT治疗使GSH和ATP的消耗最大化。
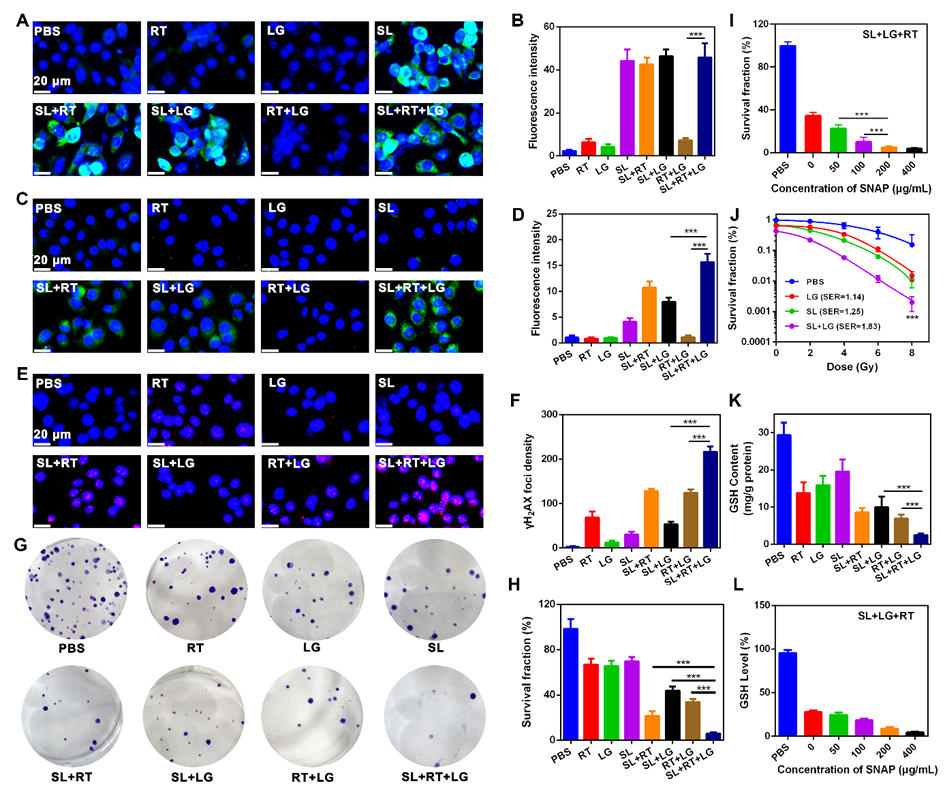
图3 SL体外抗肿瘤疗效评价
接着,该工作对SL联合NO气体促进RT诱导的免疫原性细胞死亡(ICD)进行了系统的表征。免疫荧光图像和流式细胞术定量分析的结果显示,SL+RT+LG组处理的细胞中观察到最强的CRT表达量,说明SL联合RT和LG可上调4T1细胞的CRT表达。免疫荧光成像显示HMGB1从肿瘤细胞中释放,同时通过ELISA测定SL+RT+LG组细胞释放的HMGB1量明显高于其他组。以上结果表明,SL+RT+LG可诱导ICD,有利于肿瘤免疫治疗。通过Transwell实验进一步证明SL+RT+LG组诱导的ICD可增强免疫原性抗原的释放,从而导致树突状细胞(DCs)的成熟和浸润,进一步提高T细胞介导的抗肿瘤免疫潜力。
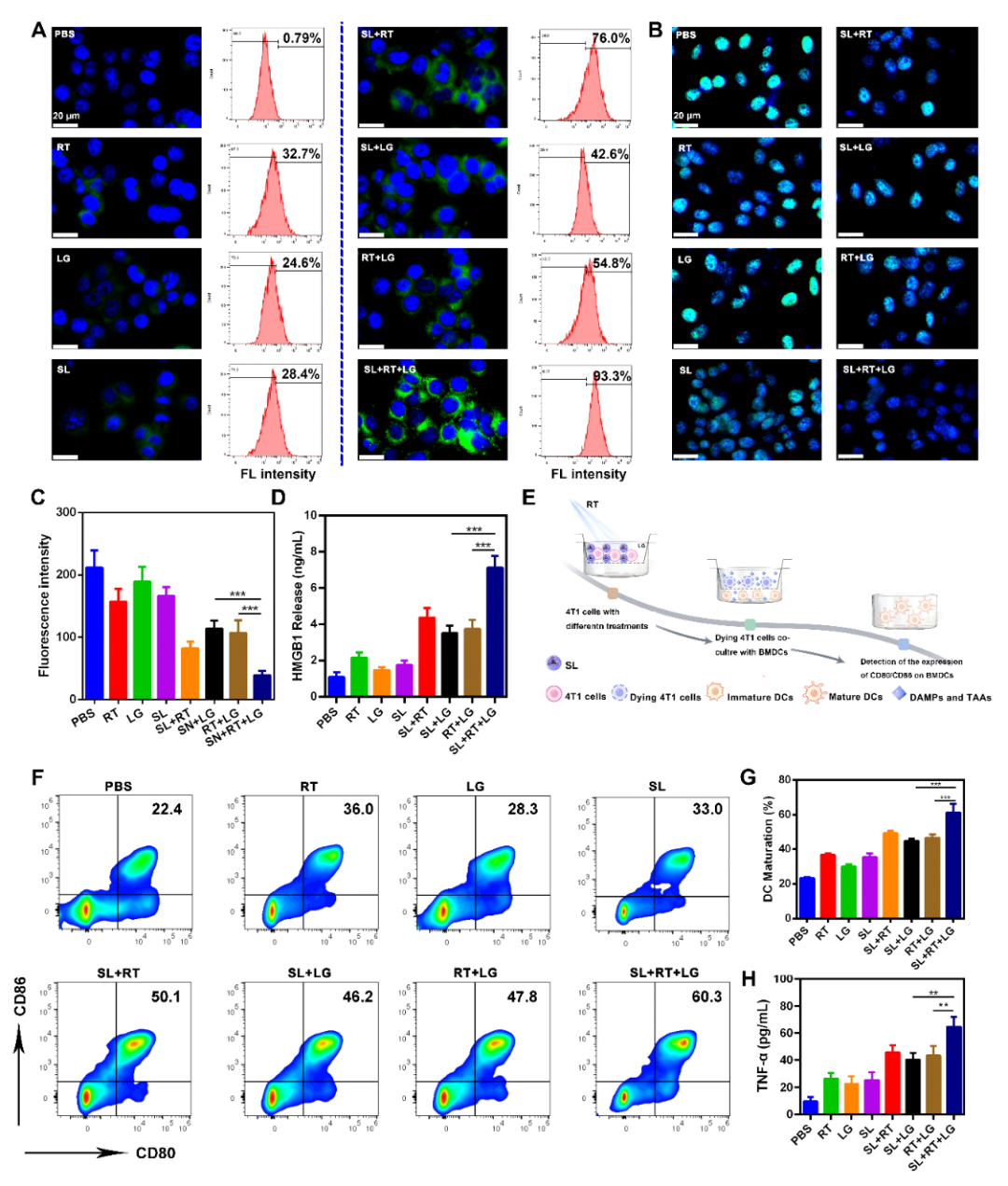
图4 体外诱导ICD
进一步探讨SL+RT+CE联合治疗策略对4T1荷瘤小鼠的抗肿瘤作用。结果显示,SL+RT+CE联合治疗策略在体内展现出显著的治疗效果。随后为了确认联合治疗对细胞还原系统的影响,评估了两种主要还原物质NADPH和GSH的水平。在氧化作用下,NADPH和GSH会转化为相应的氧化形态NADP+和GSSG,从而失去还原能力。SL+RT+CE组的NADP+/NADPH比率显著增加,总谷胱甘肽浓度和GSH/GSSG比值下降,进一步增加ROS的生成。为深入探讨SL+RT+CE的抗肿瘤免疫机制,采用流式细胞术分析成熟DC细胞、肿瘤浸润调节性T细胞(Tregs)和CD8+T细胞。结果表明SL+RT+CE治疗最大程度地激活了抗肿瘤免疫。
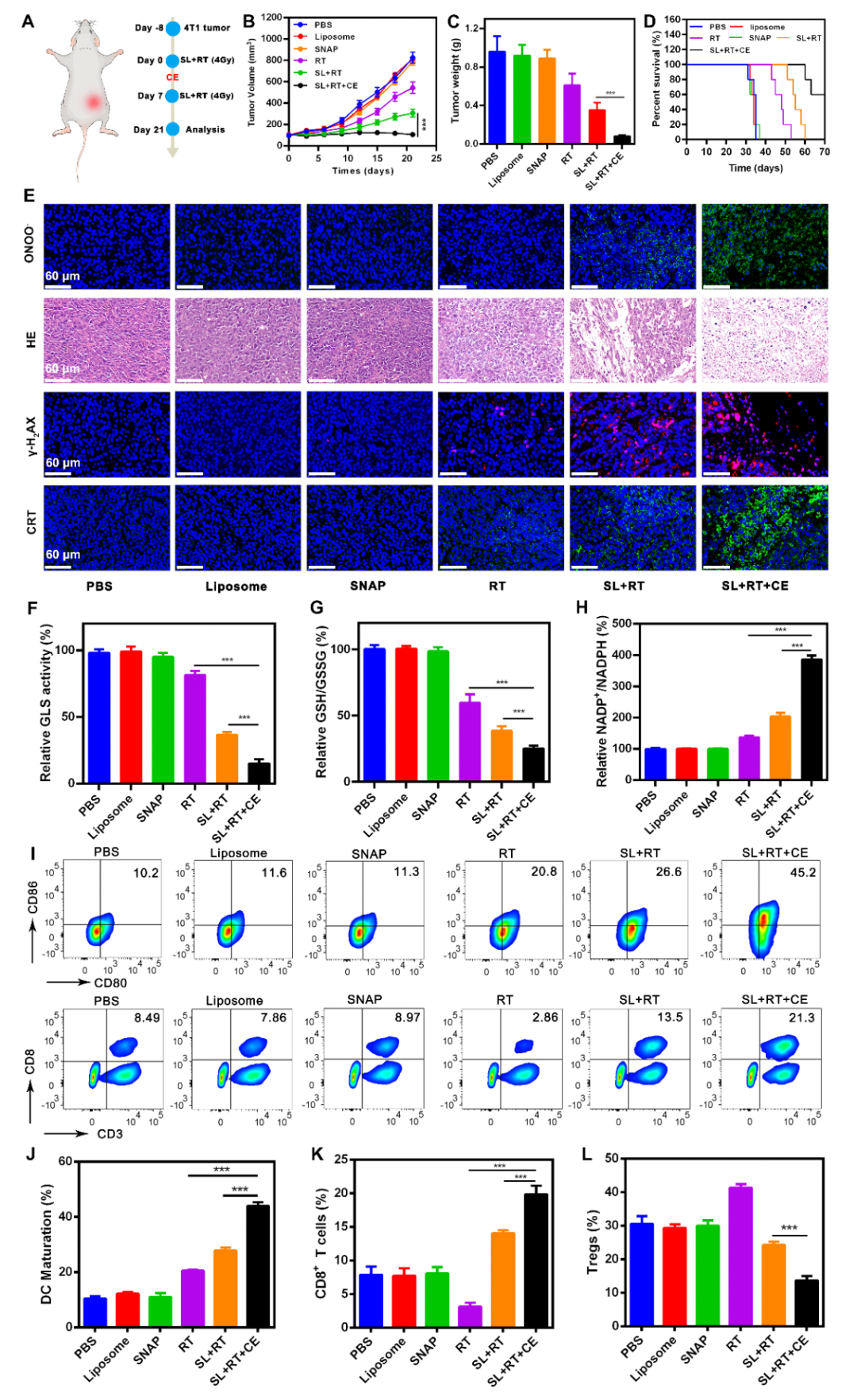
图5 体内抗肿瘤效果评价和免疫激活研究
该工作创新性的研究了CE联合NO气体治疗对肿瘤放疗增敏和促进肿瘤放射免疫治疗的作用。结果证实在放疗和NO气体治疗的基础上进行CE处理的小鼠比在温暖条件下处理的小鼠表现出更好的抗肿瘤免疫刺激,肿瘤部位的MDSCs和Tregs含量降低。本研究为CE与RT联合抗肿瘤治疗提供了坚实的理论基础和科学依据。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.4c09021
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















结果证实在放疗和NO气体治疗的基础上进行CE处理的小鼠比在温暖条件下处理的小鼠表现出更好的抗肿瘤免疫刺激,肿瘤部位的MDSCs和Tregs含量降低。
15
#乳腺癌# #冷暴露疗法# #NO气体疗法#
97