西工大李鹏教授课题组ACS Nano:发射“抗生素炮弹”的“气动纳米炮”抗感染促成骨涂层
2024-06-28 BioMed科技 BioMed科技 发表于上海
钛植入物面临抗感染和骨整合挑战,西北工业大学团队设计近红外响应“气动纳米炮”涂层,实现可控抗菌和稳定成骨,为改进钛植入物功能提供新策略。
钛及其合金因其卓越的机械性能和生物相容性,在骨科植入物领域有着广泛的应用。然而,尽管其性能优异,钛植入物仍面临着一系列挑战,特别是在抗感染和骨整合方面。研究表明,钛材本身对于促进骨组织与植入物之间的整合能力有限,且难以抵御植入过程中病菌的侵袭,这是导致术后无菌性松动和细菌感染风险的主要原因。因此,为了进一步提升钛基植入物的临床应用效果,需要深入研究并开发新的表面改性技术,以增强其骨整合和抗感染能力。然而,植入体表面的不同功能对时效性具有特定的需求。具体而言,抗菌功能应具备响应性和可控性,能在感染发生或即将发生时被有效激活;促成骨功能应具备稳定性和长时间持续性。
近期,西北工业大学柔性电子研究院李鹏教授课题组设计了一种基于SrTiO₃纳米管(SrNT)的近红外(NIR)光响应“气动纳米炮”涂层。该涂层通过气泡的产生,实现了对抗生素(Cip)的响应性递送和Sr²⁺离子的持续释放,从而展现出按需释药的抗菌效果和稳定的成骨性能(图1)。该涂层以抗生素为“炮弹”,以碳酸氢铵(NH₄HCO₃)为“推进剂”,通过贻贝启发的聚多巴胺(PDA)表面沉积技术,将其封装进“炮管”(SrNT)内。由于PDA具有良好的光热转换效率,在NIR的照射下,NH₄HCO₃发生热分解,在SrNT涂层内部产生CO₂和NH₃气泡,这些气泡会破坏涂层PDA的封装效果,并且外溢推动抗生素的释放,实现抗菌药物的可控释放。不仅如此,SrNT涂层还能够持续稳定地释放具有成骨活性的Sr2+离子,以增强植入体的骨整合效果。
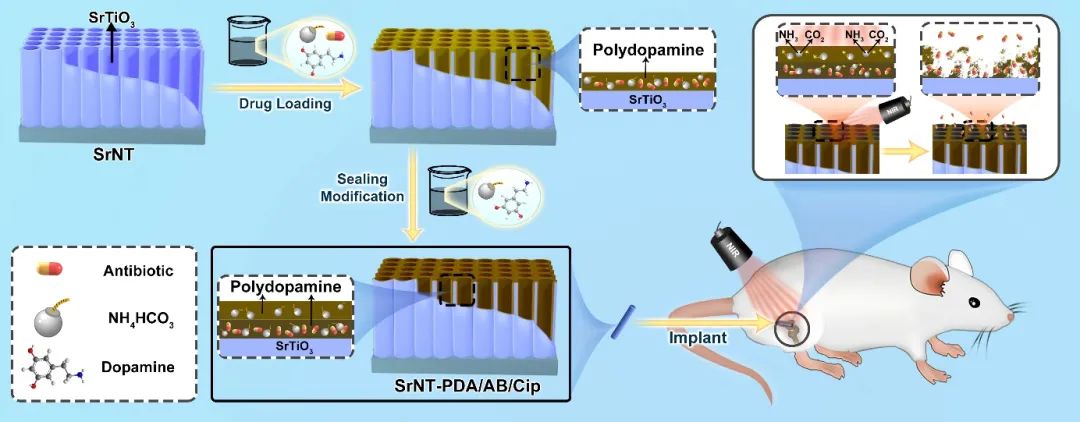
图1 钛植入体表面“气动纳米炮”涂层示意图。
实验结果显示(图2),该涂层在NIR(808 nm)光照下,表面有明显的气泡生成现象,意味NH4HCO3可被光照控制有效分解。因此,该涂层展现出了显著的抗生素响应性释放效果,与模拟感染微环境pH条件下,施加NIR光照时其24 h释放量与无NIR光照时相比提升接近3倍,相比于中性环境中无NIR光照时释放量提升了近6倍。除此之外,该涂层对Sr2+的释放具有良好的稳定性,释放持续时间超过28 天。因此,该涂层能够提供给钛植入体表面可控的杀菌性能以及稳定的促成骨效果。
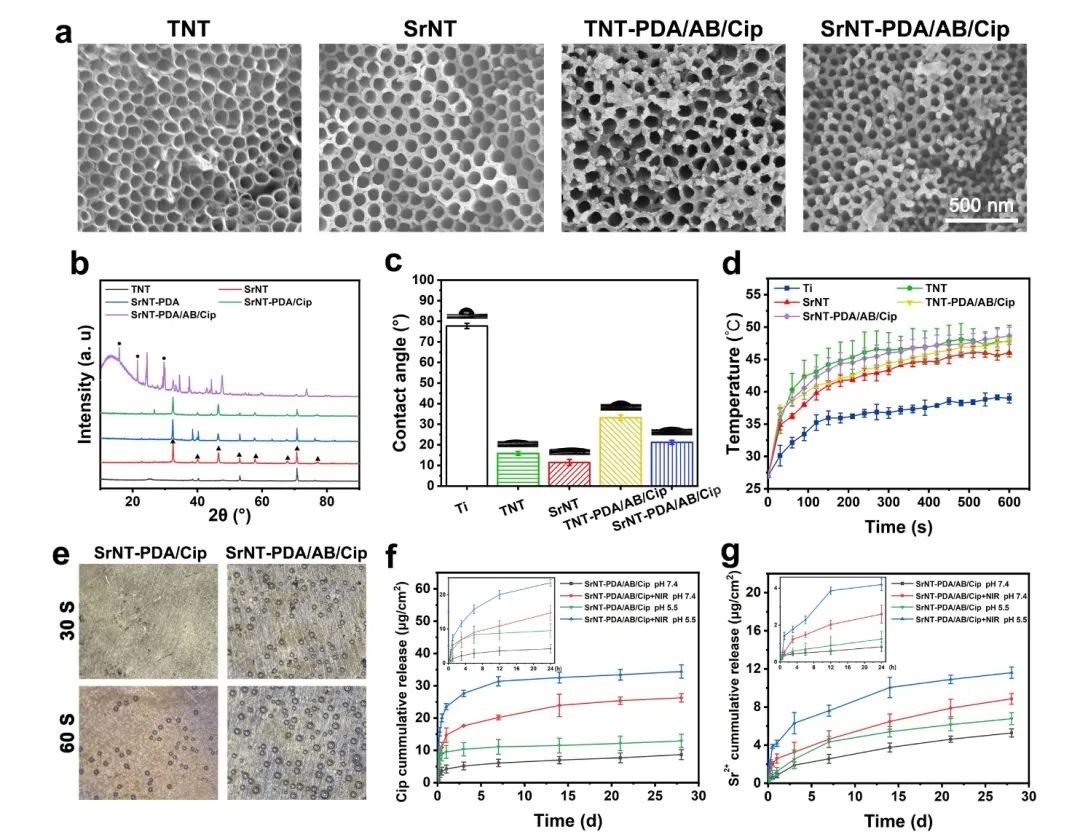
图2.(a)不同样品表面的SEM图像,(b)XRD图谱,(c)水接触角和(d)NIR光热转换曲线。(e) 在30秒和60秒的NIR照射下不同样品表面产生的气泡的照片。浸泡于PBS中样品的(f)抗生素和(g)Sr2+释放曲线。
该“气动纳米炮”涂层展现出了显著可控的抗菌性能(图3)。NIR的照射成功触发涂层中抗生素的快速释放,显著增强了其抗菌潜力,使得涂层对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)具有强力的抗菌效果(抗菌率>99.99%)。不仅如此,在NIR光照条件下,样品针对E. coli的抑菌圈直径相较于无NIR光照时增加了50%以上,针对S. aureus的抑菌圈直径增加了70%以上,这进一步证明了NIR对样品抗菌效果的增强是由于抗生素的释放所导致的,并且其抗菌效果非常显著。
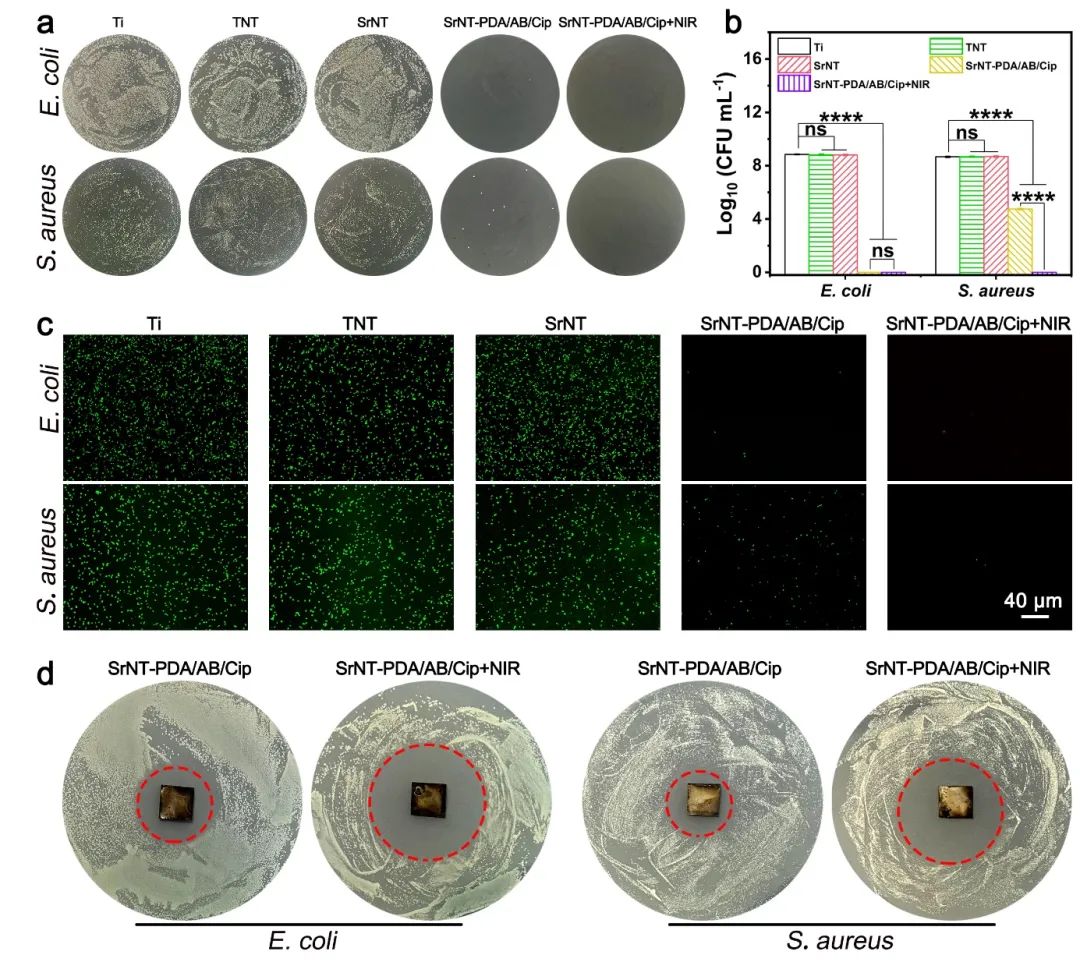
图3.不同样品对典型革兰氏阴性菌(大肠杆菌)和革兰氏阳性菌(金黄色葡萄球菌)的抗菌活性表征:(a)细菌涂板观察,(b)菌落计数,(c)活/死细菌荧光染色,(d)抑菌圈。
该涂层在大鼠股骨骨髓炎感染模型中展示出了良好的治疗效果。在植入后,NIR光能够有效穿透组织,显著提升了该涂层的抗菌性能,相较于没有NIR光照时植入部位菌落数减少了49%,并且NIR光照情况下其体内抗菌效率达到99.88%(图4)。同时,该涂层对骨整合也有显著的促进作用,在植入28天后,其周围的新骨生成量显著高于原始钛植入体,并且小梁分离度显著减少(图5),有效的提高了钛植入体的骨整合性能。
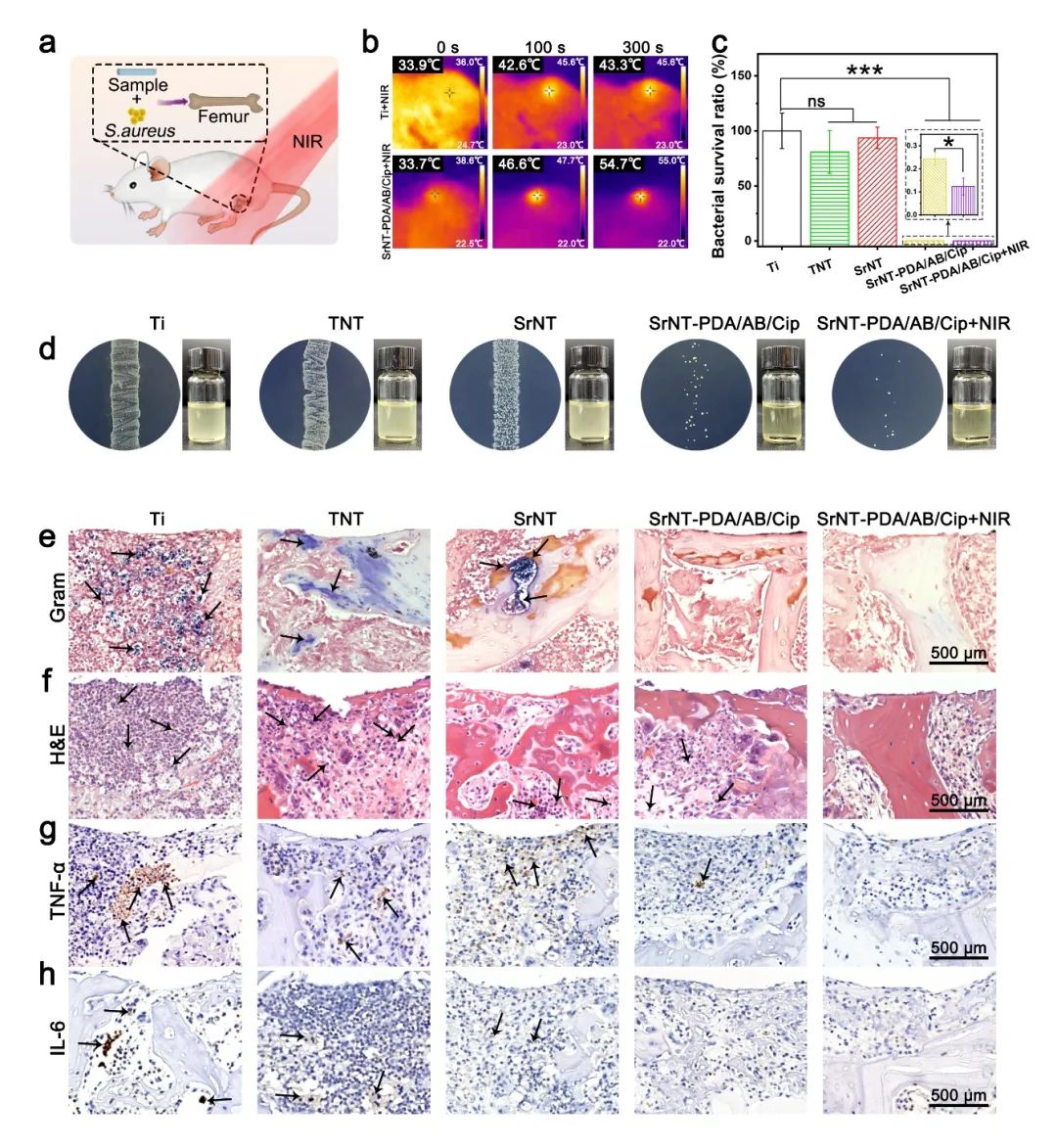
图4.植入7 d后不同样品的体内抗感染活性表征:(a)植入物相关感染的大鼠模型示意图,(b)植入后不同样品的光热成像,(c)细菌存活率,(d)细菌菌落图像,(e)革兰氏染色(箭头:细菌),(f) H&E 组织学染色(箭头:中性粒细胞),促炎因子(g)TNF-α 和 (h) L-6的免疫组织化学染色(箭头:阳性部位)。
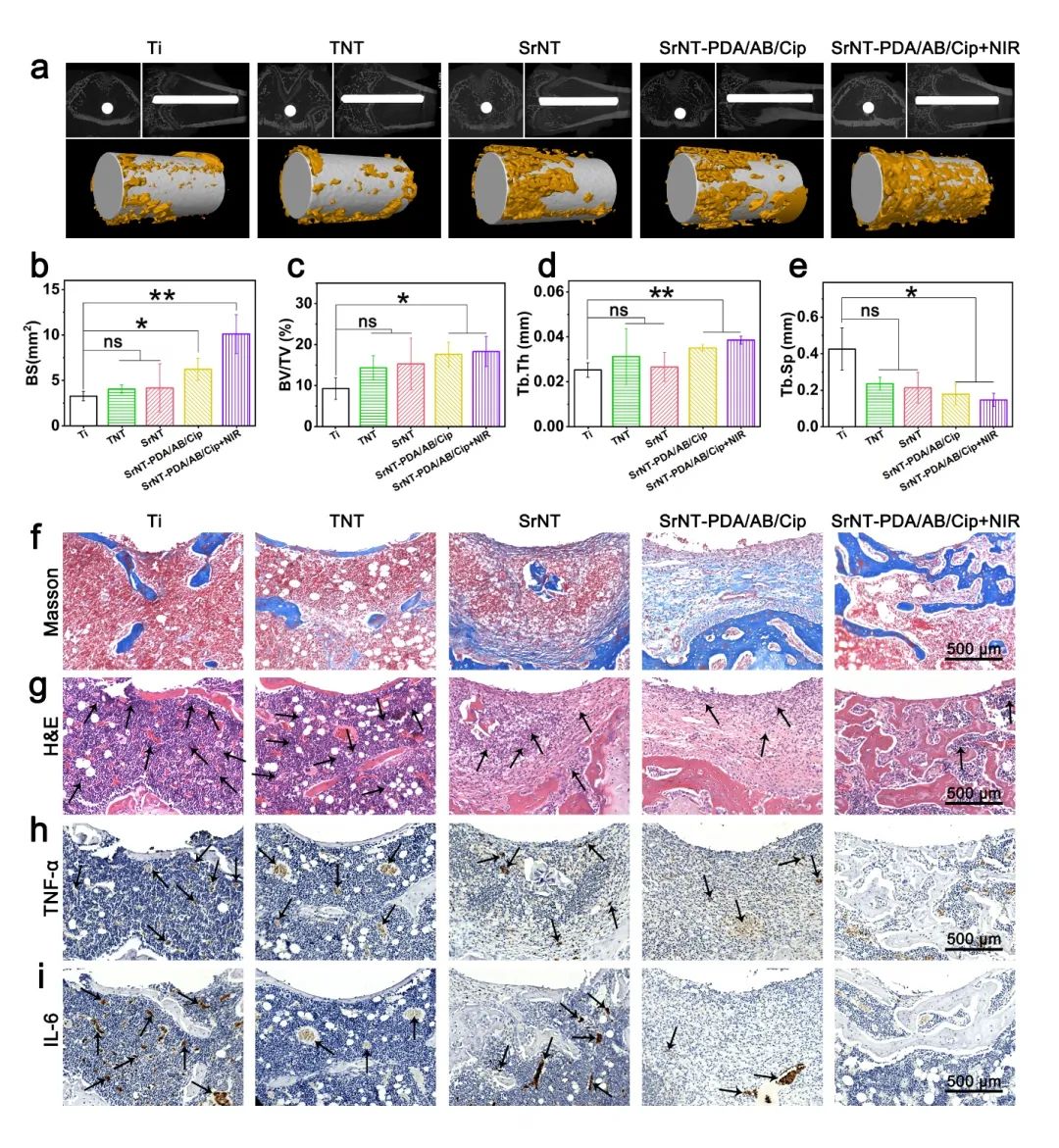
图5. 植入28 d后不同样品的体内成骨活性表征:(a) 不同样品植入后的Micro-CT图像,(b)BS、(c)BV/TV、(d)Tb.Th 和(e)Tb.SP 的定量计算,(f)Masson三色染色,(g)H&E组织学染色(箭头:中性粒细胞),促炎因子(h)TNF-α 和(i)IL-6的免疫组织化学染色(箭头:阳性位点)的图像。
本研究在钛基植入物表面构建的“气动纳米炮”涂层,在NIR照射下可控释放抗菌药物,持续释放成骨活性离子,不仅可响应性抑制植入物相关感染,而且可增强植入体骨整合效果。该涂层为钛植入物的抗感染、促成骨功能改进提升提供了新的策略,具有临床应用潜力和广阔前景。
相关工作以“SrTiO3 Nanotube-based “Pneumatic Nanocannon” for On-demand Delivery of Antibacterial and Sustained Osseointegration Enhancement”为题,发表在ACS Nano (DOI:10.1021/acsnano.4c04478)上。西北工业大学李鹏教授为该论文通讯作者。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.4c04478
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












签到学习
39
#骨整合# #钛植入物# #SrTiO₃纳米管#
45