Circ Res .:SMYD2 甲基化的 PPARγ 通过激活线粒体自噬促进缺氧诱发的肺动脉高压
19小时前 刘少飞 MedSci原创 发表于加利福尼亚
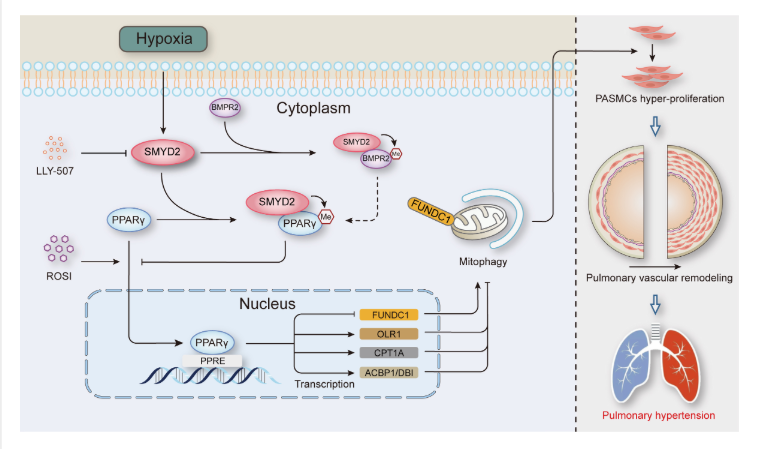
本研究结果表明,SMYD2通过对非组蛋白PPARγ的单甲基化,抑制其核转位和活化,从而通过触发线粒体自噬(mitophagy)加速PASMCs的增殖和PH的发展。

背景:
肺动脉高压(PH)的关键病理特征是肺动脉平滑肌细胞(PASMCs)的过度增殖及其导致的肺血管重塑。研究表明,蛋白质甲基化在PASMCs的增殖和PH的发生中具有关键作用,但其潜在机制仍不清楚。
方法:
通过对小鼠/大鼠进行为期4周的慢性缺氧处理,构建PH动物模型。研究中使用了SMYD2-vTg小鼠(特异性在血管平滑肌细胞中过表达SMYD2的转基因小鼠,SMYD2即抑制杂色性、增强子zeste、Trithorax和髓样Nervy DEAF-1结构域蛋白2)和野生型小鼠/大鼠,并通过LLY-507(3-氰基-5-{2-[4-[2-(3-甲基吲哚-1-基)乙基]哌嗪-1-基]-苯基}-N-[(3-吡咯烷-1-基)丙基]苯甲酰胺)处理,研究SMYD2在体内对PH发病的作用。此外,利用SMYD2敲低或过表达的大鼠原代PASMCs,探索SMYD2对细胞增殖的影响及其潜在机制。
结果:
我们发现,SMYD2(赖氨酸甲基转移酶)在PH患者和缺氧处理的大鼠/小鼠的肺动脉平滑肌细胞中表达上调,在缺氧诱导的大鼠PASMCs细胞质中也观察到了这一现象。更重要的是,LLY-507靶向抑制SMYD2,可显著减轻缺氧诱导的肺血管重塑和PH的发展,这一效果在体内的雄性和雌性大鼠中均得到验证。此外,LLY-507还在体外显著减少了大鼠PASMCs的过度增殖。相比之下,SMYD2-vTg转基因小鼠在接受4周的慢性缺氧处理后,表现出比非转基因小鼠更严重的PH表型和相关的病理变化。
进一步的研究表明,SMYD2的过表达促进了大鼠PASMCs的增殖,而SMYD2的敲低则抑制了这一过程,这与S期和G2期之间的细胞周期检查点的变化有关。机制研究显示,SMYD2可直接与过氧化物酶体增殖物激活受体γ(PPARγ)相互作用,并使其发生单甲基化修饰,从而抑制PPARγ的核转位和转录活性。这一过程进一步促进了线粒体自噬(mitophagy),加速了PASMCs的增殖和PH的发展。此外,PPARγ激动剂罗格列酮(rosiglitazone)能够显著消除SMYD2过表达对PASMCs增殖和PH的有害影响。
结论:
本研究结果表明,SMYD2通过对非组蛋白PPARγ的单甲基化,抑制其核转位和活化,从而通过触发线粒体自噬(mitophagy)加速PASMCs的增殖和PH的发展。该研究提示,靶向抑制SMYD2或激活PPARγ可能是预防和治疗PH的潜在策略。
参考文献:
Li Y, Wei X, Xiao R, Chen Y, Xiong T, Fang ZM, Huo B, Guo X, Luo H, Wu X, Liu L, Zhu XH, Hu Q, Jiang DS, Yi X. SMYD2-Methylated PPARγ Facilitates Hypoxia-Induced Pulmonary Hypertension by Activating Mitophagy. Circ Res. 2024 Jun 21;135(1):93-109. doi: 10.1161/CIRCRESAHA.124.323698. Epub 2024 May 21. PMID: 38770649.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#肺动脉高压# #缺氧# #SMYD2 甲基化#
5