JMC:中国药科大学报道新型第四代EGFR抑制剂,可有效对抗奥希替尼耐药!
2023-05-07 精准药物 网络 发表于上海
中国药科大学报道新型第四代EGFR抑制剂,可有效对抗奥希替尼耐药!
研究内容来自2023年5月4日 J. Med. Chem 发表的文章:
通讯作者:中国药科大学(杨鹏、肖易倍和孙昊鹏)
激酶及BaF3细胞活性评价:药物筛选中心

第三代EGFR-TKI:第一、二代EGFR-TKI使用不久出现耐药,超过半数的耐药原因是肿瘤细胞EGFR激酶结构域的又一新型突变,这个突变就是现在认识比较清晰的790位苏氨酸(Thr,简称T)点突变为甲硫氨酸(Met,简称M),一般称之为“T790M”。三代EGFR-TKI对“L858R”合并“T790M”、“exon19 del”合并“T790M”的EGFR突变肿瘤细胞均表现出明显抑制活性,同时具备一定选择性(不明显抑制野生型),代表(曾)上市药物有奥希替尼、阿美替尼、伏美替尼、olmutinib、Lazertinib(韩国上市)。
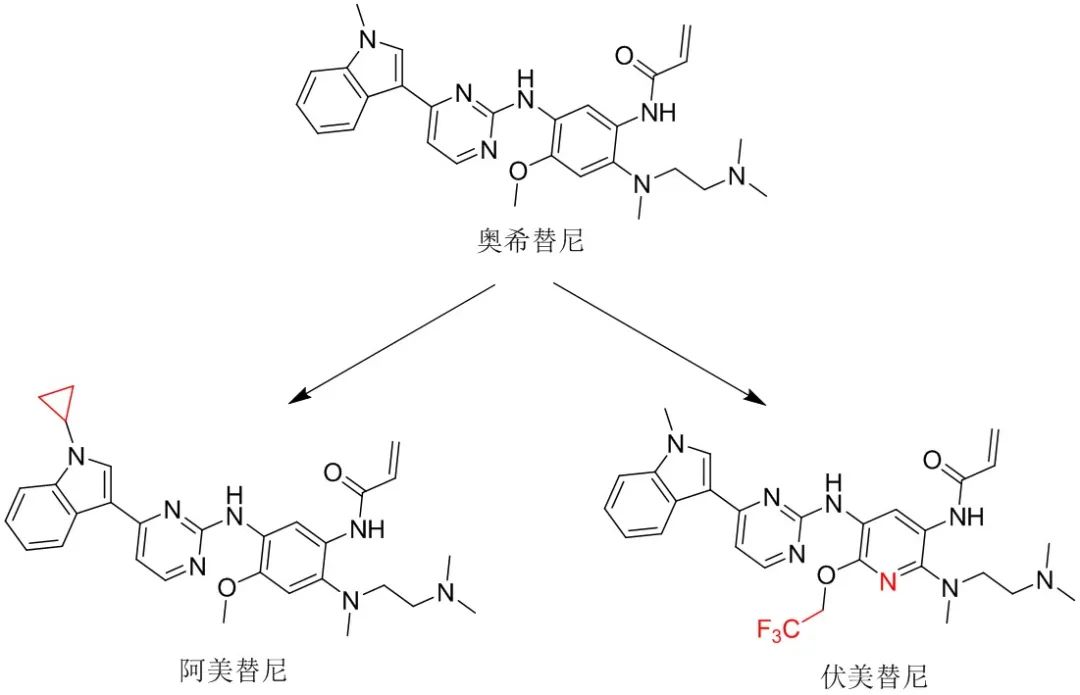
所有的第三代EGFR抑制剂都有一个丙烯酰胺弹头,可与Cys797残基发生共价反应,从而提高与细胞内高浓度ATP(mM水平)的竞争力。为了解决耐药问题而生的奥希替尼等第三代EGFR-TKI,也不可避免地会出现了耐药现象。EGFR-TKI耐药机制分为EGFR相关与EGFR非相关两种,其中EGFR相关的耐药约占30%~45%,C797S突变占比20%左右,三级 C797S (Cys 797 → Ser 797 ) 突变会破坏Cys797和丙烯酰胺弹头之间的共价形成。
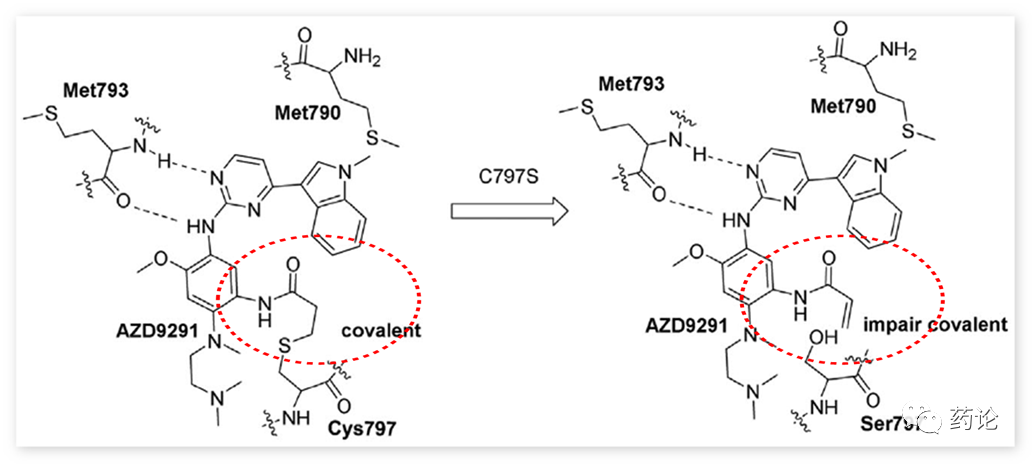
奥希替尼与EGFR/T790M和EGFR/C797S结合作用的示意图(来源:文献3)
尽管具有反式EGFR(T790M/C797S)突变的患者(其中T790M和C797S突变位于不同的等位基因上)可以通过第一代和第三代EGFR-TKI组合来有效地治疗,但是占到85%的顺式- EGFR(T790M/C797S)突变(突变位于相同等位基因)介导的耐药性仍然是未满足的临床需求。
许多努力致力于开发新药来克服含有 C797S 的 EGFR 三重突变(L858R/T790M/C797S 或 Del19/T790M/C797S),目前这一领域已经取得了令人瞩目的进展,但是仍然没有第四代 EGFR-TKI 获批上市。
2023年5月4日,JMC杂志报道了中国药科大学研究人员发现的一系列经过合理设计的作为第四代抑制剂的奥希替尼衍生物,优选化合物 D51 作为一种非共价的、有效的、选择性的第四代 EGFR 抑制剂,它可以有效抑制 EGFR L858R/T790M/C797S 突变体,同时对野生型 EGFR 没有明显抑制。

尽管携带EGFR L858R/T790M/C797S的患者获得了对奥希替尼的抗性,但奥希替尼在体外分别对三重突变的EGFR和BaF3-TM细胞(EGFR L858R/T790M/C797S)表现出适度的抑制活性(IC50=546nM)和抗增殖活性(IC50 = 1.6μM)。因此,奥希替尼被作为先导化合物进行药物设计。上面已经提到,奥希替尼耐药的主要机制是靶标蛋白EGFR的Cys797突变,阻碍与奥希替尼丙烯酰胺弹头形成共价键,研究人员拟通过环化策略增加化合物与突变体之间的相互作用。
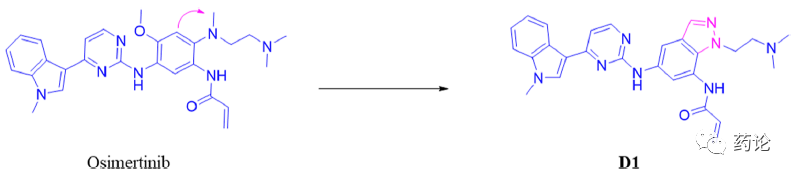
用奥希替尼环化策略设计新化合物(文献1)
具有三重突变的 EGFR与 D1 的分子对接 LibDock 为研究人员的分子设计提供支持,研究人员在晶体结构中保留了奥希替尼与EGFR L858 R/T790M/C797S的结合模式,并在计算机中将D1与相同的蛋白对接。结果表明,该设计促进了 Leu-718 和吲唑环之间 π-alkyl 的形成,并保留了氨基嘧啶和 Met-793 之间形成的氢键。
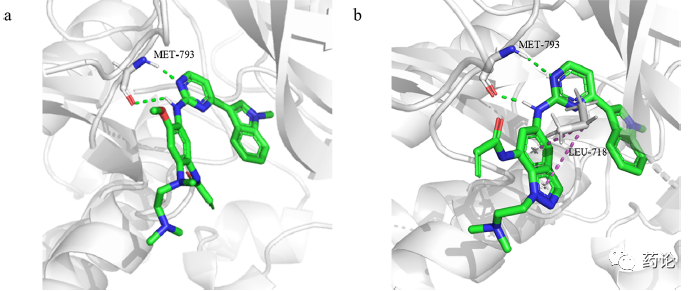
EGFR L858R/T790M/C797S 与奥希替尼 (a) 和 D1 (b) 结合模型的比较。氢键以绿色虚线显示,π-alkyl相互作用以紫色虚线显示 (PDB: 6LUD)。(来源:文献1)
在构效关系分析研究中,Brigatinib 被用作阳性对照,经过一系列优化筛选,最终优选出 5 种 IC50 值小于15nM的化合物,用于进一步评估针对不同EGFR突变体的不同细胞系的细胞活性。选择三种含有不同 EGFR 突变体的 NSCLC 细胞系,含有三重突变 EGFR 的工程化 BaF3 细胞系、BaF3 亲本细胞和含有野生型 EGFR 的 NSCLC 细胞系,以评估化合物的体外抗增殖和选择性。奥希替尼用作阴性对照。临床I期第四代抑制剂 TQB-3804 和 Brigatinib 作为阳性对照。最终,D51被优选为最佳的细胞活性化合物。
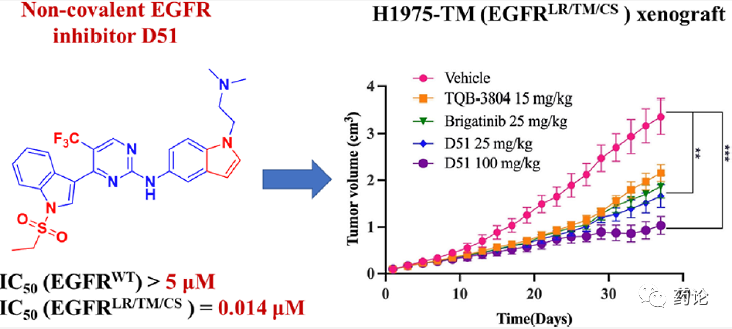
D51结构和综合性能(文献1)
Brigatinib 由日本武田制药研发,属于ALK抑制剂,美国FDA于2017 年4月28日批准Brigatinib上市,用于对克唑替尼不耐受或用药后疾病进展的ALK阳性的转移性非小细胞肺癌患者。2020年5月22日,FDA批准Brigatinib一线治疗ALK阳性的转移性非小细胞肺癌的成人患者。临床研究发现,Brigatinib或Brigatinib联合西妥昔单抗(cetuximab)等对Del19/T790M/C797S突变显示出良好的抑制率。
TQB3804由正大天晴与药明康德联合研发的第四代EGFR-TKI,TQB3804对于EGFRd746-750/T790M/C797S、L858R/T790M/C797S、d746-750/T790M和L858R/T790M具有很强的活性,IC50分别为0.46、0.13、0.26和0.19nM。
D51 对EGFR L858R/T790M/C797S 突变体的 IC50 值为 14nM,选择性是 EGFR野生型 (>5000 nM) 的 500 倍,D51还抑制 EGFR del19/T790M/C797S 突变体,IC50 值为 62nM。D51 表现出针对各种 EGFR 突变细胞的显着抗增殖活性和显着的成药性。
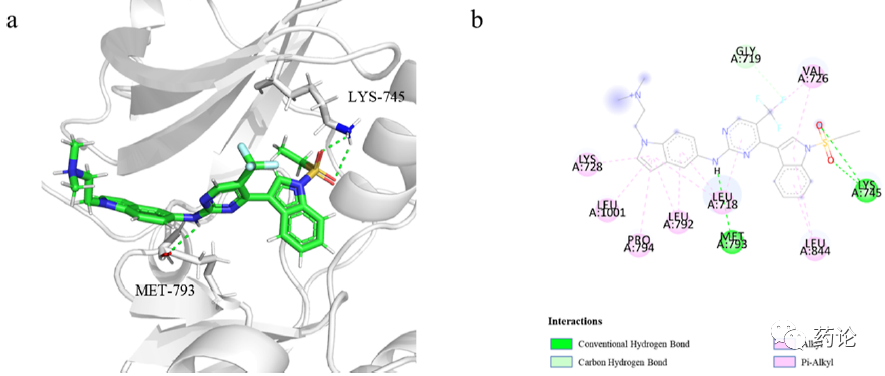
EGFR L858R/T790M/C797S 与 D51 的结合模型。(a) 3D结合模式;(b) 化合物和蛋白质之间的2D相互作用 (PDB: 6LUD)。(文献1)
研究人员进一步评估了 D51 在接种 H1975-TM(EGFR L858R/T790M/C797S)细胞的异种移植小鼠模型中的抗肿瘤功效。D51以25和100mg/Kg的剂量口服给药,每天一次。37天的连续用药之后,D51以剂量依赖的方式显著抑制异种移植肿瘤的生长,在 D51 处理的组中,肿瘤生长抑制率在50%至80%的范围内。相比之下,阳性对照 TQB-3804 和 Brigatinib 不如D51有效。
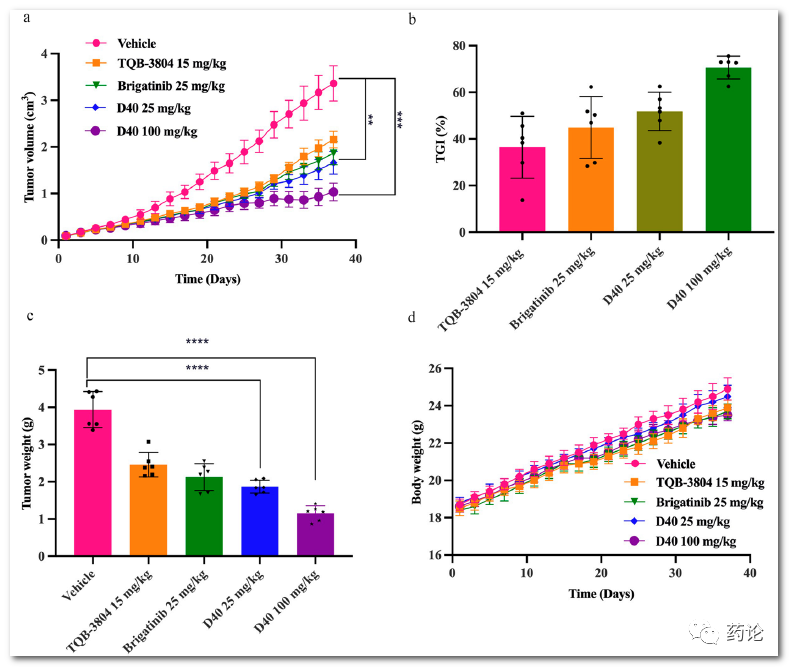
D51在H1975-TM异种移植小鼠模型中的抗肿瘤作用(来源:文献1)
此外,D51处理组(25和100 mg/kg)的平均肿瘤重量小于阳性对照组。所有组的耐受性良好,在实验过程中对体重没有影响。这些数据表明,D51可以显著抑制携带EGFR L858R/T790M/C797S的非小细胞肺癌肿瘤的发展,并且在体内具有良好的安全性。
总之,上述研究提供了一种有效且特异性强的 EGFR 抑制剂,其具有新型化学分子骨架以供进一步开发来克服对奥希替尼耐药的 EGFR C797S 突变。
参考:
1.https://doi-org.hy272.top/10.1021/acs.jmedchem.3c00277
2.https://www.cpu.edu.cn/
3.Lu X, Yu L, Zhang Z, et al. Targeting EGFRL858R/T790M and EGFRL858R/T790M/C797S resistance mutations in NSCLC: Current developments in medicinal chemistry[J]. Medicinal research reviews, 2018, 38(5): 1550-1581.
4.https://doi.org/10.1021/acs.jmedchem.1c01055.
5.https://www.rcsb.org/3d-view/6LUD
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言