npj Parkinsons Dis:血管周间隙,在早期帕金森病中,作用如何?
2022-04-13 Freeman MedSci原创
PVS负担指数是评估PD运动症状严重程度的候选生物标志物
血管周围空间(PVSs)是围绕着血管的液体填充空间,从脑表面穿过脑实质。它是中枢神经系统的一种正常解剖结构,通常在基底神经节(BG)、半卵白质中心、中脑和海马中观察到。

 图1 论文标题图
图1 论文标题图
尽管对PVS的研究结果仍有争议,但PVS的负担已被证明与衰老、认知能力、睡眠质量和抑郁状态相关。它被描述为神经系统疾病的一个特征,包括小血管疾病、阿尔茨海默病(AD)、多发性硬化症,以及帕金森病(PD)。
PD是一种慢性神经退行性疾病,以运动症状(静止性震颤、运动迟缓、僵硬和步态异常)和非运动症状(抑郁、焦虑、认知能力下降等)为特征。PD的病理特征是多巴胺能神经元变性和α-突触蛋白在黑质(SN)的异常沉积。
最近的研究表明,PVS系统在帕金森病中起着改变病情的作用。由于PVS系统参与了排除代谢废物的淋巴排泄系统,并且有证据表明PVS系统有助于从脑间质液中驱除参与神经退行性疾病的可溶性蛋白,因此我们也认为PVS参与了异常α-突触核蛋白的清除,其功能障碍可能会加重PD的病理变化。
通过磁共振成像(MRI)技术,扩大的PVS变得可见和可测量。PVS负担被定义为PVS量化指标,代表PVS扩大的严重程度,包括PVS的数量和体积。以前的研究报告说,PVS可能有助于运动症状的特征性不对称,并可能是评估PD认知能力下降的一个有用的神经影像学生物标志物。
PVS的生理和病理生理机制可能反映在其邻近的白质上,因为PVS的负担与白质高密集度相关。这些研究部分地解释了PVS的意义,然而,它以前受到MRI分辨率的限制。只有直径较大的PVS是可见的,而且大多数研究主要集中在扩大的PVS的潜在致病性上。由于7特斯拉(7T)MRI的分辨率和信噪比(SNR)较高,可以检测到更多的小尺寸PVS,PVS的数量明显高于传统的1.5或3T MRI研究。
因此,在神经退行性疾病的研究中也应考虑到小尺寸的PVS,与以往的研究相比,这可能改变PVS负担和临床特征之间的相关性。
藉此,浙江大学的Ting Shen1等人比较了:早期PD的PVS负担与健康对照组(HCs)的PVS负担,其中包括较小PVS的影响。
他们对7T MRI图像上的PVS负担进行了定量评估,以探索PVS的流行率,并描述PVS负担与临床和影像特征的相关性模式,以进一步了解其在PD中的病理生理机制。
他们招募了40名早期PD患者和41名健康对照组(HCs)。通过计算PVS的数量和体积,以评估7T磁共振成像图像上的PVS负担。
他们还比较了PD和HC之间的PVS负担,并进行了PVS负担与临床和影像特征之间的部分相关分析。PD患者的BG和中脑的PVS负担明显更严重,BG的PVS数量与PD疾病的严重程度和左旋多巴等效剂量明显相关。
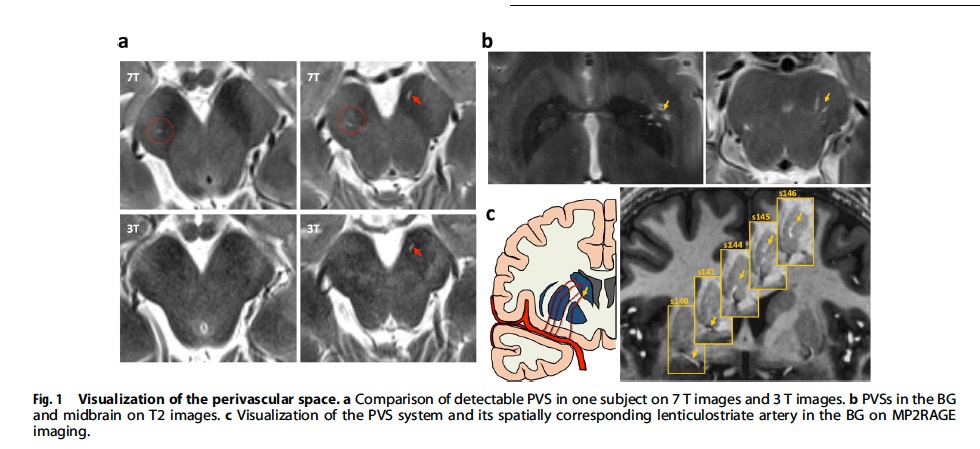
图2 PVS示意图
BG和中脑内或附近的某些皮质下核和白质纤维的各向异性和平均弥散率值与同侧PVS负担指标显著相关。
在中脑方面,双侧PVS负担的差异分别与通过双侧黑质的白纤维束的纤维数的差异相关。
我们的研究表明,PVS负担指数是评估PD运动症状严重程度的候选生物标志物,有助于预测药物剂量。该研究结果还强调了PVS负担与灰质和白质微结构之间的潜在关联性。
原文出处:
Shen T, Yue Y, Zhao S, et al. The role of brain perivascular space burden in early-stage Parkinson’s disease. npj Parkinsons Dis. 2021;7(1):12. doi:10.1038/s41531-021-00155-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#Dis#
87