间充质干细胞治疗2型糖尿病的临床进展
2023-11-07 干细胞者说 干细胞者说 发表于上海
间充质干细胞,作用是调节免疫功能,保护患者体内的β细胞,改善胰岛环境,从而减轻糖尿病症状。
全世界有4.63亿成年人 (每11人中就有1人) 患有糖尿病,预计到2045年,这一数字将达到7亿。每年有420万人死于糖尿病,我国有近1.3亿糖尿病患者。1型糖尿病占全球糖尿病病例的大约10%, 2型糖尿病占90%左右。生活方式的改变和药物治疗都是治疗2型糖尿病的有效方法,已经有很多奇迹产生。
3月10日,在CCTV12的《生命线》栏目中,中国人民解放军总医院第一医学中心内分泌科主任母义明表示,在干细胞治疗糖尿病方面已经有了大量的研究。我们已经清楚了干细胞治疗糖尿病是通过什么途径,未来我们会做得更好。
-01-
间充质干细胞治疗糖尿病的两大策略
间充质干细胞,作用是调节免疫功能,保护患者体内的β细胞,改善胰岛环境,从而减轻糖尿病症状。
间充质干细胞(Mesenchymal Stem Cells, MSCs)既能够支持、保护β细胞,可能还是β细胞的来源之一。间充质干细胞移植对2型糖尿病(T2D)患者有效,但其在1型糖尿病(T1D)患者中的疗效还存在争议,因为间充质干细胞在体外分化为功能性β细胞的能力较差,且在体内没有发生转分化。
-02-
间充质干细胞的糖尿病治疗
间充质干细胞,是目前临床试验中应用最广泛的干细胞。间充质干细胞可以从成体组织中获得,也可以从新生儿组织中获得。一般认为,间充质干细胞具有三系分化潜能,即体外分化为成骨细胞(骨组织)、软骨母细胞(软骨)和脂肪细胞(脂肪组织)的能力。
从监管的角度来看,间充质干细胞已被归类为高级治疗药物产品。尽管,间充质干细胞正成为“通用型”细胞治疗中最有前景的细胞来源,但其在1型糖尿病临床试验仍存在很大争议。
间充质干细胞治疗糖尿病,临床上有三种不同的假说:
A)使用间充质干细胞来源的胰岛前体细胞,得到功能性β细胞;
B)使用间充质干细胞在移植后,通过体内转分化直接产生β细胞;
C)使用间充质干细胞支持内源性胰岛的存活,将其诱导分化为胰岛前体细胞。
到目前为止,还缺乏强有力的证据证明间充质干细胞在体内外可分化为功能性β细胞或胰岛类器官。
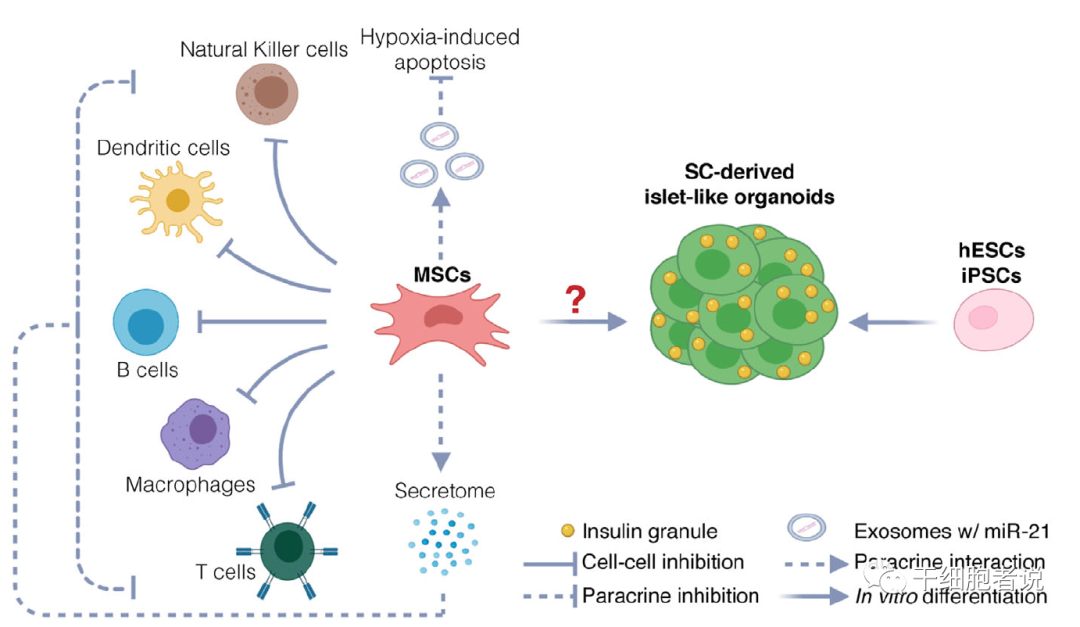
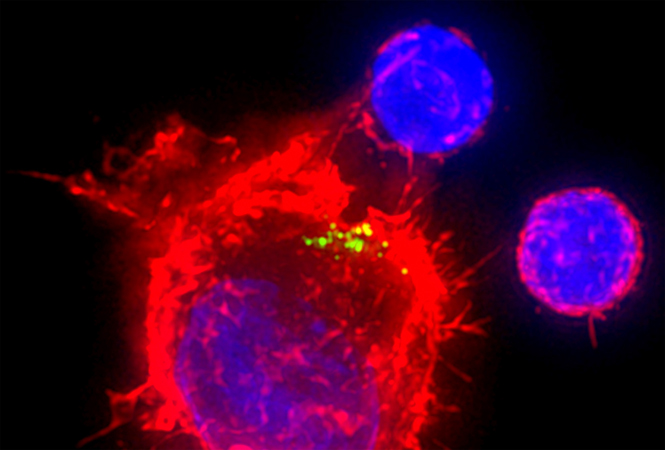
干细胞治疗糖尿病潜在的治疗机制。潜在的机制包括了保护内源性胰岛和恢复β细胞两种。MSCs通过免疫调节和抑制缺氧诱导的细胞凋亡来保护内源性β细胞。hESC和iPSC也用于产生功能性胰岛样类器官以恢复β细胞功能。
▉ 机制一:间充质干细胞转化成β细胞(证据不足)
间充质干细胞是否会分化为胰岛素生成细胞?通常,通过体外葡萄糖刺激胰岛素分泌和体内小鼠的葡萄糖耐量,来测试间充质干细胞来源的胰岛素生成细胞的功能。
C肽是胰岛素产生过程中的副产物,和胰岛素同来自于胰岛素原。C肽通常作为体内胰岛素分泌的指标<如果测试的指标使用胰岛素,而不是C肽,那么β细胞响应葡萄糖分泌胰岛素的能力常常会被高估。因为胰岛素的量可能并不代表真正的胰岛素产生,培养基中通常也有胰岛素的存在>。
一项研究显示,在体外葡萄糖刺激下的C肽分泌量上升了4倍,这提示:间充质干细胞可能分化为能够响应葡萄糖刺激的胰岛素生成细胞。葡萄糖耐量试验表明,将其移植到胰腺切除或链脲佐菌素(STZ)诱导的糖尿病小鼠后,尽管结果不够理想,但仍有一定的降糖能力。Kamalveni等人,使用了人脐带血间充质干细胞(UCB-MSC)来源的胰岛内生成细胞进行移植,在移植后60天能检测到低水平的人源C肽。虽然移植后150天,仍然可以检测到人源C肽,但这一范围是高度变化的(0.0-7.97pmol/ml),无法达到治疗目的,无法将糖尿病小鼠的血糖维持在正常水平。这表明诱导间充质干细胞产生成熟的胰岛素生成细胞,效率低下。
总而言之,间充质干细胞可分化为β细胞的证据严重不足。
▉ 机制二:间充质干细胞改善胰岛微环境和免疫调节
另一方面,过去15年中进行的临床前研究支持间充质干细胞通过两种不同的机制保护胰岛移植物,即改善细胞存活环境和免疫调节。
早在2012年,Ezquer等的研究表明,向STZ诱导糖尿病小鼠的静脉中注射小鼠间充质干细胞可以改善其血糖水平,将糖化血红蛋白降低到与非糖尿病小鼠相似的水平,并提高总胰岛素水平。荧光检测证实,间充质干细胞不能分化为胰岛素生成细胞,而是通过Treg细胞,增加IL-13等抗炎细胞因子,降低促炎细胞因子(IL-1β、IL-18、TNF-α和MCP-1等)表达。
数据表明,间充质干细胞治疗的部分有益作用是通过减轻炎症来实现的。
-03-
近2年基于间充质干细胞的临床研究
1. 2022年10月北京大学深圳医院内分泌科的研究团队在SCI期刊《World journal of diabetes(世界糖尿病杂志)》上发表了题为:Effectiveness and safety of human umbilical cord-mesenchymal stem cells for treating type 2 diabetes mellitus(人脐带间充质干细胞治疗2型糖尿病的有效性和安全性)的研究论文,并表明人脐带间充质干细胞治疗可能是2型糖尿病的新疗法。
16名入选患者(入选标准为2型糖尿病诊断,年龄在18岁到70岁之间,HbA1c糖化血红水平在7%到9.5%之间)共接受三次脐带间充质干细胞输注,三次之间间隔各一周,每次输注数量为1×106/kg。
在随访期间,参与者每周7次自我监测空腹血糖和餐后2小时血糖,同时根据患者的血糖调整口服降糖药和胰岛素的剂量,以保持水平稳定。所有患者在16周后再次接受医学评估。
研究结果提示:血糖指标显著改善,胰岛β细胞功能改善,降糖药的用量减少

2. 2023年,《干细胞转化医学》刊登了母义明教授发表的关于通过回顾性连续血糖监测评估UC-MSCs治疗2 型糖尿病的疗效研究数据。
在这个随机安慰剂对照的试验中,2015年10月至2018年12月期间共有73名患者被分配接受4代UC-MSCs(n=37)或安慰剂(n=36)的静脉输注,每次输注数量为1×106/kg,每4周输注一次,共输注3次,并随访48周。在主要终点评估TIR和糖化血红蛋白(HbA1c)的变化。
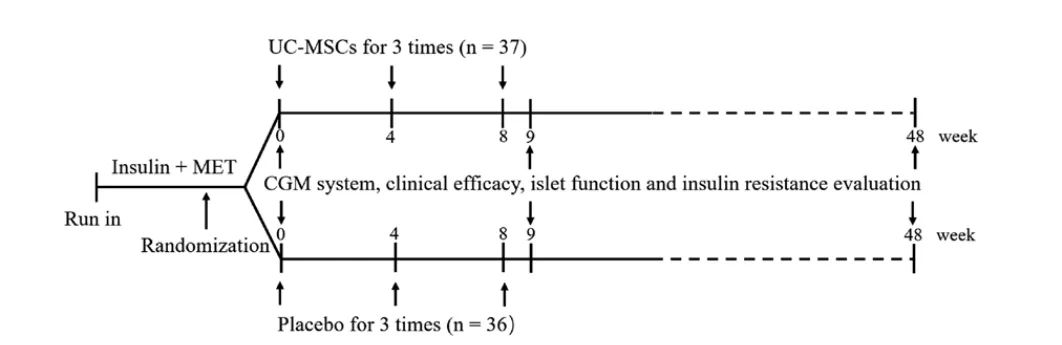
研究设计,MET,二甲双胍;UC-MSC,脐带来源的间充质干细胞;CGM,连续血糖监测
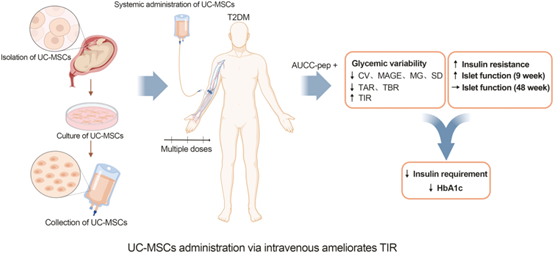
有效性:这项前瞻性、单中心、随机、双盲、安慰剂对照试验表明,静脉输注 UC-MSCs 可以增加TIR,减轻血糖变异性,降低HbA1c水平,减少每日胰岛素需要量,改善胰岛β-细胞功能并改善胰岛素抵抗。 AUCC-pep 是与接受UC-MSCs干预的T2D 疗效相关的独立危险因素,男性患者更有可能从 UC-MSCs治疗中受益。
Liu X、Kong D进行的三项开放标签临床研究初步证实了UC-MSCs治疗T2D的功效。这些观察结果一致,这项结果也表明静脉输注UC-MSCs减少了HbA1c和胰岛素消耗,强调UC-MSC疗法在治疗T2D中的效果。
安全性:一名女性患者在第3次UC-MSCs输注后1个月出现脑梗塞。一名男性患者在第三次UC-MSCs输注后3个月因意外导致股骨颈骨折。根据独立评审委员会的判断,这些事件不被认为与 UC-MSCs治疗相关。
-04-
二点思考
一、间充质干细胞的临床试验,一般是静脉给药。治疗作用机制:通过间接方式支持胰岛的健康和生存(即改善胰岛微环境和调节免疫),有益作用是通过减轻炎症来实现的。间充质干细胞治疗2型糖尿病临床试验,可有效降低血糖水平、减少外源的胰岛素使用剂量,但疗效并未达到预期且不持续。那么,间充质干细胞静脉注射是治疗2型糖尿病的理想选择吗?
二、新冠后血糖异常人群增加,据多内分泌科医生提出2023年血糖异常或者糖尿病患者增多(非官方,目前没有公开数据),那是否考虑是新冠病毒给人体免疫或者内分泌造成了一定影响而造成胰岛损伤,比如引发了炎症反应后造成了损伤,引起了血糖异常?
希望医生朋友们踊跃讨论+探索,因为研发要符合临床需求才更有实用价值!
部分参考资料:
[1]https://www.frontiersin.org/articles/10.3389/fendo.2021.631463/full
[2]Stem cell therapies for Type 1 diabetes: current status and proposed road map to guide successful clinical trials
[3]https://viacyte.com/
[4]https://doi.org/10.3389/fimmu.2022.869514
[5]Stem Cell Therapies for Treating Diabetes;Progress and RemainingChallenges
[6]Liu X, Zheng P, Wang X, et al. A preliminary evaluation of efffcacy and safety of Wharton’s jelly mesenchymal stem cell transplantation in patients with type 2 diabetes mellitus. Stem Cell Res Ther. 2014;5(2):57. https://doi.org/10.1186/scrt446
[7]Kong D, Zhuang X, Wang D, et al. Umbilical cord mesenchymal stem cell transfusion ameliorated hyperglycemia in patients with type 2 diabetes mellitus. Clin Lab. 2014;60(12):1969-1976. https:// doi.org/10.7754/clin.lab.2014.140305
[8]LiZang , YijunLi , Haojie Hao.Efficacy of umbilical cord-derived mesenchymal stem cells in the treatment of type 2 diabetes assessed by retrospective continuous glucosemonitoring,Stem Cells Translational Medicine, 2023
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习了,谢谢分享
77