Adv Sci:南京医科大学顾爱华/同济大学蒋兆彦合作构建siRNA/CS-PLGA纳米颗粒系统降低肠道脂质摄取并缓解肥胖
2024-09-23 iNature iNature 发表于上海
该研究发现肠道特异性SOAT2敲除(Soat2I-KO)小鼠能够防止由于肠道脂质吸收减少而导致的饮食诱导性肥胖的发展。
有效抑制肠道脂质吸收是治疗脂质代谢相关疾病的有效策略。甾醇O-酰基转移酶2(SOAT2)负责将游离胆固醇和脂肪酸酯化为胆固醇酯。
2024年9月19日,南京医科大学顾爱华、同济大学蒋兆彦共同通讯在Advanced Science 在线发表题为“siRNA/CS-PLGA Nanoparticle System Targeting Knockdown Intestinal SOAT2 Reduced Intestinal Lipid Uptake and Alleviated Obesity”的研究论文。该研究发现肠道特异性SOAT2敲除(Soat2I-KO)小鼠能够防止由于肠道脂质吸收减少而导致的饮食诱导性肥胖的发展。
构建了Soat2 siRNA/CS-PLGA纳米颗粒系统以实现肠道递送和抑制Soat2。该纳米颗粒系统由PLGA-block-PEG和壳聚糖组成,可特异性地将Soat2 siRNA递送到小鼠小肠中,有效抑制肠道脂质吸收并解决肥胖问题。在揭示肠道SOAT2调节脂肪酸吸收的潜在机制时,发现SOAT2抑制后肠细胞中的CD36泛素化降解增强。游离胆固醇酯化不足会促进内质网应激和E3连接酶RNF5的募集,从而激活SOAT2敲低肠细胞中的CD36泛素化。这项研究证明了肠道SOAT2对脂质摄取的潜在调节功能,突出了通过靶向肠道SOAT2对肥胖症的治疗效果,在基于siRNA疗法的肥胖症治疗中表现出良好的转化相关性。

近几十年来,肥胖被认为是一种流行的代谢紊乱,伴有血脂异常、高血糖、胰岛素抵抗等。高热量食物摄入的增加加上身体活动的减少导致能量失衡,在导致肥胖发展中起着关键作用。限制外源性脂肪摄入、抑制脂肪酸合成和通过β-氧化增强脂肪酸降解是预防肥胖发展的建议方法。胃肠道是膳食脂肪摄入的第一道大门。各种研究都试图找出针对肠道脂肪酸吸收的化合物。依折麦布是一种广泛使用的药物,靶向肠细胞中的胆固醇转运蛋白NiemanPickC1like1(NPC1L1)蛋白来控制胆固醇水平。随着低密度脂蛋白胆固醇(LDL-C)水平降低25%,依折麦布/他汀类药物联合治疗也被证明可以阻止肥胖相关疾病的进展,表明其在限制肠道脂肪酸吸收方面发挥着作用。虽然脂肪酸在肠细胞中的吸收的分子过程——膜吸收、细胞内运输和甘油三酯组装——已被阐明,但迄今为止还没有特定的抑制剂被证明能通过抑制脂肪酸吸收来有效预防肥胖。
甾醇O-酰基转移酶2(SOAT2,以前也称为酰基辅酶A:胆固醇酰基转移酶,ACAT2)是一种将游离胆固醇和脂肪酸酯化为胆固醇酯(CE)的酶,优先使用油酸和棕榈酸作为底物。由于其在肝细胞和肠细胞中的独特存在以及在极低密度脂蛋白/乳糜微粒-CE合成中的作用,其与动脉粥样硬化发展的关系已被广泛研究。特别是,抑制肝脏SOAT2已被证明可以预防动脉粥样硬化的发展。由于SOAT2在CE产生中的作用以及对动脉粥样硬化的关注,其在调节脂肪酸代谢中的作用在某种程度上被忽视了,人们只担心肝脏中SOAT2的抑制会意外地导致甘油三酯积累增加。在饲喂高脂饮食(HFD)的SOAT2全基因敲除小鼠中,肝脏甘油三酯积累和胰岛素抵抗得到改善。尽管有限,这些证据提示肠道SOAT2在控制膳食脂肪酸吸收中的作用,这暗示肠道SOAT将成为调节饮食诱导肥胖发病率的一个有希望的靶点。
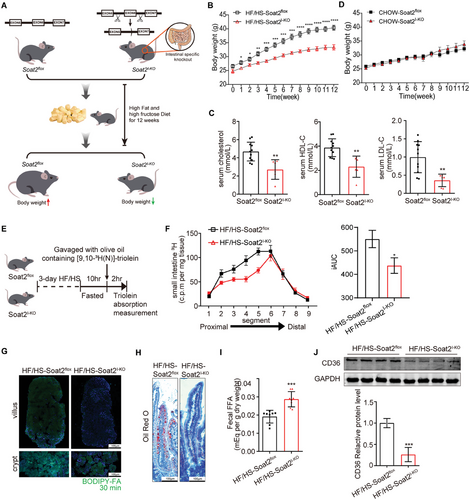
肠道中SOAT2的缺失通过减少肠道脂质吸收来防止饮食诱导的肥胖(图源自Advanced Science )
美国食品药品监督管理局(FDA)首次批准小干扰RNA(siRNA)药物(patisiran)用于治疗遗传性转甲状腺素蛋白介导(hATTR)淀粉样变性,开启了纳米载体辅助siRNA治疗的新纪元。纳米粒子是增强药物输送和治疗效果的载体。聚乳酸-乙醇酸共聚物(PLGA)纳米粒子已被用作结直肠癌治疗中输送siRNA的合适载体。细胞可以内化PLGA纳米粒子(NPs),从而将功能性siRNA释放到细胞质中。用高亲和力分子(如抗体)涂覆纳米粒子,使它们能够靶向细胞表面异常表达的分子。涂层材料壳聚糖(CS)的正电特性有助于纳米系统对带负电荷的肠粘膜的吸引力,从而有效地将siRNA输送到肠道。由于其在siRNA递送和细胞靶向方面的功效,一种靶向肠细胞中SOAT2的CS涂层新型PLGA-siRNA将成为调节肠道脂肪酸吸收以防止肥胖的有前途的治疗选择。
在本研究中,作者构建了一种由壳聚糖组成的新型纳米颗粒系统,用于在肠道内递送Soat2 siRNA。纳米配方的Soat2 siRNA/CS-PLGA纳米颗粒可以通过CS的正电荷被带负电荷的肠粘膜吸引,使其保留在肠道中并促进siRNA递送到肠上皮。用Soat2 siRNA/CS-PLGA纳米颗粒治疗能够抑制肠细胞中的SOAT2,这足以防止高脂饮食引起的肥胖症的发展。作者进一步证明,Soat2 siRNA抑制限制肠细胞脂肪酸吸收的治疗效果是由于肠细胞中脂肪酸转运蛋白CD36的泛素化相关降解增强。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202403442
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#肥胖# #siRNA/CS-PLGA纳米颗粒系统#
42